Cho hổn hợp hai kim loại kiềm kế tiếp nhau tác dụng với nước , thu được dd X và 36ml khi hidro ở (đktc) cho dd X tác dụng HCl thu được 2,075g
a, tìm kim loại
b, tìm % khối lượng mỗi kim loại
Cho 8,15g hỗn hợp 2 kim loại kiềm thổ kế tiếp tác dụng với dd HCl 10% vừa đủ thu được dung dịch X và 5,6 lít khí ở đktc. Tìm tên hai kim loại và tính C% các chất trong dd X
Gọi kim loại kiềm thổ chung là R.
\(R+2HCl\rightarrow RCl_2+H_2\)
0,25 0,25
\(\Rightarrow M_R=\dfrac{8,15}{0,25}=32,6\)
\(\Rightarrow R_1< 32,6< R_2\)
Mà hai kim loại nằm ở 2 chu kì liên tiếp nên:
\(\left\{{}\begin{matrix}R_1:24\left(Mg\right)\\R_2:40\left(Ca\right)\end{matrix}\right.\)
Cho 3,1 g hỗn hợp gồm hai kim loại kiềm ở hai chu kì kế tiếp nhau trong bảng tuần hoàn tác dụng hết với nước thu được 1,12 lít H2 ở đktc và dung dịch kiềm. Tính thể tích dd HCl 2M cần dùng để trung hòa dd kiềm và khối lượng muối clorua thu được.
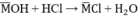
Theo pt: nHCl = nMOH = 0,1 (mol)
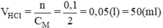
m(MCl) = 0,1.(31 + 35,5) = 6,65(g)
4. Cho 1,28 gam hỗn hợp hai kim loại kiềm ở 2 chu kỳ kế tiếp nhau tác dụng hết với nước thu được 0,896 lít khi hidro ở đktc. Xác định 2 kim loại kiềm
Gọi công thức chung của 2 kim loại là A
\(n_{H_2}=\dfrac{0,896}{22,4}=0,04\left(mol\right)\)
PTHH: 2A + 2H2O --> 2AOH + H2
_____0,08<-----------------------0,04
=> \(\overline{M}_A=\dfrac{1,28}{0,08}=16\left(g/mol\right)\)
=> 2 kim loại đó là Li và Na
giải giúp em câu này: cho 8,3g hai kim loại kiềm kế tiếp nhau tác dụng với 100g dd HCl 3,65% thu được dd X. Cho MgCl2 dư vào dd X thì thu được 4,35g kết tủa .Hai kim loại đó là?
trong SGK có bài này mà hình như mik lm òi
1.so mol ↓ chinh la so mol cua Mgoh2 va =0,075 mol.so mol HCl la 0,1 mol goi kim loai trung binh la M:M +HCl -> MCl +1/2H2
M + H2O -> MOH +1/2H2
so mol MOH la :0,075.2=0,15 mol =>so mol cua M la 0,15+0,1=0,25 mol => M=8,3/0,25=33,2=>2 hai kim loại kiềm kế tiếp do la Na va kali .
Cho 6,5 g hỗn hợp hai kim loại kiềm thổ thuộc 2 chu kì kế tiếp nhau trong bảng tuần hoàn tác dụng vừa đủ với dung dịch HCl thu được 4,48 lít khí H2 (đktc).
a) Tìm hai kim loại.
b) Tim khối lượng của mỗi kim loại trong hỗn hợp.
=> CHỈ VỚI
a, Đặt kim loại trung bình là R \(\rightarrow \) R hóa trị II
\(PTHH:R+2HCl\to RCl_2+H_2\\ \Rightarrow n_R=n_{H_2}=\dfrac{4,48}{22,4}=0,2(mol)\\ \Rightarrow M_R=\dfrac{6,5}{0,2}=32,5(g/mol)\)
Vậy 2 KL đó là Mg (24) và Ca (40)
\(b,\) Đặt \((n_{Mg};n_{Ca})=(x;y)(mol)\)
\(\Rightarrow \begin{cases} 24x+40y=6,5\\ x+y=n_{H_2}=0,2 \end{cases}\Rightarrow \begin{cases} x=0,09375(mol)\\ y=0,10625(mol) \end{cases}\\ \Rightarrow \begin{cases} m_{Mg}=2,25(g)\\ m_{Ca}=4,25(g) \end{cases}\)
Cho 7,1 gam hỗn hợp gồm kim loại kiềm X và một kim loại kiềm thổ Y tác dụng hết với lượng dư dd HCl loãng, thu được 5,6l khí (đktc). Kim loại X, Y là:
A. Natri , magie
B. Liti và beri
C. Liti và beri
D. Kali , bari
Đáp án A
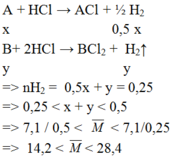
Chỉ có cặp nghiệm A = 23 (Na ) , B = 24 (Mg) thỏa mãn
Cho hh 2 kim loại liên tiếp nhau trong nhóm II A tác dụng với HCl dư. Sau phản ứng khối lượng dd tăng 0,82g. Cô cạn dd sau phản ứng thu được 1,915g hh 2 muối. Tìm 2 kim loại và khối lượng mỗi kim loại.
Gọi CTTQ hai kim loại là R
Gọi $n_{H_2} = a(mol)$
$R + 2HCl \to RCl_2 + H_2$
Theo PTHH :
Ta có :
$Ra - 2a = 0,82$
$a(R + 71) = 1,915$
Suy ra : a = 0,015 ; Ra = 0,85
$m_{hai\ kim\ loại} = Ra = 0,85(gam)$
$\Rightarrow R = \dfrac{0,85}{0,015} = 56,67$
Vậy hai kim loại là Canxi và Stronti
Cho 3,1 g hỗn hợp gồm hai kim loại kiềm ở hai chu kì kế tiếp nhau trong bảng tuần hoàn tác dụng hết với nước thu được 1,12 lít H2 ở đktc và dung dịch kiềm. Xác định tên 2 KL đó và tính thành phần phần trăm khối lượng mỗi kim loại
Gọi công thức chung cho hai kim loại kiềm là M
Số mol H2: nH2 = 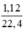 = 0,05(mol)
= 0,05(mol)
PTHH: 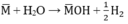
Theo pt: nM = 2. nH2 = 2. 0,05 = 0,1(mol)
⇒ M = 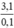 = 31 → Na, K
= 31 → Na, K
Gọi x, y lần lượt là số mol của Na và K trong hỗn hợp
Theo bài ra ta có hệ phương trình:
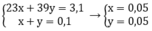
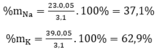
Cho 3,1 gam hỗn hợp gồm hai kim loại kiềm ở hai chu kì kế tiếp nhau trong bảng tuần hoàn tác dụng hết với nước thu được 1,12 lít H2 ở đktc và dung dịch kiềm.
a) Xác định tên hai kim loại đó và tính thành phần phần trăm khối lượng mỗi kim loại.
b) Tính thể tích dung dịch HCI 2M cần dùng để trung hoà dung dịch kiềm và khối lượng hỗn hợp muối clorua thu được.
a) Gọi công thức chung của 2 kim loại kiềm là M
2M + 2H2O → 2MOH + H2
nH2nH2 = 0,05 mol ⇒ nM= 2nH2 =0,1 mol
⇒ M = 3,1/0,1= 31 (g/mol); Vậy 2 kim loại đó là Na (23) và K (39)
Gọi x là số mol kim loại Na, ⇒ nK = 0,1 – x (mol)
ta có: m hỗn hợp = mNa + mK
⇔ 3,1 = 23x + 39(0,1 - x)
⇒ x = 0,05 mol
%mNa=mNa/mhh*100%=23*0,05/3,1*100%*100%= 37,1%;
% mK = 100% - 37,1% = 62,9%.
b) HCl + MOH → MCl + H2O
nHCl =nMOH = 0,1 mol ⇒Vdung dịch HCl = n/CM=0,1/2=0,05lítnCM=0,12=0,05lí
mhh muối= mKL + mCl= 3,1 + 35,5.0,1= 6,65 (gam)
a. Gọi công thức chung cho hai kim loại kiềm là M
Số mol H2: nH2 = 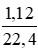
PTHH:
Theo pt: nM = 2. nH2 = 2. 0,05 = 0,1(mol)
⇒ M = 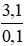
Gọi x, y lần lượt là số mol của Na và K trong hỗn hợp
Theo bài ra ta có hệ phương trình:
b.
Theo pt: nHCl = nMOH = 0,1 (mol)
m(MCl) = 0,1.(31 + 35,5) = 6,65(g)