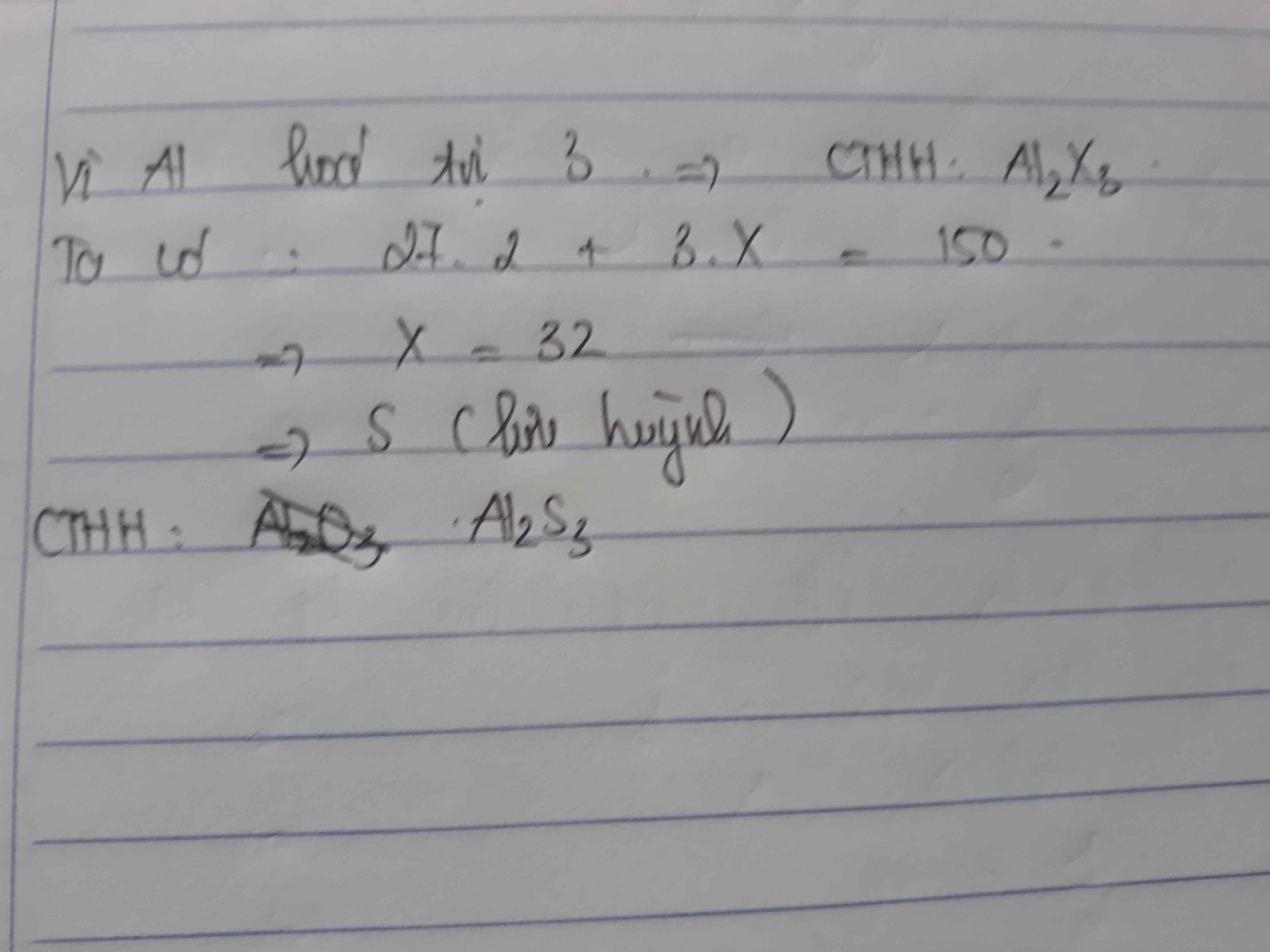a. Một nguyê tử X có thể tạo thành với Al hợp chất kiểu AlaXb, mỗi phân tử gồm 5 nguyên tử, khối lượng phân tử 150đvC. Xác định X, gọi tên hợp chất AlaXb.
b. Y là một oxit kim loại chứa 70% kim loại ( về khối lượng). Cần dùng bao nhiêu ml dd H2SO4 24,5% (d= 1,2g/ml) để hòa tan vừa đủ 40,0 gam Y

Những câu hỏi liên quan
mọt nguyên tố X có thể tạo thành với Al hợp chất kiểu AlaXb : một phân tử gồm 5 nguyên tử ,khối lượng phân tử là 150đvC .xác đinh x ,ghi CTHH của hợp chất
vì nhôm (Al) hóa trị 3 nên hợp chất có dạng :\(Al_aX_3\) gồm 5 nguyên tử \(\Rightarrow a=5-3=2\) \(Al_2X_3\)
\(\Rightarrow\) X có hóa trị 2
\(M=27.2+X.3=150\)
\(\Rightarrow X=32\) => Lưu huỳnh ( S) thõa mãn hóa trị 2.
CTHH của hợp chất \(Al_2S_3\) ( nhóm sulfua ) .
Đúng 1
Bình luận (1)
công thức hh dạng: AlaXb mà 1 ptử của nó có 5 ngtử
ta có Al hóa trị 3 nên có tối đa 2 ngtử Al trong AlaXb
theo bài ra ta có: 27.2 + 3.X =150 => X = 32 = S(lưu huỳnh)
cthh là Al2S3
Đúng 0
Bình luận (0)
Ta có a + b = 5 \Rightarrow a = 5 - b
Ta có : Al5−bXb=150
27(5−b)+Xb=150
\Rightarrow b(X−27)=15
Nếu b = 1 \Rightarrow X = 42 ( loại)
Nếu b = 2 \Rightarrow X = 34,5 (loại)
Nếu b = 3 \Rightarrow X = 32 ( X là lưu huỳnh)
Vậy CTPT của hợp chất là
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
nguyên tố X có thể tạo thành với Al hợp chất kiểu AlaXb mỗi phân tử gồm 5 nguyên tử, khối lượng phân tử 150. Xác định X
1 nguyên tố X có thể tạo thành với Al hợp chất AlaXb ; một phân tử gồm 5 nguyên tử ,khối lượng của phân tử là150 đvC
Al luôn hóa trị 3, các NTHH có hóa trị từ 1->7
+ TH1: X(I)=> có 4 nguyên tử (loại)
+TH2:X(II)=> có 5 nguyên tử(chọn)
+TH3:X(III)=>có 2 nguyên tử (loại)
+TH4:X(IV)=>có 7 nguyên tử(loại)
+TH5:X(V)=> có 8 nguyên tử (loại)
+TH6:X(VI)=> có 3 nguyên tử (loại)
+TH7LX(VII)=>có 10 nguyên tử(loại)
=> Al2X3
ta có:
150=2.27+3.X=54+3X
=>X=32=>X là S
Đúng 0
Bình luận (0)
1) Oxit kim loại ở mức hóa trị thấp chứa 22,56% O, còn oxit của kim loại đó ở mức hóa trị cao chứa 50,48% O. Xác định kim loại đó.2)hợp chất A có công thức hóa học RX2 trong đó R chiếm 63,22% về khối lượng trong hạt nhân của nguyên tử R có số hạt không mang điện nhiều hơn số hạt mang điện là 5 hạt trong hạt nhân nguyên tử X có số hạt mang điện bằng số hạt không mang điện.Tổng số hạt p trong phân tử RX2 là 41 hạt. tìm CTHH của hợp chất A3) một hợp chất hữu cơ có thành phần khối lượng các nguyên t...
Đọc tiếp
1) Oxit kim loại ở mức hóa trị thấp chứa 22,56% O, còn oxit của kim loại đó ở mức hóa trị cao chứa 50,48% O. Xác định kim loại đó.
2)hợp chất A có công thức hóa học RX2 trong đó R chiếm 63,22% về khối lượng trong hạt nhân của nguyên tử R có số hạt không mang điện nhiều hơn số hạt mang điện là 5 hạt trong hạt nhân nguyên tử X có số hạt mang điện bằng số hạt không mang điện.Tổng số hạt p trong phân tử RX2 là 41 hạt. tìm CTHH của hợp chất A
3) một hợp chất hữu cơ có thành phần khối lượng các nguyên tố như sau 85,7% C;14,3% H biết phân tử hợp chất nặng gấp 28 lần phân tử hidro.tìm CTHH của hợp chất đó
3. Khối lượng mol của hợp chất đó là :
2.28 = 56 (g/mol)
mC = \(\frac{56.85,7}{100}\approx48\left(g\right)\)
mH = 56 - 48 = 8 (g)
nC = \(\frac{48}{12}=4\left(mol\right)\)
nH = \(\frac{8}{1}=8\left(mol\right)\)
Vậy công thức hóa học là C4H8.
Đúng 0
Bình luận (0)
Nguyên tố X có thể tạo thành với Al hợp chất kiểu AlaXb,mỗi phân tử gồm 5 nguyên tử,phân tử khối 150.Hỏi X là nguyên tố gì?
Trả lời
Ta thấy:
a + b = 5
Đặt trường hợp thôi
1. Với a = 1 => b = 4 => Mx = 30.75
2. Với a = 2 => b = 3 => Mx = 32
3. Với a = 3 => b = 2 => Mx = 13.8
4. Với a = 4 => b = 1 => Mx = 42.
Trong 4 trường hợp thì trường hợp 2 có M = 32 là của Lưu huỳnh (S)
=> Hợp chất có công thức Al2S3.
Đúng 0
Bình luận (0)
Cho kim loại X tạo ra hợp chất XSO4, biết khối lượng phân tử là 120 amu. Xác định tên kim loại X ?
Gọi khối lượng nguyên tử của `X` là `x`
Ta có:
`\text {PTK =} x+32+16*4=120 <am``u>`
`-> x+32+64=120`
`-> x=120 - (32+64)`
`-> x=120-96`
`-> x=24`
Ta có: `x` có khối lượng nguyên tử là `24 am``u`
`->` `X` là nguyên tố \(\text{Magnesium (Mg)}\).
Đúng 2
Bình luận (0)
. Một nguyên tử X kết hợp với 2 nguyên tử O tạo thành hợp chất oxit. Trong phân tử oxit đó oxi chiếm 50% về khối lượng. Xác định tên của nguyên tố X và công thức hóa học của hợp chất?
Gọi công thức tổng quát là $XH_4$
\(\%H=25\%\\ \Rightarrow \dfrac{4}{X+4}.100\%=25\%\\ \Rightarrow X=12\\ Tên:\ Cacbon\\ CTHH:\ CH_4\)
Đúng 0
Bình luận (0)
nguyên tố R phản ứng với lưu huỳnh tạo thành hợp chất RaSb : một phân tử có 5 nguyên tử ,khối lượng phân tử là 150đvC .xác đinh x
Theo đề ta có a+b = 5
Lưu huỳnh có 3 hoá trị II, IV và VI
Nếu S(VI) => a + b > 5 (loại)
Nếu S(IV)
=> công thức hoá học có dạng R4S
Theo cách tính PTK ta có:
4MR + 32 = 150
=> MR = 29,5 (ko có)
Vậy S(II)
=> công thức hoá học có dạng R2S3
Theo cách tính PTK ta có:
2MR + 32.3 = 150
=> MR = 27 (Al)
Vậy công thức hoá học hợp chất là Al2S3
Đúng 0
Bình luận (0)
Hợp chất X được tạo tạo thành từ kim loại Y và oxy
TP của oxi là 36,78%
a) Xác định kim loại của y
b) Tính phân tử khối của hợp chất x
a) CTHH: AxOy
\(\%O=\dfrac{16y}{x.M_A+16y}.100\%=36,78\%\)
=> \(16y=0,3678x.M_A+5,8848y\)
=> \(M_A=\dfrac{27,5y}{x}=13,75.\dfrac{2y}{x}\left(g/mol\right)\)
Có: \(\dfrac{2y}{x}=4\) thỏa mãn
=> MR = 55 (g/mol)
=> R là Mn (Mangan)
\(\dfrac{x}{y}=\dfrac{1}{2}\) => Chọn x = 1; y = 2
CTHH: MnO2
b) PTKX = 55 + 16.2 = 87 (đvC)
Đúng 2
Bình luận (0)