Khi phân tích hợp chất sắt sunfua thì thành phần của nó chứa 63,64% Fe về khối lươngj.Tìm hóa trị của sắt trong hợp chất sunfua

Những câu hỏi liên quan
Hợp chất sắt sunfua có chứa 63,64% Fe và 36,36% S. a) Xác định cthh của hợp chất sắt sunfua. b) viết PTHH tạo thành sắt sunfua từ hai chất ban đầu Fe và S.c) Trộn 11,2 gam Fe với 8 gam S rồi đun nóng đến khi phản ứng xảy ra hoàn toàn.Tính khối lượng chất sinh ra và khối lượng chất còn dư sau pư(nếu có).
Công thức: FexSy
Ta có :
\(\frac{56x}{56x+64y}.100\%\)= 63,64%
⇒ x=1; y=1
PTHH:
Fe+ S→ FeS
nFe= 0,2 mol
nS= 0,25 mol
Ta thấy:
0,2/1<0,25/1
⇒ Fe hết; S dư
mFeS= 0,2.88=17,6 g
mS dư=( 0,25-0,2).32=1,6 g
Khi phân tích hợp chất sắt sunfat thì thành phần của nó chứa 63,64% Fe về khối lươngj.Tìm hóa trị của sắt trong hợp chất sunfat
sắt sunfua là hợp chất chứa 63.6% Fe và 36.4% S.Công thức hóa học của sắt sunfua là gì
CTHH của hợp chất cần tìm dạng: FexSy
Vì khối lượng của mỗi nguyên tố trong hợp chất tỉ lệ với thành phần phần trăm nên ta có:
\(x:y=\dfrac{M_{Fe}}{\%Fe}:\dfrac{M_S}{\%S}=\dfrac{56}{63,6}:\dfrac{32}{36,4}=1\)
=> x = y = 1
=> CTHH: FeS
Đúng 0
Bình luận (0)
Đốt nóng hỗn hợp bột Fe và S thu được hợp chất sắt Sunfua. Biết hai nguyên tố này kết hợp với nhau theo tỉ khối là 7 phần sắt và 4 phần lưu huỳnh. Tìm công thức hóa học đơn giản của sắt sunfua.
Gọi CTHHTQ của hc sắt sunfua là FexSy
Ta có :
\(\dfrac{mFe}{mS}=\dfrac{7}{4}< =>\dfrac{56x}{32y}=\dfrac{7}{4}< =>\dfrac{x}{y}=\dfrac{56.4}{32.7}=\dfrac{1}{1}\)
=> CTHH là FeS
Đúng 0
Bình luận (0)
Oxit là hợp chất gồm 2 nguyên tố, trong đó có 1 nguyên tố là oxi
Sunfua là hợp chất gôm 2 nguyên tố trong đó có 1 nguyên tố là lưu huỳnh.
Clorua là hợp chất gồm 2 nguyên tố, trong đó có 1 nguyên tố là clo.
Hãy lập công thức hóa học:
a) Gtri của các nguyên tố:
- Sắt (II) oxit , sắt (III) oxit và tính tp % theo khối lượng của nguyên tố sắt trong 2 loại oxit.
- Nito (I) oxit, nito (II) oxit, nito (III) oxit, nito (IV) oxit
- Sắt(II) sunfua và sắt(III) sunfua ( S có hóa trị II )
b) Tp khối l...
Đọc tiếp
Oxit là hợp chất gồm 2 nguyên tố, trong đó có 1 nguyên tố là oxi
Sunfua là hợp chất gôm 2 nguyên tố trong đó có 1 nguyên tố là lưu huỳnh.
Clorua là hợp chất gồm 2 nguyên tố, trong đó có 1 nguyên tố là clo.
Hãy lập công thức hóa học:
a) Gtri của các nguyên tố:
- Sắt (II) oxit , sắt (III) oxit và tính tp % theo khối lượng của nguyên tố sắt trong 2 loại oxit.
- Nito (I) oxit, nito (II) oxit, nito (III) oxit, nito (IV) oxit
- Sắt(II) sunfua và sắt(III) sunfua ( S có hóa trị II )
b) Tp khối lượng của các nguyên tố
- Một loại oxit lưu huỳnh chứa 50% s và một loại oxit lưu huỳnh chứa 40% s. Tính hóa trị của nguyên tố S trong mỗi loại hợp chất.
- Một loại sắt sunfua chứa 63,6% Fe và 36,4% S. Tính hóa trị của Fe trong hợp chất
Phân tích mẫu hợp chất tạo bởi 2 nguyên tố sắt và oxi.Kết quả cho thấy thành phần phần trăn theo khối lượng của Fe trong hợp chất là 72,414%
a ) Viết CTHH và tính PTK của hợp chất
b ) Xác định hóa trị của sắt trong hợp chất .
a ) Đặt công thức hóa học của hợp chất có dạng chung là FexOy.Ta có :
\(\%m_{Fe}=\frac{56x}{56x+16y}\times100\%=72,414\%\Rightarrow\frac{x}{y}=\frac{3}{4}\Rightarrow x=3\) và \(y=4\)
\(\Rightarrow\) CTHH của hợp chất là : \(Fe_3O_4.\)
\(\Rightarrow\) PTK của \(Fe_3O_4\)là \(56\times3+4\times16=232\) đvC
b ) \(Fe_3O_4=FE^{II}O^{II}.Fe_2^{III}O_3^{II}\)
\(\Rightarrow\) Trong phân tử Fe3O4 thì Fe có hóa trị II và III .
Đúng 0
Bình luận (0)
1. Biết :
- Oxit là hợp chất gồm 2 nguyên tố, trong đó có một nguyên tố là oxi.
- Sunfua là hợp chất gồm 2 nguyên tố trong đó có một nguyên tố là lưu huỳnh.
- Clorua là hợp chất gồm 2 nguyên tố trong đó có một nguyên tố là clo.
a) Lập công thức hóa học hợp chất Sắt(II) oxit, Sắt(II) oxit, nitơ oxit, sắt sunfua.
b) Lập công thức hóa học hợp chất biết một loại oxit lưu huỳnh chứa 50%S và một loại 40%S. Tính hóa trị S trong mỗi hợp chất sắt sunfua chứa 63,6%Fe và 36,4%S. Tính hóa trị Fe trong hợp c...
Đọc tiếp
1. Biết :
- Oxit là hợp chất gồm 2 nguyên tố, trong đó có một nguyên tố là oxi.
- Sunfua là hợp chất gồm 2 nguyên tố trong đó có một nguyên tố là lưu huỳnh.
- Clorua là hợp chất gồm 2 nguyên tố trong đó có một nguyên tố là clo.
a) Lập công thức hóa học hợp chất Sắt(II) oxit, Sắt(II) oxit, nitơ oxit, sắt sunfua.
b) Lập công thức hóa học hợp chất biết một loại oxit lưu huỳnh chứa 50%S và một loại 40%S. Tính hóa trị S trong mỗi hợp chất sắt sunfua chứa 63,6%Fe và 36,4%S. Tính hóa trị Fe trong hợp chất.
a. Sắt (II) Oxit: \(FeO\)
Sắt (III) Oxit: \(Fe_2O_3\)
Nito Oxit: \(N_2O\)
Sắt sunfua: \(FeS\)
b. Oxit lưu huỳnh chứa 50%S
Gọi CTHH tạm thời là: \(S_xO_y\)
Ta có: \(\dfrac{32x}{16y}=\dfrac{50\%}{50\%}\Leftrightarrow\left\{{}\begin{matrix}x=1\\y=2\end{matrix}\right.\)
\(\Rightarrow CTHH:SO_2\)
Oxit lưu huỳnh chứa 40%S
Gọi CTHH tạm thời là: \(S_xO_y\)
Ta có: \(\dfrac{32x}{16y}=\dfrac{40\%}{60\%}\Leftrightarrow\left\{{}\begin{matrix}x=1\\y=3\end{matrix}\right.\)
\(\Rightarrow CTHH:SO_3\)
Tính hóa trị S trong mỗi hợp chất sắt sunfua chứa 63,6%Fe và 36,4%S. Tính hóa trị Fe trong hợp chất.
Gọi CTHH tạm thời là: \(Fe_xS_y\)
Ta có: \(\dfrac{56x}{32y}=\dfrac{63,6\%}{36,4\%}\Leftrightarrow\left\{{}\begin{matrix}x=1\\y=1\end{matrix}\right.\)
Vậy hóa trị của Fe trong hợp chất là hai vì lưu huỳnh và Fe có nhiều hóa trị nhưng chỉ cùng có chung một hóa trị là hai.
Đúng 0
Bình luận (0)
a)Một loại sắt sunfua chứa 63,6% Fe và 36,4% S .Tính hóa trị của Fe trong hợp chất b)Một hợp chất của lưu huỳnh chứa 50% S và oxi. Tính hóa trị của S trong hợp chất đó Mong mọi người giúp e càng nhanh càng tốt
Câu a)
Gọi CTHH của sắt sunfua là $Fe_xS_y$
Ta có :
\(\dfrac{56x}{63,6}=\dfrac{32y}{36,4}\Rightarrow\dfrac{x}{y}=\dfrac{1}{1}\)
Vậy CTHH của muối là FeS
Gọi hóa trị của Fe là a
Theo quy tắc hóa trị :
a.1 = II.1 Suy ra a = II
vậy Fe có hóa trị II
Đúng 1
Bình luận (0)
Khi đốt 1 gam hỗn hợp đồng sunfua và kẽm sunfua có chứa 3,2% tạp chất không cháy, thu được một lượng khí có thể làm mất màu 100ml dung dịch iot 0,1M. Thành phần phần trăm theo khối lượng của hai muối sunfua trong hỗn hợp là? A. 19,83% và 80,17% B. 72,81% và 27,19% C. 32,18% và 67,82% D. 17,38% và 82,62%
Đọc tiếp
Khi đốt 1 gam hỗn hợp đồng sunfua và kẽm sunfua có chứa 3,2% tạp chất không cháy, thu được một lượng khí có thể làm mất màu 100ml dung dịch iot 0,1M. Thành phần phần trăm theo khối lượng của hai muối sunfua trong hỗn hợp là?
A. 19,83% và 80,17%
B. 72,81% và 27,19%
C. 32,18% và 67,82%
D. 17,38% và 82,62%
Đáp án A.
2CuS + 3O2 → 2CuO + 2SO2 ↑ (1)
(mol) a → a
2ZnS + 3O2 → 2ZnO + 2SO2 ↑ (2)
(mol) b → b
SO2 + I2 + 2H2 O → H2SO4 + 2HI (3)
(mol) 0,01 0,01
Khối lượng của hỗn hợp: ZnS và CuS là:
![]()
![]()
Gọi a là số mol của CuS và b là số mol của ZnS
Ta có: 96a + 97b = 0,968
a + b = 0,01
=> a = 0,002, b = 0,008 (mol)
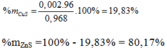
Đúng 0
Bình luận (0)




























