một nguyên tử của nguyên tố X có tổng số hạt các loại trong nguyên tử là 82 và số hạt nơtron bằng 15/13 số hạt proton. X là nguyên tố nào? viết kí hiệu hóa học của X?
Cho biết : Ca = 40, O = 16, Fe = 56, N = 14, S = 32

Những câu hỏi liên quan
Bài 1:a) Tổng số hạt Proton, Nơtron và Electron của nguyên tử một nguyên tố là 21. Kí hiệu hóa học của nguyên tố trên ?b) Tổng số hạt proton, nơtron, electron trong nguyên tử của một nguyên tố là 40. Số khối của nguyên tử là:c) Tổng số hạt proton, nơtron, electron trong nguyên tử của một nguyên tố là 16. Số khối của nguyên tử là:d) Tổng số hạt mang điện trong nguyên tử của một nguyên tố là 30. Tổng số hạt mang điện nhiều hơn hạt không mang điện là 22 hạt. Số nơtron là ?
Đọc tiếp
Bài 1:
a) Tổng số hạt Proton, Nơtron và Electron của nguyên tử một nguyên tố là 21. Kí hiệu hóa học của nguyên tố trên ?
b) Tổng số hạt proton, nơtron, electron trong nguyên tử của một nguyên tố là 40. Số khối của nguyên tử là:
c) Tổng số hạt proton, nơtron, electron trong nguyên tử của một nguyên tố là 16. Số khối của nguyên tử là:
d) Tổng số hạt mang điện trong nguyên tử của một nguyên tố là 30. Tổng số hạt mang điện nhiều hơn hạt không mang điện là 22 hạt. Số nơtron là ?
Cho biết tổng số các hạt proton, nơtron, electron tạo nên một nguyên tử một nguyên tố bằng 49, trong đó số hạt không mang điện là 17. Viết tên, kí hiệu hóa học và nguyên tử khối của nguyên tố.
Nguyên tố này là lưu huỳnh, kí hiệu S, nguyên tử khối là 32 đvC.
Đúng 0
Bình luận (0)
nguyên tử của một nguyên tố X có tổng số hạt proton và nơtron là 35. Hiệu số hạt nơtron và proton là 1. Viết kí hiệu nguyên tử
nguyên tử x có tổng số proton . số electron , số nơtron là 52 . biết số hạt không mang điện nhiều hơn số hạt mang điện trong hạt nhân là 1 a) tìm số proton , số electron , số nơ tron của x ,b) nguyên tử x thuộc nguyên tố hóa học nào , viết kí hiệu hóa học
1. Viết kí hiệu nguyên tử X (theo đúng tên nguyên tố) trong các trường hợp sau:a) Nguyên tử X có 15e và 16n.b) Nguyên tử X có tổng số hạt proton và nơtron là 35, hiệu số hạt nơtron và proton là 1.c) Nguyên tử X có số hạt ở vỏ là 15 và số hạt ở nhân là 31.d) Nguyên tử X có điện tích hạt nhân là 19+ và số nơtron nhiều hơn số proton là 1 hạt.e) Nguyên tử X có tổng số hạt trong nguyên tử là 58. Biết rằng số hạt không mang điện nhiều hơn số hạt mang điện âm là 4.f) Nguyên tử X có tổng số hạt p, n, e...
Đọc tiếp
1. Viết kí hiệu nguyên tử X (theo đúng tên nguyên tố) trong các trường hợp sau:
a) Nguyên tử X có 15e và 16n.
b) Nguyên tử X có tổng số hạt proton và nơtron là 35, hiệu số hạt nơtron và proton là 1.
c) Nguyên tử X có số hạt ở vỏ là 15 và số hạt ở nhân là 31.
d) Nguyên tử X có điện tích hạt nhân là 19+ và số nơtron nhiều hơn số proton là 1 hạt.
e) Nguyên tử X có tổng số hạt trong nguyên tử là 58. Biết rằng số hạt không mang điện nhiều hơn số hạt mang điện âm là 4.
f) Nguyên tử X có tổng số hạt p, n, e là 115. Số hạt mang điện nhiều hơn số hạt không mang điện là 25 hạt.
g) Nguyên tử X có tổng số hạt trong nguyên tử là 46. Số hạt không mang điện bằng 8/15 số hạt mang điện.
h) Nguyên tử X có tổng số hạt trong nguyên tử là 180. Tỉ số giữa số hạt không mang điện và số hạt mang điện là 37:53.
2. Trong một nguyên tử, tổng số hạt: proton, nơtron và electron
là 28. Biết rằng số nơtron bằng số proton cộng thêm một.
a) Hãy cho biết số proton có trong nguyên tử.
b) Hãy cho biết số khối của hạt nhân.
c.) Hãy cho biết đó là nguyên tử của nguyên tố nào?
3. Viết kí hiệu nguyên tử X trong các trường hợp sau đây:
a) Tổng số hạt trong nguyên tử X là 10.
b) Tổng số hạt trong nguyên tử X là 13.
4. Tổng số hạt proton, nơtron và electron trong nguyên tử của nguyên tố R là 21. Viết ký hiệu nguyên tử đầy đủ của R.
5. Tổng số hạt proton, nơtron, electron trong nguyên tử của nguyên tố X là 34 và có số khối nhỏ hơn 24. Hãy viết ký hiệu đầy đủ của nguyên tử X.
a) Ta có: p=e=15
KHNT: \(^{31}_{15}P\)
b) Ta có: \(\left\{{}\begin{matrix}p+n=35\\n-p=1\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}n=18\\p=17\end{matrix}\right.\)
KHNT: \(^{35}_{17}Cl\)
c) Ta có: \(\left\{{}\begin{matrix}e=15\\p=e\\p+n=31\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=15\\n=16\end{matrix}\right.\)
KHNT: \(^{31}_{15}P\)
d) Ta có: \(\left\{{}\begin{matrix}p=19\\n-p=1\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=19\\n=20\end{matrix}\right.\)
KHNT: \(^{39}_{19}K\)
e) Ta có: \(\left\{{}\begin{matrix}p+e+n=58\\p=e\\n-e=4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=e=18\\n=22\end{matrix}\right.\)
KHNT: \(^{40}_{18}Ca\)
f) Ta có: \(\left\{{}\begin{matrix}p+e+n=115\\p=e\\p+e-n=25\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}n=45\\p=e=35\end{matrix}\right.\)
KHNT: \(^{80}_{35}Br\)
g) Ta có: \(\left\{{}\begin{matrix}p+e+n=46\\p=e\\n=\dfrac{8}{15}\left(p+e\right)\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=e=15\\n=16\end{matrix}\right.\)
KHNT: \(^{31}_{15}P\)
h) Ta có: \(\left\{{}\begin{matrix}p+e+n=180\\p=e\\\dfrac{n}{p+e}=\dfrac{37}{53}\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}n=74\\p=e=53\end{matrix}\right.\)
KHNT: \(^{127}_{53}I\)
Đúng 4
Bình luận (0)
2.
a,Ta có: \(\left\{{}\begin{matrix}p+e+n=28\\p=e\\n=p+1\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=e=9\\n=10\end{matrix}\right.\)
b, \(A=p+n=9+10=19\left(đvC\right)\)
c, Đây là flo (F)
Đúng 5
Bình luận (0)
Em tách nhỏ bài ra nha, đêm rồi đừng có làm khó nhau :(
Đúng 2
Bình luận (0)
Tổng số hạt proton, nơtron, electron tạo nên nguyên tử nguyên tố X là 48, trong đó số hạt mang điện dương bằng số hạt không mang điện.Tính số hạt p,n,e và viết tên kí hiệu hóa học của nguyên tố?
Gọi số hạt prton, electron và nơtron của X là p,e,n
Vì p=e⇒ p+e=2p
Theo đề ta có hệ pt: \(\left\{{}\begin{matrix}\text{2p+n=48}\\p=n\end{matrix}\right.\)
⇔\(\left\{{}\begin{matrix}p=16\\n=16\\e=16\end{matrix}\right.\)
Vậy số hạt proton, electron, nơtron trong X là : 16,16,16
Đúng 0
Bình luận (0)
11. Tính số hạt p, n, e và viết tên, kí hiệu hóa học của nguyên tố trong các trường hợp sau:(a) Một nguyên tử của nguyên tố X có tổng số hạt electron, số proton, số nơtron là 34 hạt, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 10 hạt.(b) Nguyên tử của nguyên tố X có tổng số hạt electron, proton, nơtron bằng 21, trong đó số hạt mang điện gấp 2 lần số hạt không mang điện(c) Nguyên tử của nguyên tố X có tổng số hạt p, n, e bằng 58, tổng số hạt mang điện nhiều hơn số hạt không mang...
Đọc tiếp
11. Tính số hạt p, n, e và viết tên, kí hiệu hóa học của nguyên tố trong các trường hợp sau:
(a) Một nguyên tử của nguyên tố X có tổng số hạt electron, số proton, số nơtron là 34 hạt, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 10 hạt.
(b) Nguyên tử của nguyên tố X có tổng số hạt electron, proton, nơtron bằng 21, trong đó số hạt mang điện gấp 2 lần số hạt không mang điện
(c) Nguyên tử của nguyên tố X có tổng số hạt p, n, e bằng 58, tổng số hạt mang điện nhiều hơn số hạt không mang điện là 18.
Câu a)
\(\left\{{}\begin{matrix}2P+N=34\\2P-N=10\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}P=E=Z=11\\N=12\end{matrix}\right.\\ KHHH:Natri\left(KHHH:Na\right)\)
Câu b)
\(\left\{{}\begin{matrix}2P+N=21\\2P=2N\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2P+N=21\\P=N\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}P=E=Z=7\\N=7\end{matrix}\right.\Rightarrow Nitơ\left(KHHH:N\right)\)
Câu c)
\(\left\{{}\begin{matrix}2P+N=58\\2P-N=18\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}P=E=Z=19\\N=20\end{matrix}\right.\\ \Rightarrow Kali\left(KHHH:K\right)\)
Đúng 1
Bình luận (0)
nguyên tử của một nguyên tố có tổng số hạt proton, electron, nơtron bằng 82, tổng số hạt mang điện nhiều hơn số hạt không mang điện là 22 hạt. Xác định Z,A và viết ký hiệu nguyên tử của nguyên tố X
Ta có: p + e = n = 82
Mà p = e, nên: 2p + n = 82 (1)
Theo đề, ta có: 2p - n = 22 (2)
Từ (1) và (2), ta có HPT:
\(\left\{{}\begin{matrix}2p+n=82\\2p-n=22\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2n=60\\2p-n=22\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}n=30\\p=26\end{matrix}\right.\)
Vậy p = e = Z = 26 hạt, n = 30 hạt.
Dựa vào bẳng hóa trị, suy ra:
X là sắt (Fe)
Đúng 1
Bình luận (0)
Theo đề, ta có:
\(\left\{{}\begin{matrix}2\cdot Z+N=82\\2\cdot Z-N=22\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}Z=26\\N=30\end{matrix}\right.\)
hay A=56
\(X=^{26}_{56}FE\)
Đúng 1
Bình luận (0)
Tổng số các hạt proton, nơtron và electron trong nguyên tử của một nguyên tố là 40. Biết số hạt nơtron lớn hơn số hạt proton là 1. Cho biết nguyên tố trên thuộc loại nguyên tố nào?
A. Nguyên tố s.
B. Nguyên tố p.
C. Nguyên tố d.
D. Nguyên tố f.
Chọn B
Giả sử số proton, số nơtron, số electron của nguyên tố trên lần lượt là p; n và e.
Trong đó: p =e =z.
Ta có hpt:
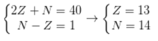
Cấu hình electron của nguyên tố là:
![]()
Nhận thấy electron cuối cùng điền vào phân lớp p → nguyên tố trên thuộc loại nguyên tố p
Đúng 0
Bình luận (0)
























