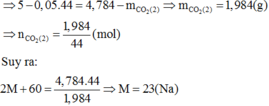Hai bình thuye tinh đựng HCl cân bằng trên hai đĩa cân. Thả vào bình thứ nhất a gam miếng kim loại Mg và bình thứ hai a gam miếng kim loại Zn. Sau khi kết thúc thí nghiệm hỏi cân còn cân bằng như cũ không?

Những câu hỏi liên quan
Trên 2 đĩa cân để 2 cốc: cốc thứ nhất đựng dung dịch HCl và cốc thứ hai dựng nước cất, cân ở vị trí cân bằng. Tiến hành thí nghiệm sau: - Cho vào cốc thứ nhất 10 gam CaCO3, - Cho vào cốc thứ hai 5,8 gam hỗn hợp 2 kim loại A và B. Sau khi phản ứng xong, trong 2 cốc chỉ thu được dung dịch trong suốt và cân vẫn ở vị trí cần bằng. Viết phương trình hóa học các phản ứng xảy ra và xác định 2 kim loại A và B. (Biết A và B là 2 kim loại nằm ở hai chu kì liên tiếp trong nhóm IA của bảng tuần hoàn; Nhóm 1...
Đọc tiếp
Trên 2 đĩa cân để 2 cốc: cốc thứ nhất đựng dung dịch HCl và cốc thứ hai dựng nước cất, cân ở vị trí cân bằng. Tiến hành thí nghiệm sau: - Cho vào cốc thứ nhất 10 gam CaCO3, - Cho vào cốc thứ hai 5,8 gam hỗn hợp 2 kim loại A và B. Sau khi phản ứng xong, trong 2 cốc chỉ thu được dung dịch trong suốt và cân vẫn ở vị trí cần bằng. Viết phương trình hóa học các phản ứng xảy ra và xác định 2 kim loại A và B. (Biết A và B là 2 kim loại nằm ở hai chu kì liên tiếp trong nhóm IA của bảng tuần hoàn; Nhóm 1A gồm các nguyên tố kim loại xếp theo thứ tự tăng dần điện tích hạt nhân là: Li, Na, K, Rb, Cs, Fr).
- Pư xong, trong 2 cốc chỉ thu được dd trong suốt
→ CaCO3 và 2 kim loại A, B tan hết.
Ta có: nCaCO3 = 0,1 (mol) = nCO2
⇒ m cốc 1 tăng = mCaCO3 - mCO2 = 10 - 0,1.44 = 5,6 (g)
Mà: Sau pư khối lượng 2 cốc bằng nhau.
⇒ m cốc 2 tăng = 5,6 (g) = 5,8 - mH2
⇒ mH2 = 0,2 (g) ⇒ nH2 = 0,1 (mol)
Vì: A và B đều thuộc nhóm IA → gọi chung là X.
PT: \(2\overline{X}+2H_2O\rightarrow2\overline{X}OH+H_2\)
Theo PT: \(n_{\overline{X}}=2n_{H_2}=0,2\left(mol\right)\)
\(\Rightarrow M_{\overline{X}}=\dfrac{5,8}{0,2}=29\left(g/mol\right)\)
Mà: A và B nằm ở 2 chu kỳ liên tiếp.
⇒ A và B là: Na và K.
Đúng 2
Bình luận (0)
Hai bình thủy tinh đựng HCl cân bằng trên 2 đĩa cân . Thả vào bình thứ nhất 40 gam miếng kim loại Mg và bình thứ hai miếng kim loại kẽm . Sau khi kết thúc thí nghiệm hỏi cân còn cân bằng như cũ không?
Hai cốc đựng dung dịch HCl đặt trên hai đĩa cân A, B. Cân ở trạng thái cân bằng. Cho 5 gam CaCO3 vào cốc A và 4,784 gam M2CO3 (M: Kim loại kiềm) vào cốc B. Sau khi hai muối đã tan hoàn toàn, cân trở lại vị trí thăng bằng. Kim loại M là A. K B. Cs C. Li D. Na
Đọc tiếp
Hai cốc đựng dung dịch HCl đặt trên hai đĩa cân A, B. Cân ở trạng thái cân bằng. Cho 5 gam CaCO3 vào cốc A và 4,784 gam M2CO3 (M: Kim loại kiềm) vào cốc B. Sau khi hai muối đã tan hoàn toàn, cân trở lại vị trí thăng bằng. Kim loại M là
A. K
B. Cs
C. Li
D. Na
trong ba bình cách nhiệt giống nhau và chứa lượng dầu như nhau và cùng nhiệt độ ban đầu . Đốt nóng một thỏi kim loại rồi thả vào bình thứ nhất. sau khi bình thứ nhất thiết lập cân bằng nhiệt ta nhấc khối kim loại cho sang bình thứ hai. sau khi bình hai thiết lập cân bằng nhiệt ta nhấc khối kim loại cho sang bình thứ ba. hỏi nhiệt độ của dầu trong bình thứ ba tăng bao nhiêu nếu dầu trong bình thứ hai tầng 5 độ trong bình thứ nhất tăng 20 độ
Đọc tiếp
trong ba bình cách nhiệt giống nhau và chứa lượng dầu như nhau và cùng nhiệt độ ban đầu . Đốt nóng một thỏi kim loại rồi thả vào bình thứ nhất. sau khi bình thứ nhất thiết lập cân bằng nhiệt ta nhấc khối kim loại cho sang bình thứ hai. sau khi bình hai thiết lập cân bằng nhiệt ta nhấc khối kim loại cho sang bình thứ ba. hỏi nhiệt độ của dầu trong bình thứ ba tăng bao nhiêu nếu dầu trong bình thứ hai tầng 5 độ trong bình thứ nhất tăng 20 độ
Trên 2 đĩa cân A và B có 2 cốc đựng dd H2SO4 (cốc A) và dd HCl (cốc B), cân ở vị trí cân bằng. Chi 13,44 gam kim loại Magie vào cốc A và 22 gam muối cacbonat của kim loại M hóa trị II vào cốc B. Sau khi phản ứng kết thúc, cân vẫn ở vị trí thăng bằng. Xác định kim loại hóa trị II, biết lượng axit trong 2 cốc đủ để tác dụng hết với kim loại và muối cacbonat
Đọc tiếp
Trên 2 đĩa cân A và B có 2 cốc đựng dd H2SO4 (cốc A) và dd HCl (cốc B), cân ở vị trí cân bằng. Chi 13,44 gam kim loại Magie vào cốc A và 22 gam muối cacbonat của kim loại M hóa trị II vào cốc B. Sau khi phản ứng kết thúc, cân vẫn ở vị trí thăng bằng. Xác định kim loại hóa trị II, biết lượng axit trong 2 cốc đủ để tác dụng hết với kim loại và muối cacbonat
\(n_{Mg}=\dfrac{13.44}{24}=0.56\left(mol\right)\)
TN1 :
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(0.56................................0.56\)
TN2 :
\(MCO_3+H_2SO_4\rightarrow MSO_4+CO_2+H_2O\)
\(x............................x\)
Vì cân thăng bằng nên :
\(m_{Mg}-m_{H_2}=m_{MCO_3}-m_{CO_2}\)
\(\Rightarrow13.44-0.56\cdot2=22-44x\)
\(\Rightarrow x=0.22\)
\(M_{MCO_3}=\dfrac{22}{0.22}=100\left(g\text{/}mol\right)\)
\(\Rightarrow M=100-60=40\left(g\text{/}mol\right)\)
\(M:Ca\)
Đúng 2
Bình luận (0)
Trong 3 bình cách nhiệt giống nhau đều chứa lượng dầu như nhau và cócùng nhiệt độ ban đầu. Đốt nóng một thỏi kim loại rồi thả vào bình thứ nhất.Sau khi bình thứ nhất thiết lập cân bằng nhiệt ta nhấc khối kim loại cho sangbình thứ hai. Sau khi bình thứ hai thiết lập cân bằng nhiệt ta nhấc khối kim loạicho sang bình thứ ba. Hỏi nhiệt độ của dầu trong bình thứ ba tăng bao nhiêunếu dầu trong bình thứ hai tăng 50C và trong bình thứ nhất tăng 200C?
Đọc tiếp
Trong 3 bình cách nhiệt giống nhau đều chứa lượng dầu như nhau và có
cùng nhiệt độ ban đầu. Đốt nóng một thỏi kim loại rồi thả vào bình thứ nhất.
Sau khi bình thứ nhất thiết lập cân bằng nhiệt ta nhấc khối kim loại cho sang
bình thứ hai. Sau khi bình thứ hai thiết lập cân bằng nhiệt ta nhấc khối kim loại
cho sang bình thứ ba. Hỏi nhiệt độ của dầu trong bình thứ ba tăng bao nhiêu
nếu dầu trong bình thứ hai tăng 50
C và trong bình thứ nhất tăng 200
C?
Trên hai đĩa cân ở vị trí thăng bằng có hai cốc giống nhau để hở trong không khí, mỗi cốc đều đựng 100 gam dung dịch HCl 3,65%. Thêm vào cốc thứ nhất 8,4 gam MgCO3, thêm vào cốc thứ hai 8,4 gam NaHCO3.a) Sau khi phản ứng kết thúc, cân còn giữ vị trí thăng bằng không? Nếu không thì lệch về bên nào? Giải thích.b) Nếu mỗi bên đĩa cân cũng lấy 100 gam dung dịch HCl nhưng nồng độ là 10% và cũng làm như thí nghiệm ban đầu thì khi phản ứng kết thúc, cân còn giữ vị trí thăng bằng không? Giải thích.giải...
Đọc tiếp
Trên hai đĩa cân ở vị trí thăng bằng có hai cốc giống nhau để hở trong không khí, mỗi cốc đều đựng 100 gam dung dịch HCl 3,65%. Thêm vào cốc thứ nhất 8,4 gam MgCO3, thêm vào cốc thứ hai 8,4 gam NaHCO3.
a) Sau khi phản ứng kết thúc, cân còn giữ vị trí thăng bằng không? Nếu không thì lệch về bên nào? Giải thích.
b) Nếu mỗi bên đĩa cân cũng lấy 100 gam dung dịch HCl nhưng nồng độ là 10% và cũng làm như thí nghiệm ban đầu thì khi phản ứng kết thúc, cân còn giữ vị trí thăng bằng không? Giải thích.
giải theo kiểu lớp 9 ạ cảm ơn ạ
Trên hai đĩa cân ở vị trí thăng bằng có hai cốc giống nhau để hở trong không khí, mỗi cốc đều đựng 100 gam dung dịch HCl 3,65%. Thêm vào cốc thứ nhất 8,4 gam MgCO3, thêm vào cốc thứ hai 8,4 gam NaHCO3.a) Sau khi phản ứng kết thúc, cân còn giữ vị trí thăng bằng không? Nếu không thì lệch về bên nào? Giải thích.b) Nếu mỗi bên đĩa cân cũng lấy 100 gam dung dịch HCl nhưng nồng độ là 10% và cũng làm như thí nghiệm ban đầu thì khi phản ứng kết thúc, cân còn giữ vị trí thăng bằng không? Giải thích.giải...
Đọc tiếp
Trên hai đĩa cân ở vị trí thăng bằng có hai cốc giống nhau để hở trong không khí, mỗi cốc đều đựng 100 gam dung dịch HCl 3,65%. Thêm vào cốc thứ nhất 8,4 gam MgCO3, thêm vào cốc thứ hai 8,4 gam NaHCO3.
a) Sau khi phản ứng kết thúc, cân còn giữ vị trí thăng bằng không? Nếu không thì lệch về bên nào? Giải thích.
b) Nếu mỗi bên đĩa cân cũng lấy 100 gam dung dịch HCl nhưng nồng độ là 10% và cũng làm như thí nghiệm ban đầu thì khi phản ứng kết thúc, cân còn giữ vị trí thăng bằng không? Giải thích.
giải theo kiểu lớp 9 ạ cảm ơn ạ
Trên hai đĩa cân ở vị trí thăng bằng có hai cốc giống nhau để hở trong không khí, mỗi cốc đều đựng 100 gam dung dịch HCl 3,65%. Thêm vào cốc thứ nhất 8,4 gam MgCO3, thêm vào cốc thứ hai 8,4 gam NaHCO3.a) Sau khi phản ứng kết thúc, cân còn giữ vị trí thăng bằng không? Nếu không thì lệch về bên nào? Giải thích.b) Nếu mỗi bên đĩa cân cũng lấy 100 gam dung dịch HCl nhưng nồng độ là 10% và cũng làm như thí nghiệm ban đầu thì khi phản ứng kết thúc, cân còn giữ vị trí thăng bằng không? Giải thích.giải...
Đọc tiếp
Trên hai đĩa cân ở vị trí thăng bằng có hai cốc giống nhau để hở trong không khí, mỗi cốc đều đựng 100 gam dung dịch HCl 3,65%. Thêm vào cốc thứ nhất 8,4 gam MgCO3, thêm vào cốc thứ hai 8,4 gam NaHCO3.
a) Sau khi phản ứng kết thúc, cân còn giữ vị trí thăng bằng không? Nếu không thì lệch về bên nào? Giải thích.
b) Nếu mỗi bên đĩa cân cũng lấy 100 gam dung dịch HCl nhưng nồng độ là 10% và cũng làm như thí nghiệm ban đầu thì khi phản ứng kết thúc, cân còn giữ vị trí thăng bằng không? Giải thích.
giải theo kiểu lớp 9 ạ cảm ơn ạ