cho 60 g Cu vào 200g dd AgNO3 nồng độ 17% . Đến khi phản ứng hoàn toàn thu được a g chất rắn và dd X
a) tính a g
b) tính nồng độ % dd X
Cho m gam Cu vao dd chứa 0,04 mol AgNO3 một thời gian thu được dd Y và 3,88 g chất rắn X. Cho 2,925 g Zn vào dd Y đến phản ứng hoàn toàn thu được dd Z và 3,217 g chất rắn T. Tính m :
A. 1,216g
B. 1,088 g
C. 1,344g
D. 1,152g
Giải thích: Đáp án D
nZn =0,052 > nAgNO3 → dd Z chỉ chứa Zn(NO3)2
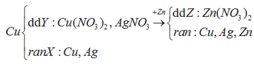
Bảo toàn số mol NO3 thì nZn(NO3)2(Z) =0,02 mol→ rắn T có mZn = 2,925-0,02.65=1,625g
Trong rắn T đặt nCu =x, nAg =y → 64x + 108y=3,217-1,625 = 1,592(g)
Bảo toàn điện tích trong dd Y có 2x + y =0,04 → x =0,018 mol y =0,004 mol
Bảo toàn khối lượng Cu và Ag trong phản ứng td với AgNO3 có
m + 0,04.108=mCu(Y) +mAg(Y) +3,88 → m =0,018.64+0,004.108+3,88-0,04.108=1,152 (g)
Bài1:Hoà tan hoàn toàn x g Mg vừa đủ trong 110ml dd HCl 1,5M. Tính x? Bài2:Cho 20,25g Al tan hoàn toàn vừa đủ trong x g dd H2SO4 18,735 a,Tính x? b,Nồng độ % của dd thu đc sau phản ứng Bài3:Cho hỗn hợp X gồm 0,1mol Cu và 0,1mol K vào nước dư. Sau phản ứng thu đc dd A và m am chất rắn.Tính giá trị của m? Mong mọi người giải giúp em
Bài 1:
PTHH: \(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\)
Ta có: \(n_{Mg}=\dfrac{1}{2}n_{HCl}=\dfrac{1}{2}\cdot0,11\cdot1,5=0,0825\left(mol\right)\)
\(\Rightarrow m_{Mg}=0,0825\cdot24=1,98\left(g\right)\)
Bài 3:
Vì Cu không tác dụng với nước
\(\Rightarrow m=m_{Cu}=0,1\cdot64=6,4\left(g\right)\)
Mg + 2HCl --> MgCl2 + H2
nHCl=0,11*1,5=0,165 mol
=>nMg-0,165/2=0,0825mol
=> mMg=0,0825*24=1,98 g
Cho 200g dd AgNO3 tác dụng vừa đủ với 200 g dd NaCl, sau phản ứng thu được 14,35g kết tủa trắng
a. Tính nồng độ % dd AgNO3
b. Tính nồng độ % dd NaCl
2/ cho 20g hổn hợp CuO, Cu, Ag tác dụng hết với 200g dd H2SO4 nồng độ 19,6% sau phản ứng thu được dd B và 4g chất rắn C. a) Viết PTHH b) tính nồng độ phần trăm các chất có trong dd B
Cho 6,9 g Natri vào 200 g dd HCl 3,65% sau phản ứng hoàn toàn chỉ thu được dd A và có V lít khí H2 thoát ra
a,Viết PTHH và tính V
b,Tính nồng độ phần trăm các chất tan có trong A
\(n_{Na}=\dfrac{6,9}{23}=0,3\left(mol\right)\\ m_{HCl}=200.3,65\%=7,3\left(g\right)\\ n_{HCl}=\dfrac{7,3}{36,5}=0,2\left(mol\right)\)
\(PTHH:2Na+2HCl\rightarrow2NaCl+H_2\uparrow\\ LTL:0,3>0,2\Rightarrow Na.dư\)
Theo pt: nH2 = 2nHCl = 2.0,2 = 0,4 (mol)
VH2 = 0,4.22,4 = 8,96 (l)
Theo pt: nNaCl = nNa (phản ứng) = nHCl = 0,2 (mol)
=> \(\left\{{}\begin{matrix}m_{NaCl}=0,2.58,5=11,7\left(g\right)\\m_{Na\left(dư\right)}=\left(0,3-0,2\right).23=2,3\left(g\right)\\m_{H_2}=0,4.2=0,8\left(g\right)\end{matrix}\right.\)
=> \(m_{dd}=200+6,9-2,3-0,8=203,8\left(g\right)\)
=> C%NaCl = \(\dfrac{11,7}{203,8}=5,74\%\)
Cho 200ml dung dịch hỗn hợp AgNO3 0,1M và Cu(NO3)2 0,5M. Thêm 2,24 gam gam bột Fe kim loại vào dung dịch đó khuấy đều tới khi phản ứng hoàn toàn thu được chất rắn A và dung dịch B.
a,Tính số gam chất rắn A
b, Tính nồng độ mol các muối trong dd B
c,Hòa tan chất rắn A bằng HNO3 đặc thì có bao nhiêu lít khí màu nâu thoát ra(đktc)?
a) m rắn=4,08 gam
b) CM Cu(NO3)2 dư=0,35M; CM Fe(NO3)2=0,2M
c) V NO2=1,792 lít
Giải thích các bước giải:
Ta có: nAgNO3=0,2.0,1=0,02 mol; nCu(NO3)2=0,5.0,2=0,1 mol; nFe=2,24/56=0,04 mol
Fe + 2AgNO3 -> Fe(NO3)2 + 2Ag
Vì nAgNO3=0,02 mol; nFe =0,04 -> Fe dư -> tạo ra 0,02 mol Ag và Fe phản ứng 0,01 mol -> dư 0,03 mol
Fe + Cu(NO3)2 -> Fe(NO3)2 + Cu
Vì Cu(NO3)2=0,1 mol; nFe =0,03 mol -> Cu(NO3)2 dư =0,07 mol ; nCu=0,03 mol
Rắn thu được gồm Ag 0,02 mol và Cu 0,03 mol -> m rắn=4,08 gam
Dung dịch sau phản ứng chứa Cu(NO3)2 dư 0,07 mol và Fe(NO3)2 0,04 mol (Bảo toàn Fe)
-> CM Cu(NO3)2=0,07/0,2=0,35M; CM Fe(NO3)2=0,04/0,2=0,2M
Hòa tan rắn bằng HNO3 đặc
Ag + 2HNO3 -> AgNO3 + NO2 + H2O
Cu + 4HNO3 -> Cu(NO3)2 +2NO2 + 2H2O
-> nNO2=nAg + 2nCu=0,02+0,03.2=0,08 mol -> V NO2=0,08.22,4=1,792 lít
cho 200g dd AgNO3 17% vào 300g dd NaCl 2.925%. Sau khi các phản ứng xảy ra hoàn toàn thu được dd X và m(g) kết tủa Y
a)tính m
b)tính nồng độ % các chất tan trong X
\(m_{AgNO3}=200.17\%=34\left(g\right)\)
\(\Rightarrow n_{AgNO3}=\frac{35}{170}=0,2\left(mol\right)\)
\(m_{NaCl}=300.2,925\%=8,775\left(g\right)\)
\(\Rightarrow n_{NaCl}=\frac{8,775}{58,5}=0,15\left(mol\right)\)
\(AgNO_3+NaCl\rightarrow AgCl+NaNO_3\)
0,15_______0,15______0,15______0,15
Sau phản ứng AgNO3 hết ( tính theo NaCl)
\(n_{AgCl}=n_{NaCl}=0,15\left(mol\right)\)
\(\Rightarrow m_{AgCl}=0,15.143,5=21,525\left(g\right)\)
\(m_{dd\left(spu\right)}=m_{NaCl}+m_{AgNO3}-n_{AgCl}\)
\(=34+8,775-21,525=21,25\left(g\right)\)
\(n_{AgNO3\left(dư\right)}=0,2-0,15=0,05\left(mol\right)\)
\(m_{AgNO3\left(dư\right)}=0,05.170=8,5\left(g\right)\)
\(C\%_{AgNO3\left(dư\right)}=\frac{8,5}{21,25}.100\%=40\%\)
\(m_{NaNO3}=0,15.85=12,75\left(g\right)\)
\(\Rightarrow C\%_{NaNO3}=\frac{12,75}{21,25}.100\%=60\%\)
Cho 8,4 gam bột sắt vào 270 gam dung dịch CuCl2 10% (d = 1,35 g/ml), khi đến phản ứng xảy ra hoàn toàn thu được a gam chất rắn và dung dịch A.
a) Viết PTPƯ, tính a?
b) Tính C% của dung dịch A.
c) Xác định nồng độ mol/lít của dd A (coi thể tích dung dịch thay đổi không đáng kể)
\(n_{Fe}=\dfrac{8,4}{56}=0,15mol\)
\(m_{CuCl_2}=\dfrac{270\cdot10\%}{100\%}=27g\Rightarrow n_{CuCl_2}=0,2mol\)
\(Fe+CuCl_2\rightarrow FeCl_2+Cu\)
0,15 0,2 0,15 0,15
\(a=m_{Cu}=0,15\cdot64=9,6g\)
\(m_{FeCl_2}=0,15\cdot127=19,05g\)
\(m_{ddFeCl_2}=8,4+270-0,15\cdot64=268,8g\)
\(C\%=\dfrac{19,05}{268,8}\cdot100\%=7,09\%\)
Hòa tan hoàn toàn 4,55g kim loại Zn vào 200 mL dd HCl (khối lượng riêng là 0,8 g/ml), sau PƯ thu đc V lít khí (đktc) và dd X
a) Tính nồng độ mol dd HCl tham gia PƯ
b) Tính giá trị V
c) Cô cạn dd X hoàn toàn, tính khối lượng chất rắn còn lại
d) Cho dd X PƯ đủ với 200g dd AgNO3, thu đc ddY. Tính nồng độ % dd Y
(Cho Zn=65, Cl=35.5, H=1)
\(n_{Zn}=\dfrac{4,55}{65}=0,07(mol)\\ Zn+2HCl\to ZnCl_2+H_2\\ a,n_{HCl}=0,14(mol)\\ \Rightarrow C_{M_{HCl}}=\dfrac{0,14}{0,2}=0,7M\\ b,n_{H_2}=0,07(mol)\\ \Rightarrow V_{H_2}=0,07.22,4=1,568(l)\\ c,n_{ZnCl_2}=0,07(mol)\\ \Rightarrow m_{ZnCl_2}=0,07.136=9,52(g)\\ c,ZnCl_2+2AgNO_3\to 2AgCl\downarrow+Zn(NO_3)_2\)
\(m_{dd_{ZnCl_2}}=200.0,8+4,55-0,07.2=164,41(g)\\ n_{AgCl}=0,14(mol);n_{Zn(NO_3)_2}=0,07(mol)\\ \Rightarrow C\%_{Zn(NO_3)_2}=\dfrac{0,07.189}{164,41+200-0,14.143,5}.100\%=3,84%\)