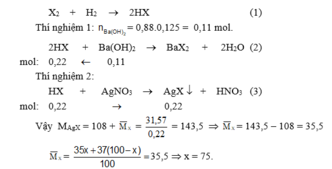một loại khí Clo có chứa 2 đồng vị 3517Cl , 3717Cl . cho Cl2 tác dụng với H2 rồi lấy sản phẩm hòa tan với nước thu được dung dịch X . chia dung dịch X thành hai phần bằng nhau:
- phần thứ nhất cho tác dụng vừa đủ với 125ml dung dịch Ba(OH)2 0.88M
- phần thứ hai cho tác dụng AgNO3 vừa đủ ta thu được 31.57g kết tủa. thành phần phần trăm số nguyên tử của mỗi đồng vị là bao nhiêu