Kim loại M có số khối bằng 56 đvC, trong phản ứng hoá học M nhường đi 2e tạo thành ion M2+, tổng số hạt trong ion M2+ là 80 hạt. Hãy xác định vị trí của M trong bảng tuần hoàn
Ai giúp e vs ah. Thanks mn nhìu..
Câu 21: Một kim loại M có số khối bằng 54, tổng số hạt các loại hạt cơ bản trong ion M2+ là 78.
a. Hãy xác định số thứ tự của M trong bảng tuần hoàn và cho biết M là nguyên tố nào trong số các nguyên tố có kí hiệu sau đây:
b. Viết phương trình phản ứng khi cho M(NO3)2 lần lượt tác dụng với Cl2, Zn, dung dịch Ca(OH)2, dung dịch AgNO3, dung dịch HNO3 loãng (tạo ra NO). Từ đó hãy cho biết tính chất hoá học cơ bản của ion M2
Câu 8: Trong tự nhiên, nguyên tố clo có 2 đồng vị \(^{35}_{17}Cl;^{37}_{17}Cl\)có % số nguyên tử tương ứng là 75% và 25%. Nguyên tố đồng có 2 đồng vị, trong đó \(^{63}_{29}Cu\)
chiếm 73% số nguyên tử. Đồng và clo tạo được hợp chất CuCl2 trong đó % khối lượng Cu chiếm 47,228%.
Tìm số khối của đồng vị còn lại của đồng.
Câu 21: Một kim loại M có số khối bằng 54, tổng số hạt các loại hạt cơ bản trong ion M2+ là 78.
a. Hãy xác định số thứ tự của M trong bảng tuần hoàn và cho biết M là nguyên tố nào
b. Viết phương trình phản ứng khi cho M(NO3)2 lần lượt tác dụng với Cl2, Zn, dung dịch Ca(OH)2, dung dịch AgNO3, dung dịch HNO3 loãng (tạo ra NO). Từ đó hãy cho biết tính chất hoá học cơ bản của ion M2+ .
+ A(M) = 54 => Z + N = 54 (1)
+ M2+ có tổng số hạt là 78
=> 2Z + N - 2 = 78
<=> 2Z + N = 80 (2)
Từ (1) (2) ta giải đc: Z = 26; N = 30
=> M là Fe
b) em có thể viết pt đc chứ
Hợp chất A tạo bởi ion M2+ và ion X2-. Tổng số hạt cơ bản tạo nên trong hợp chất A là 241 trong đó tổng số hạt mang điện nhiều hơn số hạt không mang điện là 47. Tổng số hạt mang điện của ion M2+ nhiều hơn của ion X2- là 76 hạt. Vị trí của M trong bảng tuần hoàn là
A. Ô 12, chu kỳ 3, nhóm IIA.
B. Ô 20, chu kỳ 4, nhóm IIA.
C. Ô 56, chu kỳ 6, nhóm IIA.
D. Ô 38, chu kỳ 5, nhóm IIA.
Đáp án C
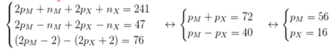
Vậy, M ở ô 56, chu kì 6, nhóm IIA
Hợp chất A tạo bởi ion M 2 + và ion X 2 - . Tổng số hạt cơ bản tạo nên trong hợp chất A là 241 trong đó tổng số hạt mang điện nhiều hơn số hạt không mang điện là 47. Tổng số hạt mang điện của ion M 2 + nhiều hơn của ion X 2 - là 76 hạt. Vị trí của M trong bảng tuần hoàn là
A. Ô 12, chu kỳ 3, nhóm IIA
B. Ô 20, chu kỳ 4, nhóm IIA
C. Ô 56, chu kỳ 6, nhóm IIA
D. Ô 38, chu kỳ 5, nhóm IIA
Hợp chất ion G tạo nên từ các ion đơn nguyên tử M 2 + và X 2 - . Tổng số hạt (nơtron, proton, electron) trong phân tử G là 84, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 28 hạt. Số hạt mang điện của ion X 2 - ít hơn số hạt mang điện của ion M 2 + là 20 hạt. Vị trí của M trong bảng tuần hoàn là
A. ô 8, chu kì 2, nhóm VIA
B. ô 20, chu kì 4, nhóm IIA
C. ô 26, chu kì 4, nhóm VIIIB
D. ô 12, chu kì 3, nhóm IIA
Hợp chất ion G tạo nên từ các ion đơn nguyên tử M2+ và X2-. Tổng số hạt (nơtron, proton, electron) trong phân tử G là 84, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 28 hạt. Số hạt mang điện của ion X2- ít hơn số hạt mang điện của ion M2+ là 20 hạt. Vị trí của M trong bảng tuần hoàn là
A. ô 8, chu kì 2, nhóm VIA.
B. ô 20, chu kì 4, nhóm IIA.
C. ô 26, chu kì 4, nhóm VIIIB.
D. ô 12, chu kì 3, nhóm IIA.
Đáp án B
Gọi a, b là lần lượt tổng số proton và nơtron
Ta có: 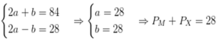
Ta có:
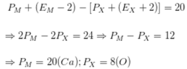
M là canxi ở ô 20, chu kì 4, nhóm IIA
Chọn B
ion M3+ có tổng số hạt P, E , N là 73 , số khối M là 52
- xác định số điện tích hạt nhân M
- viết hiệu nguyên tử M
- viết cấu hình electrong của M
- vị trí của m trong bảng tuần hoàn
a) Trong ion X3- có tổng số các hạt (p,e,n) là 49, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 17. Xác định số khối, viết cấu hình electron của nguyên tử X và cho biết vị trí của X trong bảng tuần hoàn các nguyên tố hoá học. b) Trong tự nhiên Flo có 2 dồng vị: 18F chiếm 0,2%, xác định số khối của đồng vị thứ 2, biết rằng Flo có nguyên tử khối trung bình là 18,998u
Một hợp chất ion Y được cấu tạo từ ion M+ và ion X-. Tổng số hạt electron trong Y bằng 36. Số hạt proton trong M+ nhiều hơn trong X- là 2. Vị trí của nguyên tố M và X trong bảng tuần hoàn hóa học các nguyên tố hóa học là
A. M: chu kì 3, nhóm IA; X: chu kì 3, nhóm VIIA.
B. M: chu kì 3, nhóm IB; X: chu kì 3, nhóm VIIA.
C. M: chu kì 4, nhóm IA; X: chu kì 4, nhóm VIIA.
D. M: chu kì 4, nhóm IA; X: chu kì 3, nhóm VIIA.
Đáp án D
Hợp chất Y được cấu tạo từ ion M+ và ion X- Hợp chất Y là MX
Theo giả thiết ta có:
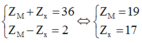
=> M là Kali và X là Cl
K có cấu hình electron là: 1s22s22p63s23p64s1
=> K thuộc chu kì 4; nhóm IA
Cl có cấu hình electron là: 1s22s22p63s23p5
=> Cl thuộc chu kì 3; nhóm VIIA