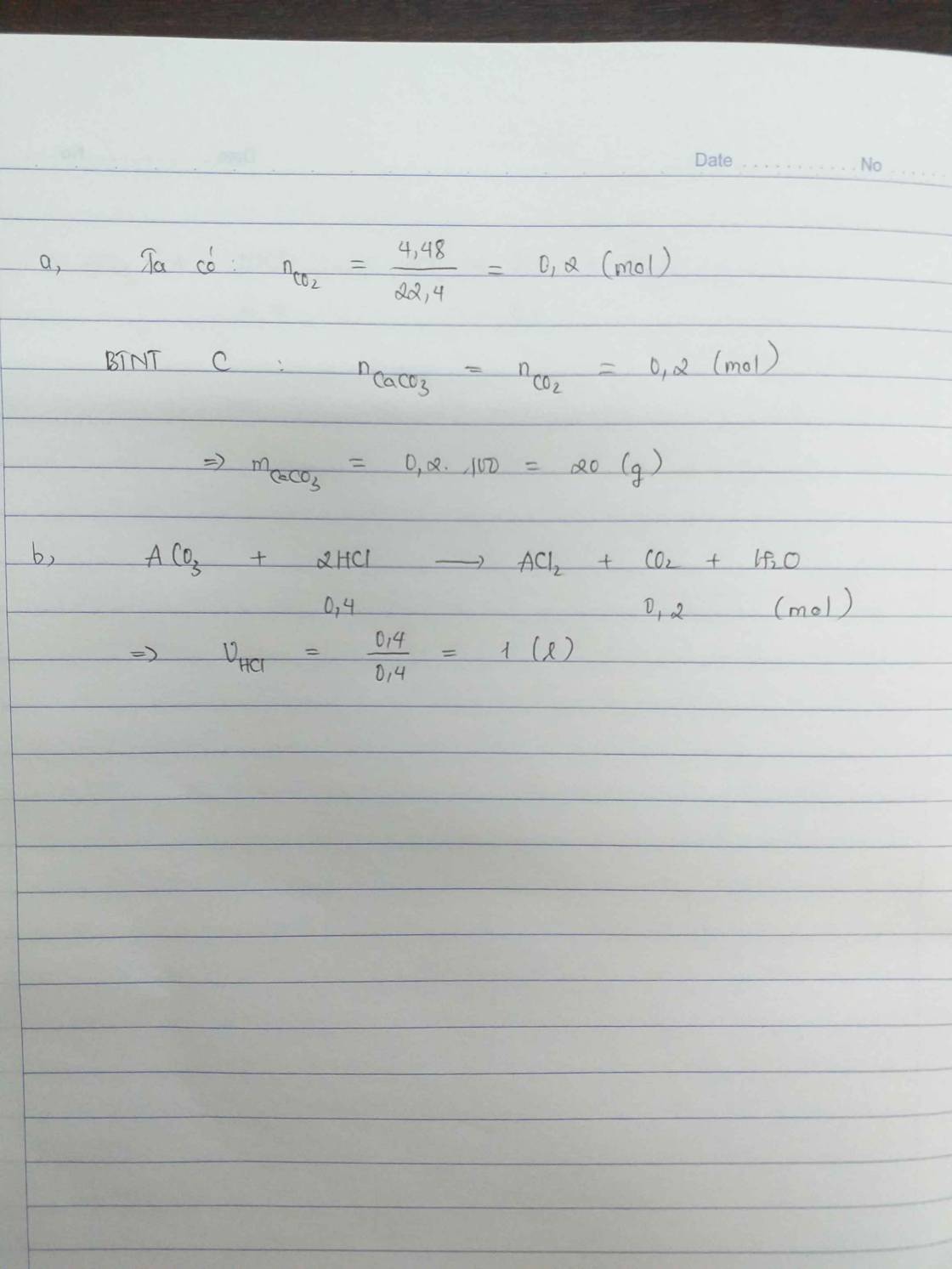Dẫn từ từ V lít CO2 (đktc) vào 1500 ml dd Ca(OH)2 0,1M thu được 10 gam kết tủa. Tính V, cho biết khối lượng dd thay đổi như thế nào và vẽ đồ thị.

Những câu hỏi liên quan
Dẫn từ từ V lít khí CO2 ở đktc vào 400 ml dung dịch chứa đồng thời Ca(OH)2 0,8M và KOH 1,5M thì thu được 10 gam kết tủa trắng. Tính V.
\(n_{Ca\left(OH\right)_2}=0,32\left(mol\right)\)
\(n_{KOH}=0,6\left(mol\right)\)
\(n_{CaCO_3}=\dfrac{10}{100}=0,1\left(mol\right)\)
PTHH :
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3\downarrow+H_2O\)
0,1 0,32 0,1
Ca(OH)2 dư nên tính theo CaCO3
\(CO_2+2KOH\rightarrow K_2CO_3+H_2O\)
0,3 0,6
\(V_{CO_2}=\left(0,1+0,3\right).22,4=8,96\left(l\right)\)
Đúng 0
Bình luận (6)
\(n_{Ca\left(OH\right)_2}=0,4.0,8=0,32mol\\ n_{KOH}=0,4.1,5=0,6mol\\ n_{CaCO_3}=\dfrac{10}{100}=0,1mol\)
Vì \(n_{CaCO_3}< n_{Ca\left(OH\right)_2}\)
TH1 tạo muối trung hoà(Ca(OH)2 dư)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
\(0,1...............0,1.......0,1...........0,1\)
\(2KOH+CO_2\rightarrow K_2CO_3+H_2O\)
\(0,6..........0,3........0,3...........0,3\)
\(V_{CO_2}=\left(0,1+0,3\right).22,4=8,96l\)
TH2 tạo 3 muối(CO2 dư)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
\(0,1...............0,1.......0,1...........0,1\)
\(Ca\left(OH\right)_2+2CO_2\rightarrow Ca\left(HCO_3\right)_2\)
\(0,22.............0,44........0,22\)
\(2KOH+CO_2\rightarrow K_2CO_3+H_2O\)
\(0,6...........0,3.......0,3...........0,3\)
\(V_{CO_2}=\left(0,1+0,44+0,3\right).22,4=18,816l\)
Đúng 0
Bình luận (3)
Ta có: \(n_{Ca\left(OH\right)_2}=0,4.0,8=0,32\left(mol\right)\)
\(n_{KOH}=0,4.1,5=0,6\left(mol\right)\)
\(n_{CaCO_3}=\dfrac{10}{100}=0,1\left(mol\right)\)
TH1: Kết tủa chưa bị hòa tan.
PT: \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
____0,1_________________0,1 (mol)
\(\Rightarrow V_{CO_2}=0,1.22,4=2,24\left(l\right)\)
TH2: Kết tủa đã bị hòa tan 1 phần.
PT: \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
____0,32______0,32_______0,32 (mol)
\(CO_2+2KOH\rightarrow K_2CO_3+H_2O\)
0,3_______0,6______0,3 (mol)
\(CO_2+H_2O+K_2CO_3\rightarrow2KHCO_3\)
0,3______________0,3 (mol)
\(CO_2+H_2O+CaCO_3\rightarrow Ca\left(HCO_3\right)_2\)
0,22___________0,22 (mol)
\(\Rightarrow V_{CO_2}=\left(0,32+0,3+0,3+0,22\right).22,4=25,536\left(l\right)\)
Đúng 1
Bình luận (0)
Cho A gam hỗn hợp Bari Cacbonat và Canxi Cacbonat tác dụng với V lít dd HCL 0,4M thấy giải phóng 4,48 lít CO2 (đktc), dẫn khí thu được vào dung dịch Ca(OH)2 dư. Tính
a/ Khối lượng kết tủa thu được
b/ Thể tích dd HCL cần dùng
\(a/n_{CO_2}=\dfrac{4,48}{22,4}=0,2mol\\ CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\\ n_{CO_2}=n_{CaCO_3}=0,2mol\\ m_{CaCO_3}=0,2.100=20g\\ b/BTNT\left(O\right):2n_{CO_2}=n_{H_2O}\\ \Rightarrow n_{H_2O}=0,2.2=0,4mol\\ BTNT\left(H\right):2n_{H_2O}=n_{HCl}\\ n_{HCl}=0,4.2=0,8mol\\ V_{HCl}=\dfrac{0,8}{0,4}=2l\)
Đúng 0
Bình luận (3)
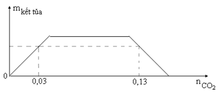
Dẫn từ từ khí CO2, vào V ml dung dịch hỗn hợp NaOH 0,2M và Ba(OH)2 0,1M. Đồ thị biểu diễn khối lượng kết tủa theo số mol CO2 như sau:
nOH– = 0,4V
Tại nCO2 = 0,03 => OH– dư => n kết tủa = nCO2 = 0,03 mol
Tại nCO2 = 0,13 mol kết tủa bị hòa tan 1 phần
nCO2 = nOH– – n kết tủa
=> nOH– = nCO2 + n kết tủa = 0,16mol = 0,4V
=> V = 0,4
Đúng 0
Bình luận (0)
Dẫn V lít khí C O 2 ở đktc vào 0,3 lít dd C a ( O H ) 2 0,02M thì thu được 0,2 gam kết tủa. Tính giá trị của V.
Sục từ từ V lít khí CO2 (đktc) vào 200ml dd Ca(OH)2 1M thu được 15 gam kết tủa. Tìm V và vẽ đồ thị về sự phụ thuộc số mol kết tủa theo CO2.
1. hấp thụ toàn bộ m g hh co2 và hơi nước vao 9l dd ca(oh)2 0,01 M thu được 4 g kết tủa. Tách bỏ phần kết tủa thành khối lượng dd tăng 1,82 g so với dd ca(oh)2 ban đầu. tính khối lượng mỗi chất.
2. dẫn từ từ V lít co2 (ddktc) vào 200 ml dd X gồm naoh 1M và ba(oh)2 0,75M thu được x gam kết tủa. tính V để x đạt giá trị lớn nhất.
1.\(n_{Ca\left(OH\right)2}=0,09\left(mol\right)\)
\(n\downarrow=n_{CaCO3}=0,04\left(mol\right)\)
\(\Rightarrow n_{CO2}=n_{CaCO3}=0,04\left(mol\right)\)
\(\Rightarrow m_{CO2}=0,04.44=1,76\left(g\right)\)
\(\Rightarrow\)mdd tăng =mCO2+mH2O-m\(\downarrow\)
\(\Leftrightarrow\) 1,82=1,76+mH2O-4
\(\Rightarrow m_{H2O}=4,06\left(g\right)\)
2.
\(n_{NaOH}=0,2\left(mol\right)\)
\(n_{Ba\left(OH\right)2}=0,15\left(mol\right)\)
\(n_{BaCO3}=m_{Ba\left(OH\right)2}=0,15\left(mol\right)\)
\(\Rightarrow n_{OH^-}=0,2+0,15.2=0,5\left(mol\right)\)
\(CO2+OH^-\rightarrow HCO3^-\)
0,2.............0,2
\(CO2+2OH^-\rightarrow CO3^{2-}+H2O\)
0,15......0,3.............0,15
\(n_{CO2}=0,2+0,15=0,35\left(mol\right)\)
\(\Rightarrow V_{CO2}=0,35.22,4=7,84l\)
Cho a g hỗn hợp BaCO3, CaCO3 tác dụng hết với V lít dd HCl 0,4 M thấy giải phóng 4,48 lít CO2 (đktc). Dẫn khí thu được vào dd Ca(OH)2 dư.a. Khối lượng kết tủa thu được là B. 15 gam C. 20g A. 10g D. 25 gamb. Thể tích dd HCI cần dùng là C. 1,6 lít B. 1,5 lít A. 1 lít D. 1,7 lítc. Giá trị của a nằm trong khoảng nào? A. 10 gam a 20 gam B. 20 gam a 35,4 gam C. 20g a 39,4g D. 20g a 40g
Đọc tiếp
Cho a g hỗn hợp BaCO3, CaCO3 tác dụng hết với V lít dd HCl 0,4 M thấy giải phóng 4,48 lít CO2 (đktc). Dẫn khí thu được vào dd Ca(OH)2 dư.
a. Khối lượng kết tủa thu được là B. 15 gam C. 20g A. 10g D. 25 gam
b. Thể tích dd HCI cần dùng là C. 1,6 lít B. 1,5 lít A. 1 lít D. 1,7 lít
c. Giá trị của a nằm trong khoảng nào? A. 10 gam <a <20 gam B. 20 gam <a <35,4 gam C. 20g <a <39,4g D. 20g < a <40g
a) \(n_{CO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: Ca(OH)2 + CO2 --> CaCO3 + H2O
0,2----->0,2
=> mCaCO3 = 0,2.100 = 20 (g)
=> C
b)
PTHH: BaCO3 + 2HCl --> BaCl2 + CO2 + H2O
CaCO3 + 2HCl --> CaCl2 + CO2 + H2O
=> nHCl = 2.nCO2 = 2.0,2 = 0,4 (mol)
=> \(V_{dd.HCl}=\dfrac{0,4}{0,4}=1\left(l\right)\)
=> A
c)
nmuối = 0,2 (mol)
Có: 100.0,2 < a < 197.0,2
=> 20 < a < 39,4
=> C
Đúng 5
Bình luận (0)
. PTHH: C O 2 + C a ( O H ) 2 → C a C O 3 + H 2 O n C O 2 = 4 , 48 22 , 4 = 0 , 2 m o l → n C a C O 3 = n C O 2 = 0 , 2 m o l → m C a C O 3 = 0 , 2.100 = 20 g a m → Chọn C. b. PTHH: B a C O 3 + 2 H C l → B a C l 2 + C O 2 + H 2 O C a C O 3 + 2 H C l → C a C l 2 + C O 2 + H 2 O Nhận xét: Từ PTHH ta thấy n H C l = 2 n C O 2 = 0 , 4 m o l → V H C l = 0 , 4 0 , 4 = 1 , 0 l í t → Chọn A. c. Giả sử hỗn hợp ban đầu chỉ có BaCO3 n B a C O 3 = n C O 2 = 0 , 2 m o l → m B a C O 3 = 0 , 2.197 = 39 , 4 g a m Giả sử hỗn hợp ban đầu chỉ có CaCO3 n C a C O 3 = n C O 2 = 0 , 2 m o l → m C a C O 3 = 0 , 2.100 = 20 g a m Thực tế, hỗn hợp ban đầu chứa cả BaCO3 và CaCO3 nên giá trị của a nằm trong khoảng 20 gam < a < 39,4 gam
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Dẫn từ từ đến hết V lít khí CO2 (đktc) vào 200 ml dung dịch Ca(OH)2 1,5M thu được 20 gam kết tủa. Giá trị của V là:
A. 4,48 lít hoặc 6,72 lít
B. 4,48 lít hoặc 8,96 lít
C. 2,24 lít hoặc 6,72 lít
D. 2,24 lít hoặc 8,96 lít
Đáp án B
Ta có: n C a ( O H ) 2 = 0,2.1,5 = 0,3 mol; n C a C O 3 = 20/100= 0,2 mol
Ta có : n C a ( O H ) 2 > n C a C O 3 nên có 2 trường hợp xảy ra :
- TH1 : Ca(OH)2 dư :
CO2+ Ca(OH)2 → CaCO3+ H2O
Ta có: n C O 2 = n C a C O 3 = 0,2 mol → V = V C O 2 = 0,2.22,4 = 4,48 lít
- TH2 : Ca(OH)2 phản ứng hết :
CO2+ Ca(OH)2 → CaCO3+ H2O
0,2 0,2 0,2
2CO2+ Ca(OH)2 → Ca(HCO3)2
0,2← (0,3-0,2)
Ta có: n C O 2 = 0,2 + 0,2 = 0,4 mol
→ V= V C O 2 = 0,4.22,4 = 8,96 lít
Đúng 0
Bình luận (0)
Câu 26: Cho 0,672 lít khí CO2 (đktc) vào 200ml dd Ca(OH)2 0,1M. Tính khối lượng kết tủa tạo thành.
Xem chi tiết
Ta có: \(\left\{{}\begin{matrix}n_{Ca\left(OH\right)_2}=0,2\cdot0,1=0,02\left(mol\right)\\n_{CO_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) Tạo cả 2 muối
PTHH: \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3\downarrow+H_2O\) (1)
\(2CO_2+Ca\left(OH\right)_2\rightarrow Ca\left(HCO_3\right)_2\) (2)
Đặt \(\left\{{}\begin{matrix}n_{Ca\left(OH\right)_2\left(1\right)}=n_{CaCO_3}=a\left(mol\right)\\n_{Ca\left(OH\right)_2\left(2\right)}=b\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}a+b=0,02\\a+2b=0,03\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=n_{CaCO_3}=0,01\left(mol\right)\\b=0,01\end{matrix}\right.\)
\(\Rightarrow m_{CaCO_3}=0,01\cdot100=1\left(g\right)\)
Đúng 1
Bình luận (0)