Một dung dịch x chưa 0,1 Na+,0,2 Cu2+ ,a mol S042- thêm Bacl2 vào thu được m gam muối tính m đó
Dung dịch X gồm: 0,2 mol K+; 0,15 mol Cu2+; 0,1 mol Cl- và x mol SO42-. Cô cạn dung dịch X thu được m gam muối khan. Giá trị của m là
A. 40,15.
B 59,35.
C. 49,75 gam.
D 30,55.
Dung dịch X gồm: 0,2 mol K+; 0,15 mol Cu2+; 0,1 mol Cl- và x mol SO42-. Cô cạn dung dịch X thu được m gam muối khan. Giá trị của m là:
A. 40,15.
B. 59,35.
C. 49,75 gam.
D. 30,55.
Dung dịch X gồm: 0,2 mol K+; 0,15 mol Cu2+; 0,1 mol Cl- và x mol SO42-. Cô cạn dung dịch X thu được m gam muối khan. Giá trị của m là:
A. 40,15.
B. 59,35.
C. 49,75 gam.
D. 30,55.
Dung dịch X gồm: 0,2 mol K+; 0,15 mol Cu2+; 0,1 mol Cl- và x mol SO42-. Cô cạn dung dịch X thu được m gam muối khan. Giá trị của m là:
A. 40,15.
B 59,35.
C. 49,75 gam.
D 30,55.
Đáp án A
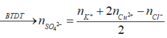
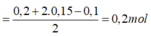
![]()
= 0,2.39 + 0,15.64 + 0,1.35,5 + 0,2.96 = 40,15 (g)
Dung dịch X gồm 0,1 mol K+; 0,2 mol Mg2+; 0,1 mol Na+; 0,2 mol Cl- và a mol Y2-. Cô cạn dung dịch X thu được m gam muối khan. Ion Y2- và giá trị của m là:
A. CO32- và 30,1
B. SO42- và 56,5
C. CO32- và 42,1
D. SO42- và 37,3
Đáp án D
Để dung dịch tồn tại thì ion Y2- là SO42-
Theo định luật bảo toàn điện tích: 0,1.1+ 0,2.2+0,1.1=0,2+ 2a
Suy ra a= 0,2
Muối khan thu được là: 0,1.39+ 0,2.24+ 0,1.23+0,2.35,5+ 0,2.96= 37,3 gam
Dung dịch X có 0,1 mol K+; 0,2 mol Mg2+; 0,1 mol Na+; 0,2 mol Cl- và a mol Y-. Cô cạn dung dịch X thu được m gam muối khan. Ion Y- và giá trị của m là?
A. OH- và 30,3
B. NO3- và 23,1
C. NO3- và 42,9
D. OH- và 20,3
Đáp án : C
Bảo toàn điện tích trong dung dịch: nY = 0,1 + 0,2. 2 + 0,1 – 0,2 = 0,4 mol
Đáp số cho ta hai ion Y- là và , nhưng loại vì nó không thể tồn tại trong cùng 1 dung dịch với ion
mmuối = 0,1. 39 + 0,2. 24 + 0,1. 23 + 0,2. 35,5 + 0,4. 62 = 42,9 g
Dung dịch X gồm 0,1 mol K+; 0,2 mol Mg2+; 0,1 mol Na+; 0,2 mol Cl- và a mol Y2-. Cô cạn dung dịch X, thu được m gam muối khan. lon Y2- và giá trị của m là
A. C O 3 2 - và 42,1
B. S O 4 2 - và 37,3
C. S O 4 2 - và 56,5
D. C O 3 2 - và 30,1
Quan sát 4 đáp án ta thấy
![]()
Vì dung dịch tồn tại 0,2 mol Mg2+ mà MgCO3 là chất kết tủa do đó Y sẽ là ![]() . Áp dụng định luật bảo toàn điện tích ta có
. Áp dụng định luật bảo toàn điện tích ta có
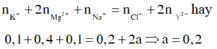
Khối lượng muối bằng tổng khối lượng của các ion trong dung dịch:
![]() gam
gam
Đáp án B.
Dung dịch X gồm 0,1 mol K+; 0,2 mol Mg2+; 0,1 mol Na+; 0,2 mol Cl- và a mol Y2- . Cô cạn dung dịch X, thu được m gam muối khan. Ion Y2- phù hợp và giá trị của m là:
A. CO32- và 30,1
B. CO32 và 42,1
C. SO42- và 56,5
D. SO42- và 37,3
Bảo toàn điện tích và bảo toàn khối lượng:
0,1.1 + 0,2.2 + 0,1.1 = 0,2.1+ a.2 => a = 0,2.
Mà muốn dung dịch tồn tại được thì các ion không được phản ứng với nhau. Do đó Y2- chỉ có thể là SO42-(theo đáp án)
m = 0,1.39 + 0,2.24 + 0,1.23 + 0,2.35,5 + 0,2.96 = 37,3 gam.
=> Đáp án D
Hòa tan m gam hỗn hợp X gồm hai muối vào nước thu được dung dịch chứa 0,05 mol Na + ; 0,1 mol Mg 2 + ; 0,2 mol Cl - và x mol SO 4 2 - . Giá trị của m là
A. 29,85.
B. 23,7.
C. 16,6
D. 13,05
Chọn D
Bảo toàn điện tích có: 0,05 + 0,1.2 = 0,2 + 2x → x = 0,025.
mmuối = ∑mion = 0,05.23 + 0,1.24 + 0,2.35,5 + 0,025.96 = 13,05 (gam).