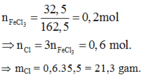Cần bao nhiêu gam MnO2 và bao nhiêu mililit dd axitHCl 1M dđ điều chế đủ khí Clo tác dụng với sắt tao nên 16,25g Fecl3

Những câu hỏi liên quan
Cần bao nhiêu gam KMnO4 và bao nhiêu ml dung dịch axit clohiđric 1M để điều chế khí clo tác dụng với sắt, tạo nên 16,25g FeCl3?
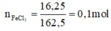
Phương trình hóa học của phản ứng:
3Cl2 + 2Fe → 2FeCl3
Theo pt: 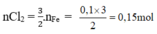
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
Theo pt:
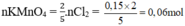
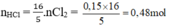
mKMnO4 cần = 0,06. 158 = 9,48g
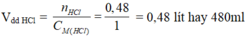
Đúng 0
Bình luận (0)
Cần bao nhiêu gam Mno2 và bao nhiêu ml dd hcl 1M để điều chế đủ khí cl2 tác dụng với sắt tạo ra 16,35 g fecl3
Xem chi tiết
2Fe + 3Cl2 --> 2FeCl3
16,25 gam FeCl3 tương đương với 0,1 mol FeCl3
Từ phương trình ta thấy để tạo ra được 0,1 mol FeCl3 thì số mol Cl2 dùng để phản ứng = 0.1.3/2 = 0,15 mol
Điều chế Clo: MnO2 + 4HCl --> MnCl2 + Cl2 + H2O
Mà để điều chế 0,15 mol Cl2 thì cần 0,15 mol MnO2 tức 0,15.87=13,05 gam MnO2 và 0,6 mol HCl => VHCl 1M = 0,6 lít
Đúng 0
Bình luận (0)
Cần bao nhiêu gam KMnO4 và bao nhiêu ml dung dịch axit clohidric 1M để điều chế đủ khí clo tác dụng với sắt tạo nên 16,25 g FeCl3
2Fe+ 3Cl2=(t0) 2FeCl3
nFeCl3=16,25/162,5=0,1 mol => nCl2=3/2nFeCl3=3/2.0,1=0,15 mol
2KMnO4+ 16HCl=2KCl+2MnCl2+5Cl2+8H2O
nKMnO4=2/5.nCl2=2/5. 0,15=0,06 mol --> mKMnO4=0.06. 158=9,48 g
nHCl=16/5. nCl2=16/5. 0,15=0,48 mol
--> VddHCl=0,48/ 1=0,48 lit= 480 ml
Đúng 0
Bình luận (0)
Cần bao nhiêu gam KMnO4 và bao nhiêu ml dung dịch HCl 1M để điều chế đủ khí Clo tác dụng với Fe tạo nên 16,25 gam FeCl3 ?
Xem chi tiết
\(n_{FeCl_3}=\dfrac{16.25}{162.5}=0.1\left(mol\right)\)
\(Fe+\dfrac{3}{2}Cl_2\underrightarrow{t^0}FeCl_3\)
\(......0.15......0.1\)
\(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
\(0.06...............0.48........................................0.15\)
\(m_{KMnO_4}=0.06\cdot158=9.48\left(g\right)\)
\(V_{dd_{HCl}}=\dfrac{0.48}{1}=0.48\left(l\right)=480\left(ml\right)\)
Đúng 3
Bình luận (2)
\(2Fe+ 3Cl_2 \xrightarrow{t^o} 2FeCl_3\\ n_{Cl_2} = \dfrac{3}{2}n_{FeCl_3} = \dfrac{3}{2}.\dfrac{16,25}{162,5} = 0,15(mol)\\ 2KMnO_4 + 16HCl \to 2KCl + 2MnCl_2 + 5Cl_2 + 8H_2O\\ n_{KMnO_4} = \dfrac{2}{5}n_{Cl_2} = 0,06(mol)\\ \Rightarrow m_{KMnO_4} = 0,06.158 = 9,48(gam)\\ n_{HCl} = \dfrac{16}{4}n_{Cl_2} = 0,48(mol)\\ \Rightarrow V_{dd\ HCl} = \dfrac{0,48}{1} = 0,48(lít) = 480(ml)\)
Đúng 1
Bình luận (0)
cần bao nhiêu gam KMnO4 và bao nhiêu mililít dung dịch axit clohidric 1M để điều chế đủ khí clo tác dụng với sắt , tạo nên 16,25 g FeCl3
2KMnO4 + 16HCl ---> 2KCl + 2MnCl2 + 5Cl2 + 8H2O
2Fe + 3Cl2 ---> 2FeCl3
Để điều chế đủ khí Clo thì số mol Cl2 = 3/2 số mol FeCl3 = 1,5.16,25/162,5 = 0,15 mol.
Số mol KMnO4 = 2/5 số mol Cl2 = 0,06 mol; m(KMnO4) = 0,06.158 = 9,48 g
V(HCl) = 0,48/1 = 480 ml.
Đúng 0
Bình luận (0)
KMnO4 + 16HCl ---> 2KCl + 2MnCl2 + 5Cl2 + 8H2O
2Fe + 3Cl2 ---> 2FeCl3
Để điều chế đủ khí Clo thì số mol Cl2 = 3/2 số mol FeCl3 = 1,5.16,25/162,5 = 0,15 mol.
Số mol KMnO4 = 2/5 số mol Cl2 = 0,06 mol; m(KMnO4) = 0,06.158 = 9,48 g
V(HCl) = 0,48/1 = 480 ml.
Đúng 0
Bình luận (0)
Cần bao nhieu gam KMnO4 và bao nhieu ml dd axit HCL 2M để dieu chế đủ luong khí clo tác dụng với sắt tạo nên 16,25 gam FeCl3
Cần bao nhiêu gam KMnO4 và bao nhiêu ml dd axit clohidric 1M để điều chế đủ khí clo tác dụng với sắt tạo nên 32,5g FeCl3.
A.19,86g,958ml
B.18,96g.960ml
C 18,86g.720ml
D.18,68g.880ml
\(2KMnO_4+16HCl\rightarrow2MnCl_2+2KCl+5Cl_2+8H_2O\)
\(2Fe+3Cl_2\rightarrow2FeCl_3\)
Ta có :
\(n_{FeCl3}=\frac{32,5}{56+35,5.3}=0,2\left(mol\right)\)
\(n_{Cl2}=\frac{3}{2}n_{FeCl3}=0,3\left(mol\right)\)
Theo phản ứng:
\(n_{KMnO4}=\frac{2}{5}n_{Cl2}=0,12\left(mol\right)\Rightarrow m_{KMnO4}=0,12.\left(39+55+16.4\right)=96\left(g\right)\)
\(n_{HCl}=\frac{16}{5}n_{Cl2}=0,96\left(mol\right)\)
\(\Rightarrow V_{HCl}=\frac{0,96}{1}=0,96\left(l\right)=960\left(ml\right)\)
Bao nhiêu gam clo tác dụng vừa đủ kim loại sắt tạo ra 32,5 gam FeCl3?
A. 21,3 gam
B. 14,2 gam.
C. 13,2 gam.
D. 23,1 gam.
Người ta điều chế khí ClO trong phòng thí nghiệm từ MnO2 với dd HCl đậm đặc. Nếu dùng 200ml dd HCl 2M thì phải dùng bao nhiêu g MnO2?
200ml = 0,2l
\(n_{HCl}=2.0,2=0,4\left(mol\right)\)
Pt : \(MnO_2+4HCl_{đặc}\underrightarrow{t^o}MnCl_2+Cl_2+2H_2O|\)
1 4 1 1 2
0,1 0,4
\(n_{MnO2}=\dfrac{0,4.1}{4}=0,1\left(mol\right)\)
⇒ \(m_{MnO2}=0,1.87=8.7\left(g\right)\)
Chúc bạn học tốt
Đúng 5
Bình luận (0)