dẫn từ từ 11,2 lít hỗn hợp X gồm metan, etilen, axetilen vào dd Br2 dư thấy có 80g Br2 phản ứng và thoát ra 2,24 lít khí (đktc).
a) tính % V từng khí trong X
b) tính khối lượng của bình đựng dd Br2 tăng lên
Cho 3,36 lít ( đktc ) hỗn hợp Y gồm axetilen và metan đi qua bình đựng dung dịch Br2 dư, sau phản ứng thấy thoát ra 2,24 lít khí ( đktc ). a. Viết phương trình phản ứng. b. Tính số mol mỗi khí trong hỗn hợp. c. Tính % về khối lượng từng khí trong hỗn hợp.
Cứu với! Mình hiện đang rất cần gấp!!
a. Phương trình phản ứng giữa axetilen và dung dịch Br2:
C2H2 + Br2 → C2H2Br2
b. Theo định luật Avogadro, số mol khí thể tích bằng nhau ở cùng điều kiện nhiệt độ và áp suất. Vì vậy, số mol của hỗn hợp Y bằng số mol của khí thoát ra sau phản ứng.
Theo đó, ta có thể tính số mol mỗi khí trong hỗn hợp:
Số mol khí thoát ra: n = V/ Vm = 2,24/ 22,4 = 0,1 molSố mol axetilen ban đầu: n(C2H2) = n = 0,1 molSố mol metan ban đầu: n(CH4) = (V(Y) - V(C2H2)) / Vm = (3,36 - 2,24) / 22,4 = 0,05 molc. Để tính % về khối lượng từng khí trong hỗn hợp, ta cần biết khối lượng riêng của từng khí. Ở đktc, khối lượng riêng của axetilen là 1,096 g/L và khối lượng riêng của metan là 0,717 g/L.
Khối lượng axetilen trong hỗn hợp: m(C2H2) = n(C2H2) x M(C2H2) = 0,1 x 26 = 2,6 gKhối lượng metan trong hỗn hợp: m(CH4) = n(CH4) x M(CH4) = 0,05 x 16 = 0,8 gTổng khối lượng của hỗn hợp Y: m(Y) = V(Y) x ρ(Y) = 3,36 x 1,25 = 4,2 gVậy, % về khối lượng của axetilen trong hỗn hợp là:
% m(C2H2) = (m(C2H2) / m(Y)) x 100% = (2,6 / 4,2) x 100% = 61,9%
% về khối lượng của metan trong hỗn hợp là:
% m(CH4) = (m(CH4) / m(Y)) x 100% = (0,8 / 4,2) x 100% = 19,0%
Dẫn 2,24 lít (đktc) hỗn hợp A (gồm C2H4 và C2H6) vào bình đựng dung dịch Br2, thấy bình Br2 bị nhạt màu và có khí thoát ra. Sau phản ứng thấy khối lượng bình Br2 tăng 1,40 gam. Tính % thể tích từng khí trong hỗn hợp A?
nhh khí = 2,24/22,4 = 0,1 (mol)
nC2H4 = 1,4/28 = 0,05 (mol)
%VC2H4 = 0,05/0,1 = 50%
%VC2H6 = 100% - 50% = 50%
Hỗn hợp khí X gồm metan và etilen. Cho 5,6 lít X (đktc) qua bình đựng dung dịch Br2 dư, thấy lượng Br2 phản ứng là 24 gam và có m gam khí Y thoát ra ngoài.
a) Viết PTHH và tính m
b) Tính thành phần phần trăm về thể tích các khí trong X
C2H4+Br2->C2H4Br2
0,15---0,15
n Br2=\(\dfrac{24}{160}\)=0,15 mol
VCH4=5,6-0,15.22,4=2,24l
=>n CH4=\(\dfrac{2,24}{22,4}\)=0,1mol
=>m CH4=0,1.16=16g
=>%CH4=\(\dfrac{2,24}{5,6}\).100=40%
=>%C2H4=100-40=60%
Dẫn 8,96 l hỗn hợp X gồm metan và etilen vào 200ml dd Br2. Sau pư hoàn toàn thấy thoát ra 2,24l khí
a, Tính %V mỗi khí trong hỗn hợp X
b,Tính Cm dd Br2 pư và cho biết sau khi pư kết thúc khối lượng bình Br2 tăng hay giảm bao nhiêu gam ?
a)
$V_{CH_4} = V_{khí\ thoát\ ra} = 2,24(lít)$
$\%V_{CH_4} = \dfrac{2,24}{8,96}.100\% = 25\%$
$\%V_{C_2H_4} = 100\% -25\% = 75\%$
b)
$n_{Br_2} = n_{C_2H_4} = \dfrac{8,96.75\%}{22,4} = 0,3(mol)$
$C_{M_{Br_2}} = \dfrac{0,3}{0,2} = 1,5M$
$m_{tăng} = m_{C_2H_4} = 0,3.28 = 8,4(gam)$
Cho 13,34 lít hỗn hợp gồm 2 khí là metan và axetilen đi qua bình đựng dd Br2 dư , thì dùng hết 250ml dd Br2 và thoát ra 5,6 lít khí
a/ Tính thành phần % thể tích các khí trong hỗn hợp
b/ Tính nồng độ mol dd Br đã dùng
c/ Tính thể tích O2 (đktc) cần dùng để đốt cháy hoàn toàn hỗn hợp khí trên.
mọi người giúp mik với mai mik kiểm tra 1 tiết rồi !!
Khí thoát ra là metan
\(\%V_{CH_4} = \dfrac{5,6}{13,44}.100\% =41,67\%\\ \%V_{C_2H_4} = 100\% - 41,67\% = 58,33\%\\ b) V_{C_2H_2} = 13,44 -5,6 = 7,84(lít)\\ n_{C_2H_2} = \dfrac{7,84}{22,4} = 0,35(mol)\\ C_2H_2 + 2Br_2 \to C_2H_2Br_4\\ n_{Br_2} = 2n_{C_2H_2} = 0,7(mol)\\ \Rightarrow C_{M_{Br_2}} = \dfrac{0,7}{0,25} = 2,8M\\ c)\)
\(CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O\\ C_2H_4 + 3O_2 \xrightarrow{t^o} 2CO_2 + 2H_2O\\ V_{O_2} = 2V_{CH_4} + 3V_{C_2H_4} = 5,6.2 + 7,84.3 = 34,72(lít)\)
Cho hỗn hợp 7.437 lít khí metan và etilen vào dd brom dư thấy có 200g dd brom dư thấy có 200g dd br2 8% phản ứng hết
a/viết pt
b/tính % V từng khí
c/tính Vo2 cháy hết lượng khí trên
a) \(n_{Br_2\left(p\text{ư}\right)}=\dfrac{200.8\%}{160}=0,1\left(mol\right);n_{hh}=\dfrac{7,437}{24,79}=0,3\left(mol\right)\)
PTHH: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
0,1<-----0,1
b) \(\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,1}{0,3}.100\%=33,33\%\\\%V_{CH_4}=100\%-33,33\%=66,67\%\end{matrix}\right.\)
c) \(n_{CH_4}=0,3-0,1=0,2\left(mol\right)\)
PTHH: \(CH_4+2O_2\xrightarrow[]{t^o}CO_2+2H_2O\)
0,2--->0,4
\(C_2H_4+3O_2\xrightarrow[]{t^o}2CO_2+2H_2O\)
0,1--->0,3
\(\Rightarrow V_{O_2}=\left(0,3+0,4\right).24,79=17,353\left(l\right)\)
Dẫn từ từ 5,6 lít hỗn hợp gồm metan và etilen đi qua bình đựng dd Brom dư, thấy có 1,12 lít một chất khí thoát ra khỏi bình.
a) Viết PTPƯ, cho biết tên chất khí thoát ra khỏi bình.
b) Tính % thể tích từng chất khí trong hỗn hợp.
c) Tính khối lượng dd Brom đã tham gia phản ứng. Biết các khí đều đo ở đktc.
a, PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
Khí thoát ra khỏi bình là CH4 (metan).
b, Ta có: \(\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{1,12}{5,6}.100\%=20\%\\\%V_{C_2H_4}=100-20=80\%\end{matrix}\right.\)
c, Ta có: \(V_{C_2H_4}=5,6.80\%=4,48\left(l\right)\)
\(\Rightarrow n_{C_2H_4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Theo PT: \(n_{Br_2}=n_{C_2H_4}=0,2\left(mol\right)\)
\(\Rightarrow m_{Br_2}=0,2.160=32\left(g\right)\)
Bạn tham khảo nhé!
Câu 11. Dẫn 8,96 lít hỗn hợp khí metan, etilen và axetilen qua bình đựng dung dịch Br2 dư thấy có 64 gam Br2 pư. Nếu đốt cháy hoàn toàn hỗn hợp trên thu được 15,68 lít khí CO2.
a) Tìm % thể tích và % khối lượng mỗi khí trong hỗn hợp đầu?
b) Tính khối lượng rượu etylic cần dùng để điều chế lượng khí etilen trên?
\(a,Gọi\left\{{}\begin{matrix}n_{CH_4}=a\left(mol\right)\\n_{C_2H_4}=b\left(mol\right)\\n_{C_2H_2}=c\left(mol\right)\end{matrix}\right.\\ n_{hhkhí}=0,4\left(mol\right)\\ n_{CO_2}=\dfrac{15,68}{22,4}=0,7\left(mol\right)\\ n_{Br_2}=\dfrac{64}{160}=0,4\left(mol\right)\\ PTHH:C_2H_4+Br_2\rightarrow C_2H_4Br_2\\ Mol:a\rightarrow a\\ C_2H_2+2Br_2\rightarrow C_2H_2Br_4\\ Mol:b\rightarrow2b\\ CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\\ Mol:a\rightarrow2a\rightarrow a\)
\(C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\\ Mol:b\rightarrow3b\rightarrow2b\\ 2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\\ Mol:c\rightarrow2,5c\rightarrow2c\\ Hệ.pt\left\{{}\begin{matrix}a+b+c=0,4\\b+2c=0,4\\a+2b+2c=0,7\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,1\left(mol\right)\\b=0,2\left(mol\right)\\c=0,1\left(mol\right)\end{matrix}\right.\)
\(\%V_{CH_4}=\%V_{C_2H_2}=\dfrac{0,1}{0,4}=25\%\\ \%V_{C_2H_4}=\dfrac{0,2}{0,4}=50\%\)
\(m_{CH_4}=0,1.16=1,6\left(g\right)\\ m_{C_2H_4}=28.0,2=5,6\left(g\right)\\ m_{C_2H_2}=0,1.26=2,6\left(g\right)\\ \%m_{CH_4}=\dfrac{1,6}{1,6+5,6+2,6}=16,32\%\\ \%m_{C_2H_4}=\dfrac{5,6}{1,6+5,6+2,6}=57,14\%\\ \%m_{C_2H_2}=100\%-16,32\%-57,14\%=26,54\%\)
\(b,PTHH:C_2H_5OH\rightarrow C_2H_4+H_2O\\ Mol:0,2\leftarrow0,2\\ m_{C_2H_5OH}=0,2.46=9,2\left(g\right)\)
Dài quá!!!
Một hỗn hợp A gồm etan (C2H6), etilen, axetilen, hiđro. Tỉ khối của hỗn hợp A so với CO2 là 0,4. Cho 11,2 lít hỗn hợp A đi qua dung dịch Br2 dư thấy khối lượng bình Br2 tăng thêm m gam. Hỗn hợp khí B thoát ra khỏi bình Br2 có thể tích 6,72 lít, trong đó khí có khối lượng phân tử nhỏ hơn chiếm 11,765% về khối lượng. Biết các phản ứng xảy ra hoàn toàn và các thể tích khí đo ở điều kiện tiêu chuẩn.
a. Viết các phương trình hóa học xảy ra.
b. Tính phần trăm thể tích các khí trong B.
c. Tính m gam.
a. Phương trình phản ứng :
C2H2 + 2Br2 → C2H2Br4 (1)
C2H4 + Br2 → C2H4Br2 (2)
b. Hỗn hợp khí B gồm có H2, C2H6. Gọi x, y ( mol ) lần lượt là số mol của H2 và C2H6 có trong 6,72 lít hỗn hợp B.
nB = x + y = 6,72 : 22,4 = 0,3 mol (I)
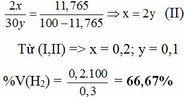
% V(C2H6) = 100% – 66,67% = 33,33%
c. nA = 11,2 : 22,4 = 0,5 mol , M A = 0,4 . 44 = 17,6 g/ mol
mA = 0,5 . 17,6 = 8,8 gam
mB = 0,2 . 2 + 0,1 . 30 = 3,4 gam
Vậy khối lượng bình Br2 tăng: m = mA – mB = 8,8 – 3,4 = 5,4 gam.