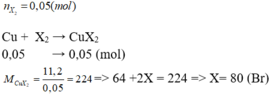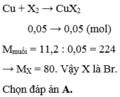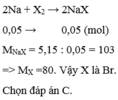Cho 1,12 lít halogen X2 tác dụng vừa đủ với kim loại đồng , thu được 11,2g CuX2 . Nguyên tố halogen đó là ??

Những câu hỏi liên quan
Cho 1,12 lít (đktc) halogen X2 tác dụng vừa đủ với đồng kim loại thu được 11,2 gam CuX2. Nguyên tố halogen là:
A. Flo
B. Clo
C. Brom
D. Iot
Cho 0,05 mol halogen X 2 tác dụng vừa đủ với đồng kim loại thu được 11,2 gam muối. Nguyên tố halogen là
A. Br.
B. Cl.
C. F.
D. I.
Giúp mình với ạ!
1. Cho 1.12l halogen X2 tác dụng vừa đủ với kl đồng, thu được 11.2 g CuX2 . Nguyên tố Halogen đó là gì?
2. Cho 10.8g kl M tác dụng với Clo tạo thành 53.4g muối clorua kim loại. Xác định kim loại M?
Bài 2 :
- Gọi hóa trị của kim loại M là x ( x > 0 )
PTHH : \(2M+xCl_2\rightarrow2MCl_x\)
\(n_M=\frac{m_M}{M_M}=\frac{10,8}{M_M}\left(mol\right)\)
\(n_{MCl_x}=\frac{m_{MCl_x}}{M_{MCl_x}}=\frac{53,4}{M_M+35,5x}\left(mol\right)\)
- Theo PTHH : \(n_M=n_{MCl_x}\left(mol\right)\)
=> \(\frac{10,8}{M_M}=\frac{53,4}{M_M+35,5x}\)
=> \(10,8M_M+383,4x=53,4M_M\)
=> \(383,4x=42,6M_M\)
=> \(M_M=9x\)
- Lập bảng giá trị :
-> MM = 27 ( đvc ) khi x = 3 .
Vậy M là kim loại nhôm ( Al ) .
1/n(X2) = 0,05 (mol)
=> n(Cu) = 0,05 (mol)
=> m(Cu) = 3,2 (g)
=> m(X2) = m(CuX2) - m(Cu) = 8 (g)
=> M(X2) = 8/0,05 = 160 => Br2
Vậy X là Brom
Cho 1,15 gam Na tác dụng vừa đủ với halogen X 2 thu được 5,15 gam muối. Nguyên tố halogen X là
A. Flo.
B. Clo.
C. Brom.
D. Iot.
Cho 2,24lit halogen X2 ở đktc tác dụng vừa đủ với magie thu được 9,5 g mgX2 .tìm nguyên tố halogen X
Mg + X2 -> MgX2
nX2 = 2,24/22,4 = 0,1 ( mol )
=> nMgX2 = 0,1 ( mol )
=> M = 9,5 / 0,1 = 95 ( đvC )
mà : MgX2 = 24 + X.2 = 95
=> X = 35,5 ( Cl )
Đó là Clo
Đúng 3
Bình luận (2)
nX2 = 2,24/22,4 = 0,1 (mol)
PTHH: Mg + X2 -> (t°) MgX2
nMgX2 = nX2 = 0,1 (mol)
M(MgX2) = 9,5/0,1 = 95 (g/mol)
<=> 24 + X . 2 = 95
<=> X = 35,5
<=> X là Cl
Đúng 0
Bình luận (0)
Cho 4,26g đơn chất Halogen X2 tác dụng vừa đủ với kim loại R thuộc nhóm IIA thu được 6,66g muối Halogen . Xác định X và R ?
Xem chi tiết
Bảo toàn khối lượng ta có: $m_{R}=2,4(g)$$R+X_2\rightarrow RX_2$
Ta có: $\frac{2,4}{R}=\frac{4,26}{2X}$
Lập bảng biện luận thông qua halogen tìm được X và R lần lượt là Cl và Ca
Đúng 1
Bình luận (3)
nX2 = nRX2 ⇒ \(\dfrac{4,26}{2X}=\dfrac{6,66}{R+2X}\)
⇒ 4,26R + 8,52X = 13.32X
⇒ 4,26R = 4,8X
⇒ \(\dfrac{X}{R}=\dfrac{80}{71}=\dfrac{40}{35,5}\)
⇒ X là Ca còn R là Cl
Đúng 0
Bình luận (0)
Cho 0,24 gam kim loại Mg tác dụng vừa đủ với khí Halogen X2,sau phản ứng thu được 1,84 gam muối khan.Xác định công thức và tên của muối Halogen thu được?
Xem chi tiết
PTHH: \(Mg+X_2\rightarrow MgX_2\)
Ta có: \(\dfrac{0,24}{24}=\dfrac{1,84}{24+2\cdot M_X}\) \(\Rightarrow M_X=80\)
Vậy Halogen cần tìm là Brom
Muối thu được là Magie Bromua
Đúng 2
Bình luận (0)
Câu 5: Cho 13,44g Cu tác dụng vừa đủ với 33,6g halogen X2 (đktc). Tìm halogen X2
Câu 6: Cho 1,38g một kim loại Na tác dụng hết với halogen X2 thu đc 9g muối. Tìm halogen X2
\(Cu+X2-->CuX2\)
\(n_{Cu}=\frac{13,44}{64}=0,21\left(mol\right)\)
\(n_{X2}=n_{Cu}=0,21\left(mol\right)\)
\(M_{X2}=\frac{33,6}{0,21}=160\)
\(=>X=80\left(Br\right)\)
Vậy......
Câu 6
\(2Na+X2-->2NaX\)
\(m_{X2}=m_{muối}-m_{Na}=9-1,38=7,62\)
\(n_{Na}=\frac{1,38}{23}=0,06\left(mol\right)\)
\(n_{X2}=\frac{1}{2}n_{Na}=0,03\left(mol\right)\)
\(M_{X2}=\frac{7,62}{0,03}=245=>X=127\left(I\right)\)
bài 5
Cu+X2--->CuX2
0,21--0,21 mol
nCu=13,44\64=0,21(mol)
nX2=nCu=0,21(mol)
MX2=33,6\0,21=160
-->X=80(Brom)
Câu 6
2Na+X2−−>2NaX
0,06---0,03 mol
mX2=mmuối−mNa
->mX2=9−1,38=7,62
nNa=1,38\23=0,06(mol)
MX2=7,62\0,03=245
-->X=127(Iôt)
4, Cho 18,4g hỗn hợp 2 kim loại Cu và Fe phản ứng vừa đủ với V lít khí Cl2 (đktc) thu được 43,25g hỗn hợp 2 muối clorua kim loại. Tìm V?
5, Cho 30,8g hỗn hợp 3 kim loại Zn, Cu và Mg phản ứng vừa đủ với V lít khí F2 (đktc) thu được 53,6g hỗn hợp 3 muối florua kim loại. Tìm V?
6, Cho 1 lượng halogen X2 tác dụng hết với kim loại kẽm thì thu được 13,6g muối. Cũng lượng halogen X2 đem tác dụng với kim loại K thì thu được 14,9g muối. X2 là?
Đọc tiếp
4, Cho 18,4g hỗn hợp 2 kim loại Cu và Fe phản ứng vừa đủ với V lít khí Cl2 (đktc) thu được 43,25g hỗn hợp 2 muối clorua kim loại. Tìm V?
5, Cho 30,8g hỗn hợp 3 kim loại Zn, Cu và Mg phản ứng vừa đủ với V lít khí F2 (đktc) thu được 53,6g hỗn hợp 3 muối florua kim loại. Tìm V?
6, Cho 1 lượng halogen X2 tác dụng hết với kim loại kẽm thì thu được 13,6g muối. Cũng lượng halogen X2 đem tác dụng với kim loại K thì thu được 14,9g muối. X2 là?
4) \(m_{Cl_2}=43,25-18,4=24,85g\)
\(n_{Cl_2}=\frac{24,85}{71}=0,35mol\)
\(V_{Cl_2}=0,35.22,4=7,84l\)
Đúng 0
Bình luận (2)
5) \(m_{F_2}=53,6-30,8=22,8g\)
\(n_{F_2}=\frac{22,8}{39}=0,6mol\)
\(V_{F_2}=0,6.22,4=13,44l\)
Đúng 0
Bình luận (0)