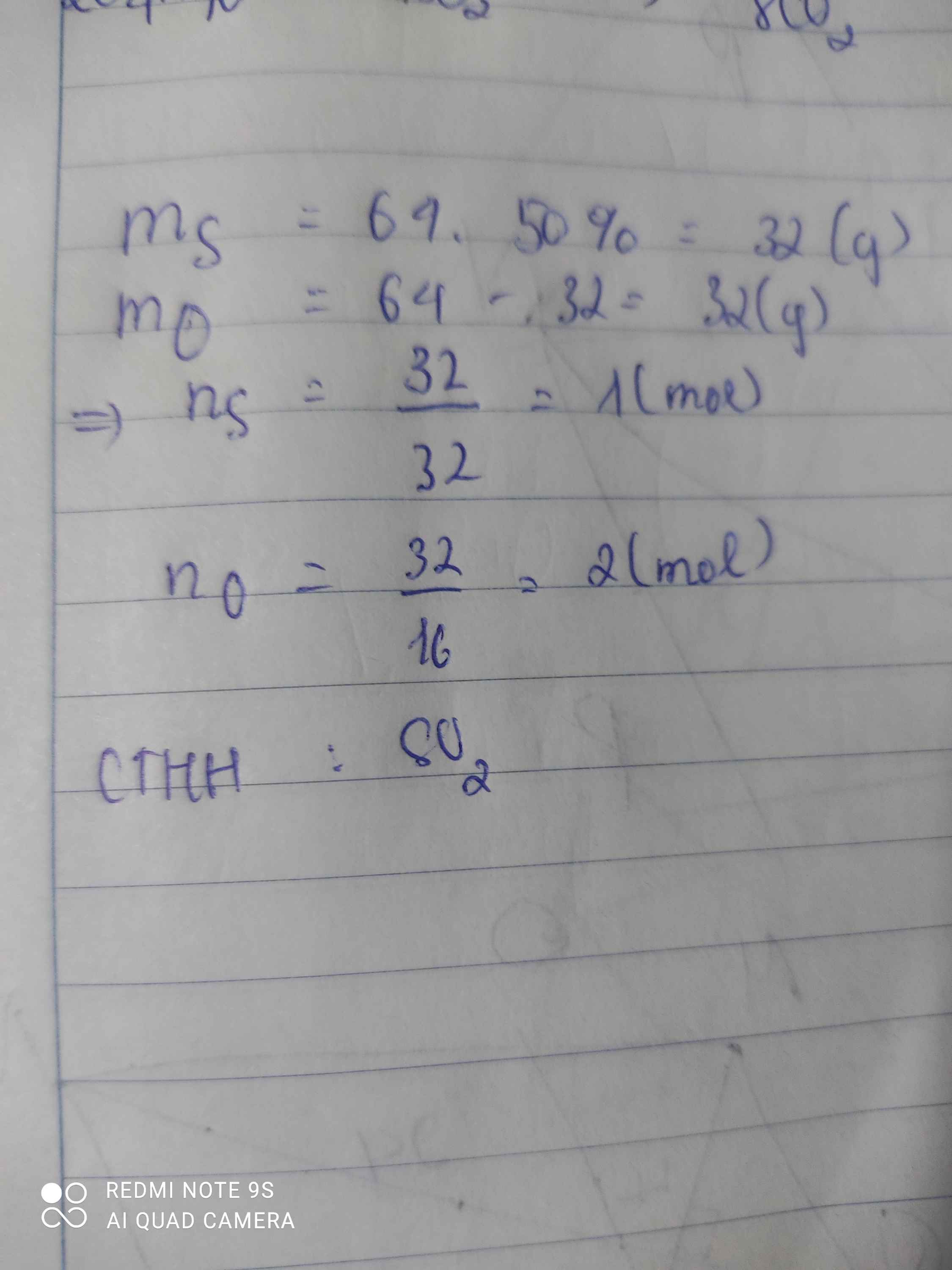Lập CTHH của hợp chất tạo bởi S và O biết S chiếm 50% và khối lượng mol của hợp chất

Những câu hỏi liên quan
Hợp chất A tạo bởi 2 nguyên tố là S và O lập cth^2 của A . Biết S chiếm 50% và khối lượng
Gọi CTHH của hợp chất `A` là: `S_xO_y`
Biết `S` chiếm `50%` về khối lượng, ta có:
\(\dfrac{M_S.100\%}{M_{S_xO_Y}}=50\%\\ \Leftrightarrow\dfrac{32.100}{32x+16y}=50\\ \Leftrightarrow32x+16y=64\)
Vì `x,y` nguyên nên suy ra: `x=1` và `y=2`
Vậy CTHH của `A` là `SO_2`
$HaNa$♬
Đúng 0
Bình luận (0)
Câu 18: Xác định CTHH của hợp chất khi biết % mỗi nguyên tố.
Bài tập: Lập CTHH của hợp chất tạo bởi 80% Cu và 20% O
- Lập CTHH của hợp chất tạo bởi 39,32 % Na và 60,68 % Cl
- Lập CTHH của hợp chất tạo bởi 40% Cu, 20% S và 40% O
\(Đặt:CTTQ:Cu_xO_y\left(x,y:nguyên,dương\right)\\ \%m_{Cu}=80\%\\ \Leftrightarrow\dfrac{64x}{64x+16y}=80\%\\ \Leftrightarrow320x=256x+64y\\ \Leftrightarrow64x=64y\\ \Leftrightarrow\dfrac{x}{y}=\dfrac{64}{64}=\dfrac{1}{1}\Rightarrow x=1;y=1\\ \Rightarrow CTHH:CuO\)
Tương tự em làm cho 2 ý dưới sẽ ra NaCl và CuSO4
Đúng 3
Bình luận (0)
Câu 1. Lập CTHH của hợp chất tạo bởi S và O, trong đó S chiếm 40% về khối lượng còn lại là O. Biết khối lượng phân tử của hợp chất là 80amu.
Câu 2. Một xe máy đi nửa đoạn đường đầu tiên với vtb là 60km/h, nửa đoạn đường sau với vtb là 40km/h. Tính vtb của cả 2 đoạn đường.
Câu 1:
Gọi CTTQ là SxOy.
Ta có:
%mS = 40%
%mO = 100% - 40% = 60%
\(x=\dfrac{\%m_S
.
M_{S_xO_y}}{M_S}
=\dfrac{40\%
.
80}{32}=1\)
\(y=\dfrac{\%m_O
.
M_{S_xO_y}}{M_O}=\dfrac{60\%
.
80}{16}=3\)
Thay x,y bằng những kết quả đã cho
=> CTHH là SO3.
Đúng 2
Bình luận (2)
Câu 2:
Tóm tắt:
\(V_{tb_1}\) = 60 km/h
\(V_{tb_2}\) = 40 km/h
\(V_{tb_{tong}}\) = ?
Giải
Gọi nửa đoạn đường là S
⇒ Cả quãng đường là 2.S(km)
Thời gian xe máy đi được quãng đường thứ nhất là:
\(t_1=\dfrac{S}{v_1}=\dfrac{S}{60}\left(h\right)\)
Thời gian xe máy đi được quãng đường thứ hai là:
\(t_2=\dfrac{S}{v_2}=\dfrac{S}{40}\left(h\right)\)
Ta có, vận tốc trung bình của xe đi trên cả hai đoạn đường là:
\(V_{tb}=\dfrac{2S}{t_1+t_2}=\dfrac{2
.
S}{\dfrac{S}{60}+\dfrac{S}{40}}=\dfrac{2
.
S}{S\left(\dfrac{1}{60}+\dfrac{1}{40}\right)}=\dfrac{2}{\dfrac{1}{60}+\dfrac{1}{40}}=48\) (km/h)
Đúng 2
Bình luận (0)
tìm CTHH của hợp chất gồm 50% S và 50% O biết khối lượng mol hợp chất là 64 gam
Lập công thức hóa học của hợp chât tạo bởi S và O biết % khối lượng của S: O lần lượt là 50% 50% và khối lượng phân tử của hợp chất là 64 amu Giúp tui với
Gọi ct chung: \(\text{S}_{\text{x}}\text{O}_{\text{y}}\)
\(\text{PTK = }32\cdot\text{x}+16\cdot\text{y}=64\text{ }< \text{amu}>\)
\(\%\text{S}=\dfrac{32\cdot\text{x}\cdot100}{64}=50\%\)
`-> 32*\text {x}*100 = 50*64`
`-> 32*\text {x}*100=3200`
`-> 32\text {x}=32`
`-> \text {x}=1`
Vậy, số nguyên tử `\text {S}` trong phân tử `\text {S}_\text {x} \text {O}_\text {y}` là `1`
\(\%\text{O}=\dfrac{16\cdot\text{y}\cdot100}{64}=50\%\)
`-> \text {y = 2 (tương tự ngtử S)}`
Vậy, số nguyên tử `\text {O}` trong phân tử `\text {S}_\text {x} \text {O}_\text {y}` là `2`
`=> \text {CTHH: SO}_2.`
Đúng 0
Bình luận (0)
Lập cthh tạo bởi hợp chất Fe, C, và O biết fe chiếm 48,28% C chiếm 10,34% và phân tử khối của hợp chất là 116
\(m_{Fe}=\dfrac{48,28.116}{100}=56\left(g\right)\Rightarrow n_{Fe}=\dfrac{56}{56}=1\left(mol\right)\)
\(m_C=\dfrac{10,34.116}{100}=12\left(g\right)\Rightarrow n_C=\dfrac{12}{12}=1\left(mol\right)\)
\(m_O=116-56-12=48\left(g\right)\Rightarrow n_O=\dfrac{48}{16}=3\left(mol\right)\)
=> CTHH: FeCO3
Đúng 2
Bình luận (0)
Một hợp chất khí Y được cấu tạo từ 2 nguyên tố hóa học: S và O trong đó S chiếm 50% về khối lượng của hợp chất. Biết rằng khối lượng mol của Y bằng 64 gam/mol. Tìm công thức của Y?
Giúp mình nhé
Ta có:
\(M_Y=64\left(\dfrac{g}{mol}\right)\\ \%S=50\%\\ m_S=64.50\%=32\left(g\right)\\ m_O=64-32=32\left(g\right)\\ n_S=\dfrac{32}{32}=1\left(mol\right)\\ n_{O_2}=\dfrac{32}{16}=2\left(mol\right)\\ CTHH:SO_2\)
Đúng 1
Bình luận (0)
Khối lg của S trong Y là: 64.50%= 32(g/mol)
Tỉ số của S trong Y là: 32:32=1
Khối lg của O trong Y là: 64.50%= 32(g/mol)
Tỉ số của O trong Y là: 32:16=2
=>CTHH của Y là: SO2
Đúng 1
Bình luận (0)
Lập cthh của các chất tạo bởi:
A, 75%C ;25%H và tỉ khối hợp chất so với khí hidro là 8
B, Na,S,O trong đó Na chiếm 32,4%; O chiếm 45,07% về khối lượng. Khối lượng mol phân tử là 142g
a) Gọi CTHH là: CxHy
\(M_{C_xH_y}=2\times8=16\left(g\right)\)
Ta có: \(12x\div16y=75\div25\)
\(\Rightarrow x\div y=\dfrac{75}{12}\div\dfrac{25}{1}\)
\(\Rightarrow x\div y=1\div4\)
Vậy CTHH đơn giản là (CH4)n
Ta có: \(16n=16\)
\(\Leftrightarrow n=1\)
Vậy CTHH là CH4
Đúng 0
Bình luận (0)
b) Gọi CTHH là NaxSyOz
\(\%S=100\%-32,4\%-45,07\%=22,53\%\)
Ta có: \(23x\div32y\div16z=32,4\div22,53\div45,07\)
\(\Rightarrow x\div y\div z=\dfrac{32,4}{23}\div\dfrac{22,53}{32}\div\dfrac{45,07}{16}\)
\(\Rightarrow x\div y\div z=2\div1\div4\)
Vậy CTHH đơn giản là (Na2SO4)n
Ta có: \(142n=142\)
\(\Leftrightarrow n=1\)
Vậy CTHH là Na2SO4
Đúng 0
Bình luận (2)
gọi CTHC : CxHy
x : y = \(\dfrac{75}{12}:\dfrac{25}{1}=6,25:25=1:4\)
CT đơn giản: CH4
Vì M= 8.2 = 16
đặt CTCT: (CH4)n = 16
=> 16n=16=>n=1
Vậy CTPT: CH4
b/
đặt CT: NaxSyOz
x:y:z = \(\dfrac{32,4}{23}:\dfrac{22,53}{32}:\dfrac{45,07}{16}=1,4:0,7:2,8=2:1:4\)
CT đơn giản: Na2SO4
Vì M = 142
đặt CT: (Na2SO4)n
=> 142n=142=> n=1
Vậy CTPT: Na2SO4
Đúng 0
Bình luận (1)
1) Xác định CTHH của hợp chất tạo bởi nguyên tố C và H, trong đó H chiếm 25% về khối lượng và khối lượng mol của hợp chất là 16g/mol. 2) Đốt cháy hoàn toàn 12 gam kim loại Mg.a. Tính thể tích khí oxi (đktc) cần dùng và khối lượng magie oxit MgO tạo rra.b. Cần bao nhiêu gam khí CO2 để có số phân tử bằng số phân tử khí oxi đã dùng ở trên.
Đọc tiếp
1) Xác định CTHH của hợp chất tạo bởi nguyên tố C và H, trong đó H chiếm 25% về khối lượng và khối lượng mol của hợp chất là 16g/mol.
2) Đốt cháy hoàn toàn 12 gam kim loại Mg.
a. Tính thể tích khí oxi (đktc) cần dùng và khối lượng magie oxit MgO tạo rra.
b. Cần bao nhiêu gam khí CO2 để có số phân tử bằng số phân tử khí oxi đã dùng ở trên.
\(m_H=16.0,25\%=4\left(g\right)\\ m_C=16-4=12\left(g\right)\\ n_H=\dfrac{4}{1}=4\left(mol\right)\\ n_C=\dfrac{12}{12}\left(mol\right)\\ CTHH:CH_4\)
Đúng 1
Bình luận (1)
a.\(PTHH:2Mg+O_2\underrightarrow{t^o}2MgO\)
\(n_{Mg}=\dfrac{12}{24}=0,5\left(mol\right)\)
Từ PTHH ta có:
Đốt 2 mol Mg với 1 mol khí oxi sinh ra 2 mol MgO
=> Đốt 0,5 mol Mg với 0,25 mol khí oxi sinh ra 0,5 mol MgO
\(\Rightarrow\left\{{}\begin{matrix}V_{O_2}=22,4.0,25=5,6\left(l\right)\\m_{MgO}=0,5.40=20\left(g\right)\end{matrix}\right.\)
\(\Rightarrow n_{CO_2}=n_{O_2}=0,25mol\\ \Rightarrow m_{CO_2}=44.0,25\left(g\right)\)
Đúng 0
Bình luận (0)