Hòa tan hết một lượng Ma vào dung dịch HCl 10% , thu được 46,88 gam dung dịch gồm NaCl và NaOH và 1,568 lít khí H2(đktc).
Nồng độ % của Nacl trong dung dịch là bn ?
Hòa tan hết một lượng Na vào dung dịch HCl 10% thu được 46,88 gam dung dịch gồm NaCl và NaOH và 1,568 lít H 2 (đktc). Nồng độ % NaCl trong dung dịch thu được là
A. 14,97
B. 12,48
C. 12,68
D. 15,38
Hòa tan hết một lượng Na vào dung dịch HCl 3,65% thu được 103,3 gam dung dịch gồm NaCl và NaOH và 1,68 lít H 2 (đktc). Nồng độ % NaCl trong dung dịch thu được là
A. 5,66
B. 12,48
C. 6,24
D. 7,84
Hòa tan hết 1 lượng Na vào dung dịch HCl 10% thu được 46,88g dung dịch gồm NaCl và NaOH và 1,568 lít H2 (đktc). Tính nồng độ % NaCl trong dung dịch
Hòa tan hết 17,2 gam hỗn hợp X gồm Fe và một oxit sắt vào 200 gam dung dịch HCl 14,6% thu được dung dịch A và 2,24 lít khí H2 (đktc). Thêm 33,0 gam nước vào dung dịch A được dung dịch B. Nồng độ phần trăm của HCl trong dung dịch B là 2,92%. Mặt khác, cũng hòa tan hết 17,2 gam hỗn hợp X vào dung dịch H2SO4 đặc, nóng thì thu được V lít khí SO2 duy nhất (đktc). a) Xác định công thức hóa học của oxit sắt trong hỗn hợp X.
Chỉ mình tại sao tính khối lượng Fe trong oxit lại tính như thế kia ạ( chỗ khoanh tròn màu đỏ )

Lấy khối lượng hỗn hợp trừ khối lượng oxit sắt nhé
Đề chưa giải ra đc nên chưa viết CTHH đc đâu nhé
Có khối lượng hỗn hợp là 17,2(g)
mO = 0,2 . 16
mFe = 0,1 . 56
Bạn lấy tổng trừ cho 0,2 . 16 và 0,1 . 56 là:
17,2 - 0,1.56 - 0,2.16 = 8,4(g)
Hòa tan 64,258 gam hỗn hợp rắn gồm Cu(NO3)2.5H2O và NaCl vào nước được dung dịch X. Điện phân X với cường độ dòng điện không đổi, sau một thời gian thì thu được dung dịch Y có khối lượng giảm đi 18,79 gam so với dung dịch X. Cho 10 gam Fe vào dung dịch Y đến khi phản ứng xảy ra hoàn toàn thu được m gam chất rắn T gồm 2 kim loại, đồng thời thoát ra 1,568 lít hỗn hợp Z gồm 2 khí màu nâu đỏ (đktc), màu nâu đậm dần trong không khí, tỉ khối hơi của Z so với H2 là 129/7. Giá trị của m là:
A.5,928.
B.6,142.
C.4,886.
D.5,324.
Hòa tan hết 8,72 gam hỗn hợp X gồm Cr, CrO và Cr2O3 bằng một lượng dung dịch H2SO4 loãng vừa đủ thu được 1,568 lít H2 (đktc) và dung dịch Y. Cho toàn bộ dung dịch Y tác dụng với một lượng dư dung dịch NaOH, khuấy đều, lọc thu được 8,6 gam kết tủa và dung dịch Z trong suốt, sục khí Cl2 dư vào dung dịch Z, rồi lại thêm một lượng dư dung dịch BaCl2 thu được m gam kết tủa. Các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 10,12
B. 5,06
C. 42,34
D. 47,40
Hòa tan hết 8,72 gam hỗn hợp X gồm Cr, CrO và Cr2O3 bằng một lượng dung dịch H2SO4 loãng vừa đủ thu được 1,568 lít H2 (đktc) và dung dịch Y. Cho toàn bộ dung dịch Y tác dụng với một lượng dư dung dịch NaOH, khuấy đều, lọc thu được 8,6 gam kết tủa và dung dịch Z trong suốt, sục khí Cl2 dư vào dung dịch Z, rồi lại thêm một lượng dư dung dịch BaCl2 thu được m gam kết tủa. Các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 10,12.
B. 5,06.
C. 42,34.
D. 47,40.
Đáp án D
8,72 X C r : x m o l C r O : y m o l C r 2 O 3 : z m o l → H 2 S O 4 0 , 07 m o l H 2 + Y C r S O 4 : x + y C r ( S O 4 ) 3 : ≈ → d u N a O H ( y + x ) m o l C r ( O H ) 2 + Z N a [ C r ( O H ) 4 ] N a O H N a 2 S O 4 : x + y + 3 ≈ → + B a C l 2 + C l 2 B a C r O 4 : 2 B a S O 4 : x + y + 3
Gọi số mol của Cr, CrO, Cr2O3 lần lượt là x, y, z mol
Khi tác dụng với H2SO4 chỉ có Cr tác dụng sinh ra khí H2
Bảo toàn electron → x = nH2 = 0,07 mol
Có nCr(OH)2 = x+ y = 8,6 : 86 = 0,1 → y = 0,03 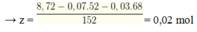
m↓ = 0,04. 253 + ( 0,07 + 0,03 + 3. 002) . 233= 47,4 gam.
Hòa tan hoàn toàn hỗn hợp X gồm Fe3O4 và FeS2 trong 63 gam dung dịch HNO3 thu được 1,568 lít khí NO2 duy nhất (đktc). Dung dịch thu được tác dụng vừa đủ với 200 ml dung dịch NaOH 2M, lọc kết tủa rồi đem nung trong không khí đến khối lượng không đổi thì thu được 9,76 gam chất rắn. Nồng độ phần trăm của dung dịch HNO3 ban đầu là:
A.42,6%.
B. 46,6%.
C. 47,2%.
D. 46,2%.
+ Tính được những gì có thể tính được
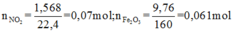
+ Với bài toán gồm nhiều giai đoạn liên tiếp nhau như thế này ta nên tóm tắt lại bài toán:
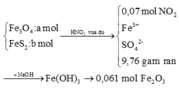
Bây giờ ta phải thiết lập được mối quan hệ giữa a và b với hi vọng là tìm được a và b rồi sau đó áp dụng các định luật bảo toàn như khối lượng, nguyên tố, electron ....
+ Bảo toàn nguyên tố Fe: 3a + b = nFe = 2.0,061 = 0,122
+ Bảo toàn sốmol electron trao đổi: a + 15b = 0,07.1 ( Chú ý FeS2→Fe3+ + 2S+6 + 15e)
Giải được a = 0,04; b = 0,002.
+ Tiếp tục sử dụng bảo toàn nguyên tố S:
![]()
+ Vì phản ứng xảy ra hoàn toàn và vừa đủ nên sau khi phản ứng với dung dịch NaOH ta chỉ thu được 2 muối là Na2SO4 và NaNO3.
Áp dụng định luật bảo toàn nguyên tố Na:
![]()
+ Cuối cùng dựa vào sơ đồ tóm tắt, ta sẽ dùng bảo toàn nguyên tố N
![]()
=>![]()
Đáp án D
1. (1,5 điểm) Hòa tan hết 36,1 gam hỗn hợp A gồm Fe và Al vào 200 mL dung dịch HCl (dùng vừa đủ).
Sau phản ứng thu được dung dịch B và 21,28 lít khí H2 (đktc). Hãy tính:
a. Khối lượng mỗi chất trong hỗn hợp A ban đầu.
b. Tính nồng độ dung dịch HCl đã dùng.
c. Tính nồng độ mol/l của chất tan trong dung dịch B.
a) PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
a_____2a______a_____a (mol)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
b_____3b_______b_____\(\dfrac{3}{2}\)b (mol)
Ta lập HPT: \(\left\{{}\begin{matrix}56a+27b=36,1\\a+\dfrac{3}{2}b=\dfrac{21,28}{22,4}=0,95\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,5\\b=0,3\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Fe}=0,5\cdot56=28\left(g\right)\\m_{Al}=8,1\left(g\right)\end{matrix}\right.\)
b+c) Theo các PTHH: \(\left\{{}\begin{matrix}n_{HCl}=2a+3b=1,9\left(mol\right)\\n_{FeCl_2}=0,5\left(mol\right)\\n_{AlCl_3}=0,3\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}C_{M_{HCl}}=\dfrac{1,9}{0,2}=9,5\left(M\right)\\C_{M_{FeCl_2}}=\dfrac{0,5}{0,2}=2,5\left(M\right)\\C_{M_{AlCl_3}}=\dfrac{0,3}{0,2}=1,5\left(M\right)\end{matrix}\right.\)