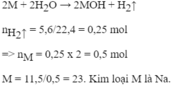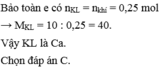cho 11,5g một kim loại kiềm tác dụng hết với nước thu được 5,6 lít khí hydro (đktc).xác định tên kim loại

Những câu hỏi liên quan
Cho 11,5 gam một kim loại kiềm tác dụng hết với nước thu được 5,6 lít khí hidro (đktc). Xác định tên của kim loại (Li=7, Na=23, K=39, Ba=137).
Bài 1: Cho 5.52g một kim loại kiềm tác dụng với nước tạo ra 2.688 lít khí H2 (đktc). Xác định tên kim loại đó.
Bài 2: Cho 1.84g một kim loại kiềm tác dụng với nước tạo ra 896ml khí H2 (đktc). Xác định tên kim loại đó.
Bài 1:
Gọi kim loại kiềm là R
\(n_{H_2}=\dfrac{2,688}{22,4}=0,12\left(mol\right)\)
Giả sử R hóa trị I:
\(R+H_2O\rightarrow ROH+\dfrac{1}{2}H_2\\ \Rightarrow n_R=0,12.2=0,24\left(mol\right)\\ \Rightarrow M_R=\dfrac{5,52}{0,24}=23\left(đvC\right)\)
Giả sử đúng, tên kim loại đó là sodium (Na)
Bài 2: Tự làm tương tự bài 1 nhé=0
Đúng 2
Bình luận (0)
Cho 8,0 gam một kim loại kiềm thổ ( hóa trị II) tác dụng với nước dư thu được 4,48 lít khí H2 (đktc). Xác định tên kim loại kiềm thổ trên?
Giúp em với
\(n_{H_2}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(M+2H_2O\rightarrow M\left(OH\right)_2+H_2\)
\(0.2........................................0.2\)
\(M_M=\dfrac{8}{0.2}=40\left(\dfrac{g}{mol}\right)\)
\(M:Ca\left(Canxi\right)\)
Đúng 3
Bình luận (1)
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: A + 2H2O --> A(OH)2 + H2
_____0,2<--------------------------0,2
=> \(M_A=\dfrac{8}{0,2}=40\left(g/mol\right)=>Ca\)
Đúng 0
Bình luận (0)
Cho 11,5g một kim loại A ( I ) tác dụng hết với nước tạo ra 5,6 lít khí Hiddro ( đktc) . Tìm kim loại A
\(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH: 2A + 2H2O --> 2AOH + H2
0,5<------------------0,25
=> \(M_A=\dfrac{11,5}{0,5}=23\left(g/mol\right)\)
=> A là Na
Đúng 3
Bình luận (0)
Cho 10 gam một kim loại kiềm thổ tác dụng hết với nước thoát ra 5,6 lít khí (đktc). Tên của kim loại kiềm thổ đó là ?
vi la kiem tho nen Pu voi nuoc la : R +2 H2O ->R(oh)2 +H2
nH2 = nR = 0.25mol => M(R) = 10/0.25 = 40 => R la Ca
Chon C
Đúng 0
Bình luận (0)
Cho 7,02 gam kim loại kiềm tác dụng hết với nước thu được 0,18 gam khí ( đktc). Xác định tên kim loại là ( Na=23, K=39, Ba=137, Ca=40)
Gọi CTHH của kim loại kiềm là A
A + H2O ----> AOH + 1/2H2
nH2 = 0,18/2 = 0,09 (mol)
Theo pthh : nA = 2nH2 = 0,18 (mol)
=> MA = mA/nA = 7,02/0,18 = 39 (g/mol)
=> Kim loại cần tìm là Kali
Đúng 1
Bình luận (0)
Cho 10 gam một kim loại kiềm thổ tác dụng hết với nước thoát ra 5,6 lít khí (đktc). Kim loại kiềm thổ đó là
A. Ba.
B. Mg.
C. Ca.
D. Sr.
Cho 10 gam một kim loại kiềm thổ M tác dụng hết với nước thoát ra 5,6 lít khí (đktc). Kim loại kiềm thổ đó là
A. Ba
B. Mg
C. Ca
D. Sr
Cho 7,1 gam hỗn hợp gồm một kim loại kiềm X và một kim loại kiềm thổ Y tác dụng hết với lượng dư dung dịch HCl loãng, thu được 5,6 lít khí (đktc). Kim loại X, Y là
A. Kali và bari
B. Liti và beri
C. Natri và magie
D. Kali và canxi