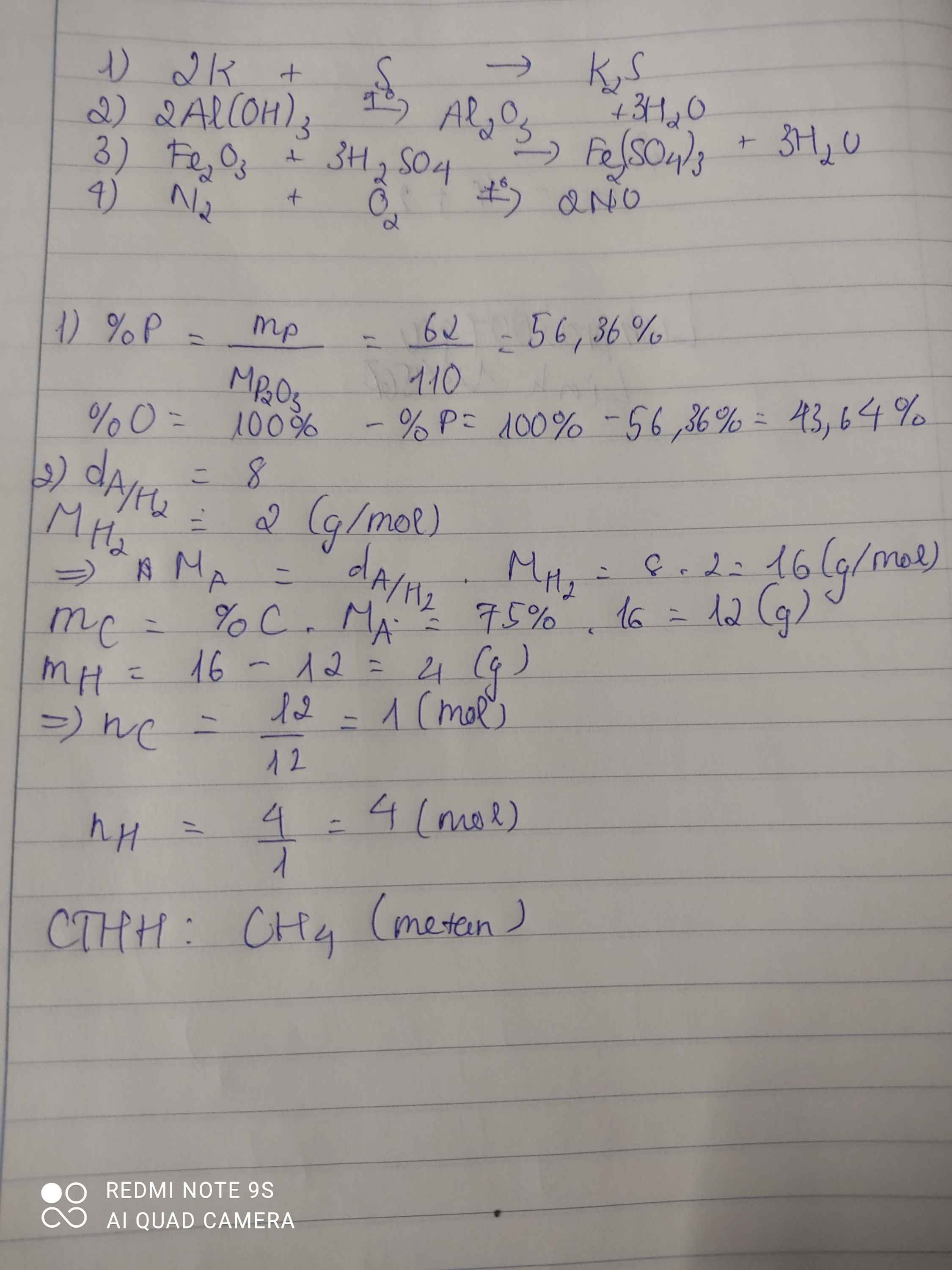Hợp chất B tạo thành 75 phần trăm C và 25 phần trăm H về khối lượng . Xác định CTHH của B, biết 1 mol khí B nặng 16g

Những câu hỏi liên quan
1.Tính thành phần phần trăm khối lượng các nguyên tố hoá học có trong hợp chất P2O3 2. Hợp chất A có chứa 75%C và 25%H về khối lượng, biết tỉ khối của A so với khí hiđrô bằng 8. Xác định CTHH của chất A
1
\(MP_2O_3=110g/mol\)
\(\%P=\dfrac{31.2.100}{110}=58,2\%\)
\(\%O=100-58,2=41,8\%\)
2
\(MA=8.2=16g/mol\)
Tính theo hoá trị
=> cthh của A là CH\(_4\)
Đúng 1
Bình luận (1)
tìm CTHH của hợp chất, biết:a/ khối lượng mol của hợp chất A là 142 gam,thành phần phần trăm theo khối lượng của các nguyên tố: 32,39%Na;22,54%S;45,07%Ob/ khối lượng mol của hợp chất B là 123 gam, thành phần phần trăm theo khối lượng của các nguyên tố: 58,5%C;4,1%H;11,4%N;26%Oc/ hợp chất C có khối lượng mol nặng gấp 23 lần khí hidro, thành phần phần trăm theo khối lượng của các nguyên tố: 52,17%C; 13,05%H; 34,74%O
Đọc tiếp
tìm CTHH của hợp chất, biết:
a/ khối lượng mol của hợp chất A là 142 gam,thành phần phần trăm theo khối lượng của các nguyên tố: 32,39%Na;22,54%S;45,07%O
b/ khối lượng mol của hợp chất B là 123 gam, thành phần phần trăm theo khối lượng của các nguyên tố: 58,5%C;4,1%H;11,4%N;26%O
c/ hợp chất C có khối lượng mol nặng gấp 23 lần khí hidro, thành phần phần trăm theo khối lượng của các nguyên tố: 52,17%C; 13,05%H; 34,74%O
a)
-Đặt công thức: NaxSyOz
x=\(\dfrac{32,29.142}{23.100}\approx2\)
y=\(\dfrac{22,54.142}{32.100}\approx1\)
z=\(\dfrac{45,07.142}{16.100}\approx4\)
-CTHH: Na2SO4
Đúng 1
Bình luận (0)
Câu b này mình giải cách khác câu a:
nC:nH:nN:nO=\(\dfrac{\%C}{12}:\dfrac{\%H}{1}:\dfrac{\%N}{14}:\dfrac{\%O}{16}=\dfrac{58,5}{12}:\dfrac{4,1}{1}:\dfrac{11,4}{14}:\dfrac{26}{16}\)
nC:nH:nN:nO=4,875:4,1:0,81:1,625=6:5:1:2
-Công thức nguyên: (C6H5NO2)n
-Ta có: (12.6+5+14+16.2)n=123\(\Leftrightarrow\)123n=123\(\Leftrightarrow\)n=1
-CTHH: C6H5NO2
Đúng 1
Bình luận (0)
Câu c:
\(M_C=23.2=46đvC\)
nC:nH:nO=\(\dfrac{\%C}{12}:\dfrac{\%H}{1}:\dfrac{\%O}{16}=\dfrac{52,17}{12}:\dfrac{13,05}{1}:\dfrac{34,74}{16}\)
nC:nH:nO=4,3475:13,05:2,17125\(\approx\)2:6:1
-Công thức nguyên: (C2H6O)n
-Ta có: (12.2+6+16)n=46\(\Leftrightarrow\)46n=46\(\Leftrightarrow\)n=1
-CTHH: C2H6O
Đúng 1
Bình luận (0)
một hợp chất X gồm 2 nguyên tố C và H, có tỉ khối với hidro là 8a,Hãy xác định CTHH của X biết hợp chất khí có thành phần phần trăm theo khối lượng của C bằng 75%.b,Hãy cho biết khí X ở điều kiện tiêu chuẩn có khối lượng là bao nhiêu?
Gọi CTHH của X là CxHy
Tỉ khối X so với H2 = 8 => Mx = 8.2 = 16(g/mol)
%mC = 75% , X chỉ chứa C và H => %mH = 100 - 75 = 25%
=> %mC = \(\dfrac{12.x}{16}\).100% = 75% <=> x = 1
%mH = \(\dfrac{y.1}{16}.100\)% = 25% <=> y = 4
Vậy CTHH của X là CH4.
Đúng 2
Bình luận (0)
một hợp chất X có thành phần trăm theo khối lượng là 42,875 phần trăm C và 57,143 phần trăm O . Xác định CTHH của hợp chát X , biết tỉ khối của X đối với khí là 0,875 .
a. Xác ddingj CTHH của hợp chất x , biết tie khối của X với khí oxi là 0,875
\(d_{\dfrac{X}{O_2}}=0,875\)
\(M_X=0,875.32=28\left(\dfrac{g}{mol}\right)\)
\(m_C=\dfrac{28.42,875}{100}\approx12g\)
\(m_O=\dfrac{28.57,143}{100}\approx16g\\ n_C=\dfrac{12}{12}=1mol\\ n_O=\dfrac{16}{16}=1mol\\ CTHH:CO\)
Đúng 2
Bình luận (0)
một hợp chất X có thành phần trăm theo khối lượng là 42,875 phần trăm C và 57,143 phần trăm O . Xác định CTHH của hợp chát X , biết tỉ khối của X đối với khí là 0,875
Đề bạn bị thiếu chỗ tỉ khối của X so với khí ?
\(ĐặtCTcủaX:C_xO_y\\ M_X=0,875M_{O_2}=28\left(g/mol\right)\\ Tacó:\%C=\dfrac{12x}{28}.100=42,875\Rightarrow x=1\\ \Rightarrow y=\dfrac{28-12}{16}=1\\ VậyCTX:CO\)
Đúng 2
Bình luận (0)
CTHH của hợp chất Y có dạng là NaxNyOz. Thành phần phần trăm theo khối lượng các nguyên tố Y như sau: 27,06% Na; 16,47% N và 56,47% O. xác định CTHH của Y, biết khối lượng mol của Y là 85g/mol
nêu các bước giải bài toán xác định CTHH của hợp chất khi biết thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chất
B1 : Tìm khối lượng của mỗi nguyên tố có trong 1 mol hợp chất.
B2 : Tìm số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất.
B3 : Lập CTHH.
Đúng 0
Bình luận (1)
còn xác định công thức hóa hc của Y nữa mà bn
Đúng 0
Bình luận (4)
Bước 1: Tìm khối lượng mol của nguyên tố có trong 1 mol hợp chất.
Bước 2: Tìm số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất.
Bước 3: Lập CTHH của hợp chất.
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
1) Xác định CTHH của hợp chất tạo bởi nguyên tố C và H, trong đó H chiếm 25% về khối lượng và khối lượng mol của hợp chất là 16g/mol. 2) Đốt cháy hoàn toàn 12 gam kim loại Mg.a. Tính thể tích khí oxi (đktc) cần dùng và khối lượng magie oxit MgO tạo rra.b. Cần bao nhiêu gam khí CO2 để có số phân tử bằng số phân tử khí oxi đã dùng ở trên.
Đọc tiếp
1) Xác định CTHH của hợp chất tạo bởi nguyên tố C và H, trong đó H chiếm 25% về khối lượng và khối lượng mol của hợp chất là 16g/mol.
2) Đốt cháy hoàn toàn 12 gam kim loại Mg.
a. Tính thể tích khí oxi (đktc) cần dùng và khối lượng magie oxit MgO tạo rra.
b. Cần bao nhiêu gam khí CO2 để có số phân tử bằng số phân tử khí oxi đã dùng ở trên.
\(m_H=16.0,25\%=4\left(g\right)\\ m_C=16-4=12\left(g\right)\\ n_H=\dfrac{4}{1}=4\left(mol\right)\\ n_C=\dfrac{12}{12}\left(mol\right)\\ CTHH:CH_4\)
Đúng 1
Bình luận (1)
a.\(PTHH:2Mg+O_2\underrightarrow{t^o}2MgO\)
\(n_{Mg}=\dfrac{12}{24}=0,5\left(mol\right)\)
Từ PTHH ta có:
Đốt 2 mol Mg với 1 mol khí oxi sinh ra 2 mol MgO
=> Đốt 0,5 mol Mg với 0,25 mol khí oxi sinh ra 0,5 mol MgO
\(\Rightarrow\left\{{}\begin{matrix}V_{O_2}=22,4.0,25=5,6\left(l\right)\\m_{MgO}=0,5.40=20\left(g\right)\end{matrix}\right.\)
\(\Rightarrow n_{CO_2}=n_{O_2}=0,25mol\\ \Rightarrow m_{CO_2}=44.0,25\left(g\right)\)
Đúng 0
Bình luận (0)
1) Xác định CTHH của hợp chất tạo bởi nguyên tố C và H, trong đó H chiếm 25% về khối lượng và khối lượng mol của hợp chất là 16g/mol. 2) Đốt cháy hoàn toàn 12 gam kim loại Mg.a. Tính thể tích khí oxi (đktc) cần dùng và khối lượng magie oxit MgO tạo rra.b. Cần bao nhiêu gam khí CO2 để có số phân tử bằng số phân tử khí oxi đã dùng ở trên.
Đọc tiếp
1) Xác định CTHH của hợp chất tạo bởi nguyên tố C và H, trong đó H chiếm 25% về khối lượng và khối lượng mol của hợp chất là 16g/mol.
2) Đốt cháy hoàn toàn 12 gam kim loại Mg.
a. Tính thể tích khí oxi (đktc) cần dùng và khối lượng magie oxit MgO tạo rra.
b. Cần bao nhiêu gam khí CO2 để có số phân tử bằng số phân tử khí oxi đã dùng ở trên.
Gọi CTTQ: \(C_xH_y\)
⇒ \(\%H=\dfrac{1.y}{16}=25\%\)
⇒ \(y=4\)
⇒ \(\%C=\dfrac{12.x}{16}=75\%\)
⇒ \(x=1\)
⇒ \(CTHH:CH_4\)
Đúng 1
Bình luận (0)
một hỗn hợp khí x gồm: O2,SO2 và CHx biết thành phần phần trăm về khối lượng của các chất trong X lần lượt là 40%, 40%,20%. Thành phần phần trăm về thể tích của O2 có trong hỗn hợp là 40%. Xác định CTHH của CHx