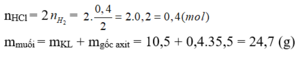cho x(g) bột sắt tác dụng với dung dịch cơ chứa 14,6g HCl sinh ra 25,4g Fecl2 và 0,4g khí H2. hãy tính x

Những câu hỏi liên quan
Cho 13g Zn tác dụng dung dịch HCL có chứa 14,6g. hãy tính thể tích khí H2 sinh ra ở đktc
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\); \(n_{HCl}=\dfrac{14,6}{36,5}=0,4\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
Xét tỉ lệ: \(\dfrac{0,2}{1}=\dfrac{0,4}{2}\) => pư vừa đủ
PTHH: Zn + 2HCl --> ZnCl2 + H2
0,2----------------->0,2
=> VH2 = 0,2.22,4 = 4,48 (l)
Đúng 5
Bình luận (0)
nZn=13/65=0,2mol
nHCl=14,6/36,5=0,4mol
Zn+2HCl→ZnCl2+H2
Xét: 0,2 < 0,4 ( mol )
0,4 0,4 ( mol )
VH2=0,4.22,4=8,96
Đúng 2
Bình luận (0)
Cho x(gam) bột sắt tác dụng với dung dịch có chứa 14,6 g hidro sinh ra 25,4g Fe2 clourua và 0,4 g H2. Hãy tính x
Hình như đề có nhầm :)
Ta có PTHH sau :
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Theo định luật bảo toàn khối lượng ta có :
\(^mFe+^mHCl=^mFECl_2+^mH_2\)
\(\Leftrightarrow x+14,6=25,4+0,4\left(g\right)\)
\(\Leftrightarrow x=11,2g\)
Vậy..
Đúng 0
Bình luận (3)
Mx+MH= MFE2+ MH2
=>Mx+M14,6=M25,4+M0,4
=>Mx+M14,6=M25,8
=>Mx=M25,8-M14,6
=>Mx=M11,2
=>x=11,2
Đúng 0
Bình luận (2)
PTHH:
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Theo định luật bảo tàn khối lượng:
\(m_{Fe}+m_{HCl}=m_{FeCl_2}+m_{H_2}\)
\(\Leftrightarrow x+14,6=25,4+0,4\)
\(\Leftrightarrow x=25,8-14,6=11,2\left(g\right)\)
Đúng 0
Bình luận (3)
Cho 8g hỗn hợp 2 kim loại Magiê và sắt tác dụng hết với dung dịch chứa 14,6g HCl a) tìm khối lượng mỗi kim loại b) Tính khối lượng mỗi muối Sinh ra và thể tích H2
a) Gọi số mol Mg, Fe là a, b (mol)
=> 24a + 56b = 8 (1)
\(n_{HCl}=\dfrac{14,6}{36,5}=0,4\left(mol\right)\)
PTHH: Mg + 2HCl --> MgCl2 + H2
a---->2a------>a------>a
Fe + 2HCl --> FeCl2 + H2
b--->2b------>b---->b
=> 2a + 2b = 0,4 (2)
(1)(2) => a = 0,1 (mol); b = 0,1 (mol)
=> \(\left\{{}\begin{matrix}m_{Mg}=0,1.24=2,4\left(g\right)\\m_{Fe}=0,1.56=5,6\left(g\right)\end{matrix}\right.\)
b)
\(\left\{{}\begin{matrix}m_{MgCl_2}=0,1.95=9,5\left(g\right)\\m_{FeCl_2}=0,1.127=12,7\left(g\right)\end{matrix}\right.\)
\(n_{H_2}=a+b=0,2\left(mol\right)\)
=> \(V_{H_2}=0,2.22,4=4,48\left(l\right)\)
Đúng 2
Bình luận (0)
cho 5,6 gam sắt (Fe) tác dụng hết với dung dịch HCl, tạo thành muối sắt (II) clorua (FeCl2) và khí hidro (H2)
a. Viết phương trình phản ứng?
b. Tính thể tích khí Hidro (H2) sinh ra ở (đktc)?
c. Tính khối lượng muối FeCl2 tạo thành ?
\(a.Fe+2HCl\rightarrow FeCl_2+H_2\\b.n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\\ n_{H_2}=n_{Fe}=0,1\left(mol\right)\\ \Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\\ c.n_{FeCl_2}=n_{Fe}=0,1\left(mol\right)\\ m_{FeCl_2}=0,1.127=12,7\left(g\right) \)
Đúng 2
Bình luận (0)
Cho 5,6 g sắt tác dụng với dung dịch axit clohidric(HCl) loãng sau phản ứng thu được sắt(II) clorua (FeCl2) và V lit khí H2. Thể tích khí hiđro sinh ra là
cần gấp giúp mình vs
\(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
0,1---------------------->0,1
=> VH2 =0,1.22,4 = 2,24(l)
Đúng 2
Bình luận (1)
\(PTHH:Fe+2HCl\rightarrow FeCl_2+H_2\\ n_{Fe}=\dfrac{m}{M}=\dfrac{5,6}{56}=0,1\left(mol\right)\\ Theo.PTHH:n_{H_2}=n_{Fe}=0,1\left(mol\right)\\ V_{H_2\left(đktc\right)}=n.22,4=0,1.22,4=2,24\left(l\right)\)
Đúng 0
Bình luận (0)
Cho 6,9 g sắt Fe tác dụng với dung dịch axit clohiđric HCl tạo ra 15,8g sắt (II) clorua FeCl2 và 0,2 g khí H2. Khối lượng HCl đã dùng?
Áp dụng định luật bảo toàn khối lượng :
'm Fe+mHCl=m FeCl2+m H2
=>m HCl=15,8+0,2-6,9=9,1g
Đúng 2
Bình luận (0)
Fe +2HCl -> FeCl2 + H2
Áp dụng định luật bảo toàn khối lượng
\(m_{Fe}+m_{HCl}=m_{FeCl_2}+m_{H_2}\\ =>m_{HCl}=15,8+0,2-6,9\\ =>m_{HCl}=9,1\left(g\right)\)
Đúng 0
Bình luận (0)
Cho 10,5g hỗn hợp bột Mg, Fe tác dụng với dung dịch HCl dư thấy có 0,4g khí H2 bay ra. Khối lượng muối thu được:
A. 17,6g
B. 25,1g
C. 24,7g
D. 17,8g
cho 5,6 (g) kim loại (Fe) tác dụng với dung dịch axit clohiđric (HCl) sinh ra 0,2 (g) khí hiđro (H2) và 205,4(g) dung dịch sắt(II) clorua (FeCl2)
a) viết phương rình hóa học chữ của phản ứng trên
b) viết phương trình hóa học của phản ứng và cho biết tỉ lệ số phân tử của các chất trong phản ứng
c) tình khối lượng dung dịch axit clohiđric đã dùng
a. sắt + axit clohydric -> sắt(II) clorua + hidro
b. \(Fe+2HCl->FeCl_2+H_2\)
\(N_{HCl}:N_{FeCl_2}:N_{H_2}=2:1:1\\ c.BTKL:m_{ddHCl}=205,4+0,2-5,6=200\left(g\right)\)
Đúng 1
Bình luận (1)
a
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,1 0,1
b
Số nguyên tử Fe: số phân tử `HCl`: số phân tử `FeCl_2`: số phân tử `H_2` là `1:2:1:1`
c
\(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\\ n_{H_2}=\dfrac{0,2}{2}=0,1\left(mol\right)\)
Do \(n_{Fe}=n_{H_2}\) nên `Fe` không dư.
\(m_{dd.FeCl_2}=m_{Fe}+m_{dd.HCl}-m_{H_2}\\ \Leftrightarrow205,4=5,6+m_{dd.HCl}-0,2\)
\(\Rightarrow m_{dd.HCl}=200\left(g\right)\)
Đúng 0
Bình luận (0)
. Cho 5,6 g sắt Fe tác dụng với dung dịch có chứa 7,3 g axit clohidric HCl tạo thành sắt (II) clorua FeCl2 và 0,2 g khí hidro. Tính khối lượng sắt (II) clorua tạo thành ?
Bảo toàn KL: \(m_{Fe}+m_{HCl}=m_{FeCl_2}+m_{H_2}\)
\(\Rightarrow m_{FeCl_2}=5,6+7,3-0,2=12,7(g)\)
Đúng 1
Bình luận (0)