cho X và Y thuộc nhóm A, biết trong hợp chất H2X, hidro chiếm 11,1% về khối lượng, biết %X trong hợp chất XaY và YXb lần lượt là 50% và 60%. tìm X, Y, XaY, Ỹb Mọi người cứu em gấp ạ, em cảm ơn nhiều
Cho X, Y là 2 phi kim, trong nguyên tử X và Y có số hạt mang điện nhiều hơn số hạt không mang điện lần lượt là 14 và 16. Biết trong hợp chất XYn, X chiếm 15,0486% về khối lượng, tổng số proton là 100, tổng số notron là 106. Xác định số khối của X, Y lần lượt là
A. 31 và 35
B. 31 và 36
C. 31 và 19
D. 14 và 35
Đáp án A
Số hạt mang điện nhiều hơn số hạt không mang điện của X là 14 → 2pX -nX = 14
Số hạt mang điện nhiều hơn số hạt không mang điện của Y là 16 → 2pY -nY = 16
Tổng số proton là 100 → pX + n.pY=100
Tổng số notron là 106→ nX + n. nY = 106
→ (2pX + 2n.pY) - (nX + n. nY ) = 200-106 = 84
→ (2pX -nX) - (2n.pY- n. nY) = 84 → 14 + 16n = 84 → n = 5

→ AX = 0,1504856. (100+106) = 31 ( P)
Số khối của của Y là 206 - 31 5 = 35
BÀI 2. Cho biết hai nguyên tố A và B thuộc nhóm A và thuộc hai chu kì liên tiếp trong bảng tuần hoàn .A ở lớp ngoài cùng có 6e. Hợp chất (X) của A với hidro trong đó %H = 11,1%(về khối lượng ).Xác định tên Avà B .
Bài 3: Hỗn hợp khí X gồm: NO2, CH4 và khí Y (là đơn chất chưa biết). Tỉ khối của X đối với hiđro là 15. Trong hỗn hợp X, CH4 chiếm 16% về khối lượng. Khí Y chiếm 50% về thể tích. Tổng số phân tử trong hỗn hợp X là 6.1023 phân tử.
a/ Tìm CTHH của khí Y. Cho biết Y là khí nào?
b/ Lượng khí Y có trong hỗn hợp trên có đủ để đốt cháy hết 6,72 lít khí CH4 (đktc) không?
a) \(n_X=\dfrac{6.10^{23}}{6.10^{23}}=1\left(mol\right)\)
=> \(n_Y=0,5\left(mol\right)\)
Gọi số mol NO2, CH4 là a, b
=> a + b = 0,5
Có: \(\dfrac{46a+16b+0,5.M_Y}{1}=15.2\)
=> 46a + 16b + 0,5.MY = 30
Có: \(\dfrac{16b}{46a+16b+0,5.M_Y}.100\%=16\%\)
=> b = 0,3 (mol)
=> a = 0,2 (mol)
=> MY = 32(g/mol)
Mà Y là đơn chất
=> Y là O2
b) \(n_{CH_4}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
Xét tỉ lệ: \(\dfrac{0,3}{1}>\dfrac{0,5}{2}\)=> CH4 dư, O2 hết
=> Lượng O2 trong hỗn hợp trên không đủ để đốt cháy 6,72 lít CH4
1. Hợp chất y chứ C và O trong đó Cacbon chiếm 27.27% theo khối lượng và PTK=44đvC. Xác định nguyên tử của Oxi trong hợp chất Z
2. Biết X chưa 2 nguyên tố C và H trong đó Cacbon chiếm 85.71% theo khối lượng và PTK cảu X như 7 phần 8 lần PTK của O2. Xác định công thứ của X và tính PTK.
3. Xác định công thức của hợp chất A có Cacbon và Hidro có tỉ lệ khối lượng Mc:Mh=4:1 và có tỉ khối đơn vị hidro là 5
CHÚC BẠN HỌC TỐT!![]()
![]()
![]()
Câu 1+3: Mình không hiểu đề cho lắm!!?
Câu 2: Gọi CTHH của X là CxHy
Theo đề bài, ta có:
+) \(PTK_X=\dfrac{7}{8}PTK_{O2}\) \(\Rightarrow PTK_X=32.\dfrac{7}{8}=28\)
+) \(\%C=85,71\%\Rightarrow\%H=14,29\%\)
\(\Rightarrow\left\{{}\begin{matrix}\%C=\dfrac{12x}{28}.100\%=85,71\%\\\%H=\dfrac{y.1}{28}.100\%=14,29\%\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}x=2\\y=4\end{matrix}\right.\)
Vậy CTHH của X là C2H4
X và Y là các nguyên tố thuộc phân nhóm chính, đều tạo hợp chất với hiđro có dạng RH (R là kí hiệu của nguyên tố X hoặc Y). Gọi A và B lần lượt là hiđroxit ứng với hóa trị cao nhất của X và Y. Trong B, Y chiếm 35,323% khối lượng. Trung hòa hoàn toàn 50 gam dung dịch A 16,8% cần 150 ml dung dịch B 1M. Xác định các nguyên tố X và Y.
Vì hợp chất với hidro có dạng RH => X hoặc Y thuộc nhóm IA hoặc VIIA
*TH1: Y thuộc nhóm IA => CT hidroxit : YOH
theo đề ta có: Y/(Y+17)=0.35323
=>Y=9.28 (loại)
*TH2: Y thuộc nhóm VIIA=> CT hidroxit: HYO4
theo đề ta có: Y/(1+Y+16.4)=0.35323
=> Y=35.5 Cl
theo đề ta thấy: trung hòa A cần dùng dung dịch B. Mà B là axit => A là bazo
=> X thuộc nhóm IA => CTHH: XOH
PT: XOH + HClO4 -> XClO4 +H2O
0.15 0.15 (MOL)
m(XOH)=(50.16,8)/100=8,4=>M(XOH)=m/n=56=>X=39 (Kali)
Hợp chất với hiđro có dạng RH nên Y có thể thuộc nhóm IA hoặc VIIA.
Trường hợp 1 : Nếu Y thuộc nhóm IA thì B có dạng YOH
Ta có : \(\frac{Y}{17}=\frac{35,323}{64,677}\Rightarrow\)\(Y=9,284\) (loại do không có nghiệm thích hợp)
Trường hợp 2 : Y thuộc nhóm VIIA thì B có dạng HYO4
Ta có : \(\frac{Y}{65}=\frac{35,323}{64,377}\Rightarrow Y=35,5\), vậy Y là nguyên tố clo (Cl).
B (HClO4) là một axit, nên A là một bazơ dạng XOH
\(m_A=\frac{16,8}{100}.50g=8,4g\)
XOH + HClO4 \(\rightarrow\) XClO4 + H2O
\(\Rightarrow n_A=n_{HClO_4}=0,15L.0,1\text{/}L=0,15mol\)
\(\Rightarrow M_X+17g\text{/}mol=\frac{0,84g}{0,15mol}\)
\(\Rightarrow\) MX = 39 gam/mol, vậy X là nguyên tố kali (K).
cho nguyên tố R thuộc nhóm VIIA trong bảng tuần hoàn. Trong hợp chất khí với Hidro rồi chiếm a% về khối lượng. Trong công thức oxi cao nhất rồi chiếm b% về khối lượng Biết rằng a%+b%=18176/13359 x 100% Hãy xác định nguyên tố r
Hợp chất của R và hidro: RH
\(\Rightarrow a\%=\dfrac{M_R}{M_R+1}.100\%\)
Hợp chất oxit cao nhất của R: R2O7
\(\Rightarrow b\%=\dfrac{2M_R}{2M_R+112}.100\%\)
\(\Rightarrow\dfrac{M_R}{M_R+1}+\dfrac{2M_R}{2M_R+112}=\dfrac{18176}{13359}\)
\(\Rightarrow M_R=35,5\left(g/mol\right)\)
→ R là Cl.
Cho 2 nguyên tố X và Y thuộc hai chu kì liên tiếp ( Z X < Z Y ) và cùng số thứ tự của nhóm trong bảng tuần hoàn (nhóm A và nhóm B).
- Nguyên tố X tạo thành hợp chất ion với clo ứng với công thức XC1.
- Nguyên tố Y cũng tạo thành hợp chất với clo hợp chất YC1 trong đó khối lượng của clo chiếm 24,7%.
Xác định các nguyên tố X và Y.
X tạo bởi chất ion với clo có công thức là XC1, vậy X là kim loại có hoá trị I.
Y cùng số nhóm với X vậy cũng có hoá trị I, công thức clorua của nó là YC1.
Ta có:
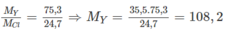
( M Y và M Cl lần lượt là NTK của nguyên tố Y và nguyên tố clo). Đó là Ag. Nguyên tố X cùng chu kì, cùng số thứ tự nhóm với Ag là kali (K))
\(\%O=\dfrac{16a}{32+16a}\cdot100\%=50\%\)
\(\Rightarrow a=2\)
\(Y:SO_2\)
\(M_X=M_{SO_2}\cdot0.53125=64\cdot0.53125=34\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow A+n=34\)
\(BL:n=2\Rightarrow A=32\)
\(X:H_2S\)