dẫn 6,72 lit hỗn hợp etilen và but-1-en vào bình đựng dung dịch Brom thấy khối lượng bình tăng 11,2(g). tính phần trăm thể tích mỗi khí trong hỗn hợp đầu

Những câu hỏi liên quan
dẫn 4 gam hỗn hợp 2 khí metan và etilen qua bình đựng dung dịch brom dư, thấy khối lượng bình đựng dung dịch brom tăng 2,8 gam thành phần phần trăm theo khối lượng mỗi khi có trong hỗn hợp đầu lần lượt là
Ta có: mC2H4 = m bình tăng = 2,8 (g)
\(\left\{{}\begin{matrix}\%m_{C_2H_4}=\dfrac{2,8}{4}.100\%=70\%\\\%m_{CH_4}=30\%\text{ }\end{matrix}\right.\)
Bạn tham khảo nhé!
Đúng 2
Bình luận (0)
Dẫn 6,72 lit hỗn hợp khí X gồm propan, etilen và axetilen đi qua dung dịch brom dư, thấy còn 1,68 lít khí không hấp thụ. Nếu dẫn 6,72 lit hỗn hợp khí X trên qua dung dịch AgNO3/NH3 thấy có 24,24 gam kết tủa. Các thể tích khí đo ở đktc. Tính thành phần phần trăm theo thể tích và theo khối lượng của mỗi khí trong hỗn hợp.
1,68 lit khí không bị dung dịch Br2 hấp thụ là propan
![]()
![]()
![]()
![]()
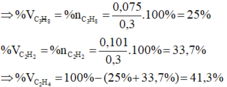
![]()
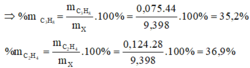
![]()
Đúng 1
Bình luận (0)
Dẫn từ từ 4,48 lít hỗn hợp khí etilen và propilen (đktc) vào dung dịch brom dư thấy khối lượng bình brom tăng 7,7 gam. Tính % thể tích của mỗi khí trong hỗn hợp ban đầu.
\(Đặt:n_{C_2H_4}=a\left(mol\right);n_{C_3H_6}=b\left(mol\right)\left(a,b>0\right)\\ C_2H_4+Br_2\rightarrow C_2H_4Br_2\\ C_3H_6+Br_2\rightarrow C_3H_6Br_2\\ m_{tăng}=m_{hh.ban.đầu}=7,7\left(g\right)\\ \Rightarrow Hpt:\left\{{}\begin{matrix}28a+42b=7,7\\a+b=0,2\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,05\\b=0,15\end{matrix}\right.\)
Vì thể tích tỉ lệ thuận với số mol nên ta có:
\(\%V_{C_2H_4\left(đktc\right)}=\%n_{C_2H_4}=\dfrac{a}{a+b}.100\%=\dfrac{0,05}{0,2}.100=25\%\\ \Rightarrow\%V_{C_3H_6}=100\%-25\%=75\%\)
Đúng 6
Bình luận (0)
dẫn hỗn hợp ( X) gồm 6,72 lít ( đktc) khí etilen và metan đi qua bình đựng dung dịch Brom thấy khối lượng bình tăng lên 5,6 gam . Tính thể tích mỗi chất khí có trong hỗn hợp ( X)
( cho nguyên tử khối Br= 80, H= 1, C=12, O=16)
giải giúp mình với
mtăng = mC2H4
=> \(n_{C_2H_4}=\dfrac{5,6}{28}=0,2\left(mol\right)\)
=> VC2H4 = 0,2.22,4 = 4,48 (l)
=> VCH4 = 6,72 - 4,48 = 2,24 (l)
Đúng 3
Bình luận (0)
Dẫn 11,2 lít hỗn hợp khí CH4 và C2H4 ở đktc qua 250 gam dung dịch brom, sau phản ứng thấy khối lượng bình brôm tăng 5,6 gam.Tính thành phần trăm theo thể tích và khối lượng của mỗi khí trong hỗn hợp đầu.b- Tính nồng độ phần trăm của dung dịch brom ban đầu. c- Nếu đốt cháy lượng C2H4 trên, rồi dẫn khí thu được vào 200ml dd NaOH 2M, thì muối nào được tạo thành? Tìm CM của muối.
Cho 11 lit hỗn hợp khí gồm metan và etylen ở đktc đi qua bình đựng 250ml dung dịch brom 1,5M, nhận thấy dung dịch brom mất màu. Tính thể tích và phần trăm thể tích mỗi khí trong hỗn hợp ban đầu. Tính khối lượng chât tan có trong dung dịch sau phản ứng.
Cho hỗn hợp qua dung dịch brom chỉ có etylen tác dụng.
\(n_{Br_2}=0,25\cdot1,5=0,375mol\)
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
0,375 0,375
\(V_{C_2H_4}=0,375\cdot22,4=8,4l\Rightarrow V_{CH_4}=11-8,4=2,6l\)
Đúng 2
Bình luận (0)
Bài 2 : Cho 11 lit hỗn hợp khi gồm metan và etylen ở đkte đi qua bình đựng 250ml dung dịch brom 1,5M , nhận thấy dung dịch brom mất màu . Tính thể tích và phần trăm thể tích mỗi khí trong hỗn hợp ban đầu . Tính khối lượng chất tan có trong dung dịch sau phản ứng .
dẫn 11,2 lít (đktc) hỗn hợp khí gồm etilen và metan qua bình đựng dung dịch Brom dư thu được 47 gam C2H4Br2
a) Tính khối lượng BROM ĐÃ PHẢN ỨNG
b) tính % thể tích mỗi khí trong hỗn hợp
a) nC2H4Br2=47/188=0,25(mol)
n(CH4,C2H4)=11,2/22,4=0,5(mol)
PTHH: C2H4 + Br2 -> C2H4Br2
0,25<----------0,25<---------0,25(mol)
mBr2(p.ứ)=0,25 x 160= 40(g)
b) V(C2H4,đktc)=0,25 x 22,4= 5,6(l)
=> %V(C2H4)=(5,6/11,2).100=50%
=>%V(CH4)=100% - 50%= 50%
Đúng 0
Bình luận (0)
Dẫn 4,48 lít hỗn hợp gồm metan etilen (dktc) vào dung dịch br2 thì thấy khối lượng bình đựng br2 tăng 2,8 g. Tính thể tích mỗi khí trong hỗn hợp
mtăng = mC2H4 = 2,8 (g)
=> \(n_{C_2H_4}=\dfrac{2,8}{28}=0,1\left(mol\right)\)
=> VC2H4 = 0,1.22,4 = 2,24 (l)
=> VCH4 = 4,48 - 2,24 = 2,24 (l)
Đúng 2
Bình luận (0)
C2H4+Br2-to>C2H4Br2
0,01---0,01 mol
n C2H4=\(\dfrac{2,8}{28}\)=0,1 mol
=>VC2H4=0,01.22,4=2,24l
=>VCH4=2,24
Đúng 1
Bình luận (0)




















