Một hợp chất Y với Cl biết Y hóa trị (III), trong đó clo chiếm 66,54% theo khối lượng.
xác định tên nguyên tố Y.
Một số hợp chất của nguyên tố T hóa trị III với nguyên tố oxi, trong đó T chiếm 53% về khối lượng. Xác định nguyên tử khối và tên nguyên tố T.
Gọi công thức của hợp chất là T 2 O 3 và a là nguyên tử khối của T.
Theo đề bài, ta có tỉ lệ phần trăm khối lượng của T:
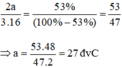
Nguyên tố T là nhôm.
Bài 1:Một hợp chất của nguyên tố M hóa trị III với nguyên tố oxi. Biết M chiếm 53% về khối lượng trong hợp chất.
a) Xác định nguyên tử khối và cho biết tên, kí hiệu hóa học của nguyên tố M.
b) Viết công thức hóa học, tính phân tử khối của hợp chất.
Câu 2. Phân loại và gọi tên các chất sau: Fe2(SO4)3, Na2HPO4, Ba (HCO3)2, N2O5, KMnO4, KClO3, H2CO3.
Câu 3. Tính số mol nguyên tử hoặc phân tử trong các lượng chất sau:
a) 1,44.1023 phân tử HCl b) 24.1023 nguyên tử Na
*Gấp ạ, mai em nạp rồi, ai làm hộ em với
một hợp chất của nguyên tố X hóa trị III với nguyên tố oxi trong đó X chiếm 52,94% về khối lượng . Xác định công thức hóa học và tính phân tử khối của hợp chất
Một hợp chất của nguyên tố R ( R chưa biết hóa trị ). Trong đó oxi chiếm 27.58621% về khối lượng . Xác định tên nguyên tố R
. Một nguyên tử Y kết hợp với 4 nguyên tử H tạo thành hợp chất với hiđro. Trong phân tử, hiđro chiếm 25% về khối lượng. Xác định tên của nguyên tố Y và công thức hóa học của hợp chất?
Hợp chất của nguyên tố R hóa trị (III) với nguyên tố oxi, trong đó nguyên tố oxi chiếm 30% theo khối lượng. Xác định nguyên tố R.
( Biết: C=12; H=1; S=32; Ca=40; Fe=56; O=16; P=31; Al=27; Hg= 201 )
Câu 49: Một hợp chất của nguyên tố Z có hóa trị V với nguyên tố oxi, trong đó oxi chiếm 56,34% về khối lượng
a/ Xác định nguyên tử khối và tên nguyên tố Z.
b/ Viết công thức hóa học và tính PTK của hợp chất.
Gọi CTHH là Z2O5
% O = 16.5 / ( MZ.2+16.5)= 56,34%
<=> MZ ∼ 31 đvc
=> Z là photpho (P)
=> CTHH là P2O5
M P2O5 = 31.2+16.5=142 đvc
Một hợp chất của ng tố R (hóa trị ll) với nguyên tố clo, trong h/c này nguyên tố R chiếm 25,26% về khối lượng.
Xác định ng tố R và viết CTHH của hợp chất .
\(CT:RCl_2\)
\(\%R=\dfrac{R}{R+71}\cdot100\%=25.26\%\)
\(\Rightarrow R=24\)
\(R:Mg\)
\(CTHH:MgCl_2\)
Cho 2 nguyên tố X và Y thuộc hai chu kì liên tiếp ( Z X < Z Y ) và cùng số thứ tự của nhóm trong bảng tuần hoàn (nhóm A và nhóm B).
- Nguyên tố X tạo thành hợp chất ion với clo ứng với công thức XC1.
- Nguyên tố Y cũng tạo thành hợp chất với clo hợp chất YC1 trong đó khối lượng của clo chiếm 24,7%.
Xác định các nguyên tố X và Y.
X tạo bởi chất ion với clo có công thức là XC1, vậy X là kim loại có hoá trị I.
Y cùng số nhóm với X vậy cũng có hoá trị I, công thức clorua của nó là YC1.
Ta có:
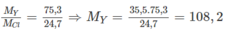
( M Y và M Cl lần lượt là NTK của nguyên tố Y và nguyên tố clo). Đó là Ag. Nguyên tố X cùng chu kì, cùng số thứ tự nhóm với Ag là kali (K))