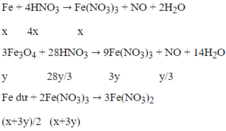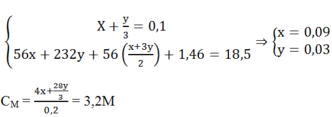Những câu hỏi liên quan
Cho 2,24g bột sắt vào 100ml dung dịch hỗn hợp gồm AgNO3 0,1M và Cu(NO3)2 0,5M khuấy đều cho tới khi phản ứng xảy ra hoàn toàn thu được chất rắn A và dung dịch B. Chất rắn A có khối lượng là:
A. 3,32g
B. 4,4g
C. 4,08g
D. 5,4g
Đáp án C
Phản ứng xảy ra theo thứ tự:
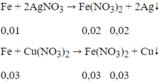
⇒ Fe tan hết
m = 0,02.108 + 0,03.64 = 4,08 (g)
Đúng 0
Bình luận (0)
Cho 2,24g bột sắt vào 100ml dung dịch hỗn hợp gồm AgNO3 0,1M và Cu(NO3)2 0,5M khuấy đều cho tới khi phản ứng xảy ra hoàn toàn thu được chất rắn A và dung dịch B. Chất rắn A có khối lượng là:
A. 3,32g
B. 4,4g
C. 4,08g
D. 5,4g
Đáp án C
Phản ứng xảy ra theo thứ tự:
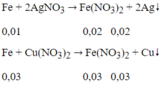
⇒ Fe tan hết
m = 0,02.108 + 0,03.64 = 4,08 (g)
Đúng 0
Bình luận (0)
Cho 22 gam hỗn hợp X gồm Al và Fe phản ứng với dung dịch chứa 0,6 mol HCl . Chứng minh hỗn hợp X tan hết.Nguời ta tiến hành 2 thí nghiệm sau:TN1: Cho 2,02 gam hỗn hợp Mg, Zn vào cốc đựng 200ml dung dịch HCl . Sau phản ứng đun nóng cho nước bay hơi hết thu được 4,86 gam chất rắn.TN2: Cho 2,02 gam hỗn hợp trên vào cốc đựng 400ml dung dịch HCl trên. Sau khi cô cạn thu được 5,57 gam chất rắn.Chứng minh trong TN1 axit hết, TN2 axit dư.Tính thể tích khí...
Đọc tiếp
Cho 22 gam hỗn hợp X gồm Al và Fe phản ứng với dung dịch chứa 0,6 mol HCl . Chứng minh hỗn hợp X tan hết.
Nguời ta tiến hành 2 thí nghiệm sau:
TN1: Cho 2,02 gam hỗn hợp Mg, Zn vào cốc đựng 200ml dung dịch HCl . Sau phản ứng đun nóng cho nước bay hơi hết thu được 4,86 gam chất rắn.
TN2: Cho 2,02 gam hỗn hợp trên vào cốc đựng 400ml dung dịch HCl trên. Sau khi cô cạn thu được 5,57 gam chất rắn.
Chứng minh trong TN1 axit hết, TN2 axit dư.
Tính thể tích khí bay ra ở TN1.
Tính số mol HCl tham gia phản ứng.
Tính số gam mõi kim loại
Hỗn hợp A gồm các kim loại Mg, Al, Fe.Lấy 14,7 gam hỗn hợp A cho tác dụng với dung dịch NaOH dư, sinh ra 3,36 lít khí (đktc). Mặt khác cũng lấy 14,7 gam hỗn hợp A cho tác dụng với dung dịch HCl dư, sinh ra 10,08 lít khí (đktc) và dung dịch B. Cho dung dịch B tác dụng với dung dịch NaOH dư, lọc kết tủa tạo thành và nung nóng trong không khí đến khối lượng không đổi thu được m gam chất rắn. Tính m và tính % theo khối lượng của mỗi kim loại tron...
Đọc tiếp
Hỗn hợp A gồm các kim loại Mg, Al, Fe.
Lấy 14,7 gam hỗn hợp A cho tác dụng với dung dịch NaOH dư, sinh ra 3,36 lít khí (đktc). Mặt khác cũng lấy 14,7 gam hỗn hợp A cho tác dụng với dung dịch HCl dư, sinh ra 10,08 lít khí (đktc) và dung dịch B. Cho dung dịch B tác dụng với dung dịch NaOH dư, lọc kết tủa tạo thành và nung nóng trong không khí đến khối lượng không đổi thu được m gam chất rắn. Tính m và tính % theo khối lượng của mỗi kim loại trong hỗn hợp A.Cho hỗn hợp A tác dụng với dung dịch CuSO4 dư, sau khi phản ứng kết thúc, lọc lấy chất rắn đem hòa tan hết chất rắn trong dung dịch HNO3 loãng dư, thu được 26,88 lít khí NO (đktc). Tính khối lượng hỗn hợp A.1.1. Al + NaOH + H2O ==> NaAlO2 + 3/2H2
nH2(1)=3,36/22,4=0.15(mol)
=> nAl(1)= nH2(1):3/2= 0.15:3/2= 0.1(mol)
2.Mg + 2HCl ==> MgCl2 + H2
3.2Al + 6HCl ==> 2AlCl3 + 3H2
4.Fe + 2HCl ==> FeCl2 + H2
=> \(n_{H_2\left(2,3,4\right)}=\) 10.08/22.4= 0.45(mol)
=> nH2(3)=0.1*3/2=0.15(mol)
MgCl2 + 2NaOH ==> Mg(OH)2 + 2NaCl
AlCl3 + 3NaOH ==> Al(OH)3 + 3NaCl
FeCl2 + 2NaOH ==> Fe(OH)2 + 2NaCl
Đúng 0
Bình luận (0)
Cho 18,5 gam hỗn hợp X gồm Fe và Fe3O4 tác dụng với 200ml dung dịch HNO3 loãng, đun nóng và khuấy đều. Sau khi phản ứng xảy ra hoàn toàn thu được 2,24 lít khí NO duy nhất (đktc), dung dịch Y và 1,46 gam kim loại. Nồng độ mol của dung dịch HNO3 là: A. 2M B. 2,4M C. 2,5M D. 3,2M
Đọc tiếp
Cho 18,5 gam hỗn hợp X gồm Fe và Fe3O4 tác dụng với 200ml dung dịch HNO3 loãng, đun nóng và khuấy đều. Sau khi phản ứng xảy ra hoàn toàn thu được 2,24 lít khí NO duy nhất (đktc), dung dịch Y và 1,46 gam kim loại. Nồng độ mol của dung dịch HNO3 là:
A. 2M
B. 2,4M
C. 2,5M
D. 3,2M
Nung 12,64 gam hỗn hợp FeCO3 và FexOy trong không khí tới khi phản ứng xảy ra hoàn toàn thu được sản phẩm khí A và 11,2 gam chất rắn. Cho khí A hấp thụ hết vào 200ml dung dịch Ba(OH)2 0,15M thấy có 3,94 gam kết tủa tạo thành.
a) Viết các phương trình hóa học xảy ra.
b) Tìm công thức phân tử FexOy.
a)
4FeCO3 + O2 --> 2Fe2O3 + 4CO2 (1)
4FexOy + (3x-2y)O2 --> 2xFe2O3 (2)
CO2 + Ba(OH)2 → BaCO3 + H2O (3)
2CO2 + Ba(OH)2 → Ba(HCO3)2 (4)
b)
Giả sử Ba(OH)2 dư , chỉ xảy ra (3) không xảy ra pư (4)
nBaCO3 = 0,02 mol = nCO2
=> nFe2O3 (1) = 0,01 mol
Mà \(\Sigma\)nFe2O3 (1) + (2) = \(\dfrac{11,2}{160}\)= 0,07 mol => nFe2O3 (2) = 0,07 -0,01 = 0,06 mol
=> nFexOy = \(\dfrac{0,12}{x}\) mol
mFexOy = 12,64 - mFeCO3 = 12,64 - 0,02.116 = 10,32 gam
=> M FexOy = 86x (g/mol)
Với x = 1,2,3 ... đều không thỏa mãn
=> Ba(OH)2 phản ứng hết, xảy ra cả phản ứng (3) và (4)
nBa(OH)2 = 0,03 mol , nBaCO3 = 0,02 mol
=> nBa(OH)2 (4) = 0,03 - 0,02 = 0,01 mol
=> nCO2 (4) = 0,01.2 = 0,02 mol
=> nCO2 (1) = nCO2 (3) + nCO2 (4) = 0,04 mol
<=> nFe2O3 (1) = 0,02 mol , nFeCO3 = 0,04 mol
=> nFe2O3 (2) = 0,07 - 0,02 = 0,05 mol <=> n FexOy = \(\dfrac{0,1}{x}\) mol
mFexOy = 12,64 - mFeCO3 = 12,64 - 0,04.116 = 8 gam
=> M FexOy = 80x (g/mol)
với x = 2 => mFexOy = 160 (g/mol) <=> Fe2O3
Đúng 1
Bình luận (1)
Cho Zn tới dư vào dung dịch gồm HCl; 0,05 mol NaNO3 và 0,1 mol KNO3. Sau khi kết thúc các phản ứng thu được dung dịch X chứa m gam muối; 0,125 mol hỗn hợp khí Y gồm hai khí không màu, trong đó có một khí hóa nâu ngoài không khí. Tỉ khối của Y so với H2 là 12,2. Giá trị của m gần nhất với: A. 64 gam B. 65 gam C. 70 gam D. 75 gam
Đọc tiếp
Cho Zn tới dư vào dung dịch gồm HCl; 0,05 mol NaNO3 và 0,1 mol KNO3. Sau khi kết thúc các phản ứng thu được dung dịch X chứa m gam muối; 0,125 mol hỗn hợp khí Y gồm hai khí không màu, trong đó có một khí hóa nâu ngoài không khí. Tỉ khối của Y so với H2 là 12,2. Giá trị của m gần nhất với:
A. 64 gam
B. 65 gam
C. 70 gam
D. 75 gam
MY= 24,4 → Y chứa H2. Khí không màu hóa nâu ngoài không khí là NO → Y chứa NO và H2.
Gọi x và y lần lượt là số mol của H2 và NO
Ta có: x+ y= 0,125; 2x+ 30y= 0,125.24,4 → x= 0,025; y= 0,1
Vì có khí H2 thoát ra và Zn dư → H+ và NO3- hết → Muối thu được là muối clorua
Do nNO3(-)ban đầu= 0,15 mol > nNO= 0,1 mol→ X chứa NH4+
Theo bảo toàn nguyên tố N → nNH4+= 0,15-0,1= 0,05 mol
Theo bảo toàn electron: 2.nZn pứ= 3.nNO+ 8nNH4++ 2nH2= 0,75 mol→ nZn pứ= nZn2+= 0,375 mol
→mmuối= mZnCl2+ mNH4Cl+ mNaCl+ mKCl= 136. 0,375+ 53,5.0,05+ 58,5.0,05+ 74,5.0,1= 64,05 gam
Đáp án A
Đúng 0
Bình luận (0)
Hoà tan hỗn hợp gồm : K2O, BaO, Al2O3, Fe3O4 vào nước (dư), thu được dung dịch X và chất rắn Y. Sục khí CO2 đến dư vào dung dịch X, sau khi các phản ứng xảy ra hoàn toàn thu được kết tủa là : A. Al(OH)3. B. Fe(OH)3. C. BaCO3 D. K2CO3.
Đọc tiếp
Hoà tan hỗn hợp gồm : K2O, BaO, Al2O3, Fe3O4 vào nước (dư), thu được dung dịch X và chất rắn Y. Sục khí CO2 đến dư vào dung dịch X, sau khi các phản ứng xảy ra hoàn toàn thu được kết tủa là :
A. Al(OH)3.
B. Fe(OH)3.
C. BaCO3
D. K2CO3.
Đáp án A
Sơ đồ phản ứng :
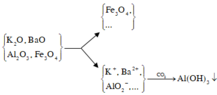
Chất rắn Y có Fe3O4 và có thể còn Al2O3 chưa phản ứng hết. Dung dịch X có có Ba2+, K+, AlO 2 - và có thể có OH - . Sục CO2 dư vào X chỉ thu được kết tủa là Al(OH)3.
Phương trình phản ứng :
![]()
Giả sử trong Y có OH - thì do CO2 có dư nên xảy ra phản ứng :
![]()
Do đó không thể có kết tủa BaCO3.
Đúng 0
Bình luận (0)
Hoà tan hỗn hợp gồm : K2O, BaO, Al2O3, Fe3O4 vào nước (dư), thu được dung dịch X và chất rắn Y. Sục khí CO2 đến dư vào dung dịch X, sau khi các phản ứng xảy ra hoàn toàn thu được kết tủa là : A. Al(OH)3. B. Fe(OH)3 C. BaCO3 D. K2CO3.
Đọc tiếp
Hoà tan hỗn hợp gồm : K2O, BaO, Al2O3, Fe3O4 vào nước (dư), thu được dung dịch X và chất rắn Y. Sục khí CO2 đến dư vào dung dịch X, sau khi các phản ứng xảy ra hoàn toàn thu được kết tủa là :
A. Al(OH)3.
B. Fe(OH)3
C. BaCO3
D. K2CO3.
Chọn A
Chất rắn Y có Fe3O4 và có thể còn Al2O3 chưa phản ứng hết. Dung dịch X có có Ba2+, K+, A l O 2 - và có thể có O H - . Sục CO2 dư vào X chỉ thu được kết tủa là Al(OH)3.
Đúng 0
Bình luận (0)