tính nồng độ mol của các chất trog dung dịch thu đc sau phản ứng:cho 2,24l khí CO2 vào 50ml dung dịch KOH 1,2 M

Những câu hỏi liên quan
Cho 18.5 gam hỗn hợp X gồm Fe, Zn, Cu vào dung dịch H2SO4 loãng dư thu được 4,48 lit khí (dktc). Nếu cũng cho lượng hỗn hợp X trên vào H2SO4 đặc nóng, eư thì thu được 7,84 lit khí SO2 (dktc)a) Tính thành phần trăm theo khối lượng của các kim loại trong hỗn hợp đầub) Dẫn lượng khí So2 thu được đi qua 200ml dd KOH 1M. Tính khối lượng và nồng độ mol các chất trong dd sau phản ứng
Đọc tiếp
Cho 18.5 gam hỗn hợp X gồm Fe, Zn, Cu vào dung dịch H2SO4 loãng dư thu được 4,48 lit khí (dktc). Nếu cũng cho lượng hỗn hợp X trên vào H2SO4 đặc nóng, eư thì thu được 7,84 lit khí SO2 (dktc)
a) Tính thành phần trăm theo khối lượng của các kim loại trong hỗn hợp đầu
b) Dẫn lượng khí So2 thu được đi qua 200ml dd KOH 1M. Tính khối lượng và nồng độ mol các chất trong dd sau phản ứng
Cho 13 gam Zn vào 340 g dung dịch AgNO3 15%.a. Tính khối lượng kim loại thu được khi phản ứng kết thúc ? Tính khối lượng muối tạo thành ?b. Tính nồng độ C% của các chất trong dung dịch sau phản ứng.
Đọc tiếp
Cho 13 gam Zn vào 340 g dung dịch AgNO3 15%.
a. Tính khối lượng kim loại thu được khi phản ứng kết thúc ? Tính khối lượng muối tạo thành ?
b. Tính nồng độ C% của các chất trong dung dịch sau phản ứng.
Cho 200 gam dung dịch NaOH tác dụng với 490 gam dung dịch H2SO4 2% thu được dung dịch A, sau khi phản ứng kết thúc cần dùng 5,6 gam KOH để trung hòa hết lượng axít dư có trong A. Tính nồng độ của dung dịch NaOH đã dùng và nồng độ của các chất có trong dung dịch A
hòa tan hoàn toàn 13,2(g) hỗn hợp hai bột ZnO và Al2O3 vào 250 (ml) dung dịch HCl 2M (vừa đủ)
a) tính thành phần % theo khối lượng mỗi chất trong hỗn hợp
b) tính nồng độ mol của các muối trong dung dịch sau phản ứng (thể tích dung dịch thay đổi không đáng kể)
cho 5.4 gam Nhôm tác dụng vừa đủ với 200gam dung dịch HCl
a) tính thể tích khí H2 sinh ra (đktc)
b) Tính nồng độ phần trăm của dung dịch HCl đã dùng
c) tính nồng độ phần trăm của dung dịch thu được sau phản ứng
Theo gt ta có: $n_{Al}=0,2(mol)$
$2Al+6HCl\rightarrow 2AlCl_3+3H_2$
a, Ta có: $n_{H_2}=0,3(mol)\Rightarrow V_{H_2}=6,72(l)$
b, Ta có: $n_{HCl}=0,6(mol)\Rightarrow \%C_{HCl}=10,95\%$
c, Sau phản ứng dung dịch chứa 0,2 mol AlCl3
Suy ra $\%C_{AlCl_3}=13,03\%$
Đúng 1
Bình luận (0)
Trộn 200ml dung dịch naoh 1m tác dụng với 100ml dung dịch hcl 1m. Bỏ qua sự thay đổi thể tích khi trộn lẫn.
a. Hỏi dung dịch thu được sau phản ứng có môi trường axit hay bazơ.
b. Tính nồng độ mol của các chất trong dung dịch thu được sau phản ứng
PTHH: \(NaOH+HCl\rightarrow NaCl+H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{NaOH}=0,2\cdot1=0,2\left(mol\right)\\n_{HCl}=0,1\cdot1=0,1\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) NaOH còn dư
\(\Rightarrow\) Dung dịch sau p/ứ có môi trường bazơ
\(\Rightarrow n_{NaCl}=0,1\left(mol\right)=n_{NaOH\left(dư\right)}\) \(\Rightarrow C_{M_{NaCl}}=\dfrac{0,1}{0,2+0,1}\approx0,33\left(M\right)=C_{M_{NaOH\left(dư\right)}}\)
Đúng 1
Bình luận (0)
Sục khí Clo tới dư vào dung dịch chứa 0,4 mol H2S. Sau phản ứng thu được dung dịch A
a) Viết và cân bằng phản ứng bằng phương pháp cân bằng e. Xác định vai trò các chất tham gia phản ứng
b) Tính thể tích dung dịch NaOH 1 M cần trung hòa hết A
c) Cho 0,3 mol BaCl2 vào A. Tính khối lượng các chất thu được
hoà tan 1,2g Magiê bằng 50 mol dung dịch HCl 3M
a, Viết phuong trình phản úng
b, Tính thể tích khí thoát ra
c, Tính nồng độ mol/l của dung dịch thu đc̣ sau phản úng( coi thể tívh dung dịch sau phản úng ko đáng kể)
Hấp thụ hoàn toàn 3,36 lít CO2 (đktc) vào 125 ml dung dịch Ba(OH)2 1M, thu được dung dịch X. Coi thể tích dung dịch không thay đổi, nồng độ mol của chất tan trong dung dịch X là:
A. 0,4M
B. 0,2M
C. 0,6M
D. 0,1M
Đáp án B
Ta có: nCO2= 0,15 mol; nBa(OH)2= 0,125 mol; nOH-= 0,25 mol
Ta thấy 1 < n OH - n CO 2 = 0 , 25 1 , 5 = 1,67 < 2 à tạo ra 2 muối.
PTPỨ:
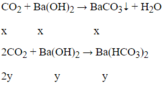
Ta có hệ
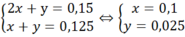
![]()
Đúng 0
Bình luận (0)















