Hòa tan 7g hỗn hợp gồm Al, Fe và Cu trong dung dịch H2SO4 loãng, dư. Phản ứng kết thúc thấy trong bình phản ứng còn lại 1,5g chất rắn và thu được 4,48 lit khí(đktc). Tính % mỗi kim loại trong hỗn hợp ban đầu
GIÚP MÌNH VỚI
Hòa tan 7g hỗn hợp gồm Al, Fe và Cu trong dung dịch H2SO4 loãng, dư. Phản ứng kết thúc thấy trong bình phản ứng còn lại 1,5g chất rắn và thu được 4,48 lit khí(đktc). Tính % mỗi kim loại trong hỗn hợp ban đầu
GIÚP MÌNH VỚI
2Al + 3H2SO4 --> Al2(SO4)3 + 3H2 (1)
Fe +H2SO4 --> FeSO4 + H2 (2)
Gọi nAl=x(mol)
nFe=y(mol)
nH2=0,2(mol)
Phản ứng kết thúc thấy trong bình phản ứng còn lại 1,5g chất rắn => mCu=1,5(g)
=> mAl,Fe=5,5(g)
=>\(\left\{{}\begin{matrix}27x+56y=5,5\\1,5x+y=0,2\end{matrix}\right.=>\left\{{}\begin{matrix}x=0,1\left(mol\right)\\y=0,05\left(mol\right)\end{matrix}\right.\)
=>mAl=2,7(g)
mFe=2,8(g)
=> %mAl=38,57(%)
%mFe=40(%)
%mCu=21,43(%)
Hòa tan 7g hỗn hợp gồm Al, Fe và Cu trong dung dịch H2SO4 loãng, dư. Phản ứng kết thúc thấy trong bình phản ứng còn lại 1,5g chất rắn và thu được 4,48 lit khí(đktc). Tính % mỗi kim loại trong hỗn hợp ban đầu
CÁC BÁC GIÚP EM VỚI. EM CAM ON NHIỀU Ạ
Mình làm mình tính toán thấy sai sai nên mình nói cách giải nhé.
Đấu tiên bạn phải tính số mol của khí thoát ra là H2.Sau đó sẽ lần lượt gọi 1 cái tên nào đó ví dụ như x,y là số mol của Al và Fe
Viết PTHH để biểu diễn ra.Sẽ có tiếp hệ phương trình ra số mol của x và y hay số mol của Al và Fe.
Tiếp theo , chỉ cần tính khối lượng của Al và Fe thôi vì khối lượng của Cu có rồi đó là 1,5g .
Có tất cả khối lượng rồi bạn tính phần trăm mỗi kim loại như bình thường thôi.
Đốt cháy hỗn hợp gồm 0,10 mol Mg và 0,16 mol Fe trong 4,48 lít (đktc) hỗn hợp khí gồm Cl2 và O2, thu được 20,88 gam hỗn hợp rắn X gồm các muối và oxit của kim loại (không thấy khí thoát ra). Hòa tan X trong dung dịch HCl loãng, thu được dung dịch Y chỉ chứa các muối. Cho dung dịch AgNO3 dư vào Y, kết thúc phản ứng thu được Y, kết thúc phản ứng thu được m gam kết tủa. Giá trị của m là:
A. 98,32.
B. 96,16.
C. 91,84.
D. 94,00.
Cho 16,6 gam hỗn hợp X gồm Al, Fe (số mol của Al và Fe bằng nhau) vào 200 ml dung dịch Y gồm Cu(NO3)2 và AgNO3. Sau khi phản ứng kết thúc, thu được chất rắn Z gồm 3 kim loại. Hòa tan toàn bộ lượng chất rắn Z vào dung dịch HCl dư, thu được 2,24 lít khí (đktc) và còn lại 40,8 gam chất rắn T không tan. Nồng độ mol/lít của Cu(NO3)2 trong Y có giá trị là
A. 2,0.
B. 1,0.
C. 1,5.
D. 1,3.
Chọn C.
Hỗn hợp X gồm Al và Fe với số mol mỗi chất bằng 0,2 mol
Hỗn hợp Y gồm Cu(NO3)2 (0,2x mol) và AgNO3 (0,2y mol)
Hỗn hợp Z gồm Ag, Cu và Fe dư Þ nFe dư = 0,1 mol và 64.0,2x + 108.0,2y = 40,8 (1)
→ BT : e 0 , 2 . 3 + 2 . ( 0 , 2 - 0 , 1 ) = 0 , 2 x . 2 + 0 , 2 y (2). Từ (1), (2) suy ra: x = 1,5
Cho 16,6 gam hỗn hợp X gồm Al, Fe (số mol của Al và Fe bằng nhau) vào 200 ml dung dịch Y gồm Cu(NO3)2 và AgNO3. Sau khi phản ứng kết thúc, thu được chất rắn Z gồm 3 kim loại. Hòa tan toàn bộ lượng chất rắn Z vào dung dịch HCl dư, thu được 2,24 lít khí (đktc) và còn lại 40,8 gam chất rắn T không tan. Nồng độ mol/lít của Cu(NO3)2 trong Y có giá trị là
A. 2,0.
B. 1,0.
C. 1,5.
D. 1,3.
Chọn C.
Hỗn hợp X gồm Al và Fe với số mol mỗi chất bằng 0,2 mol
Hỗn hợp Y gồm Cu(NO3)2 (0,2x mol) và AgNO3 (0,2y mol)
Hỗn hợp Z gồm Ag, Cu và Fe dư Þ nFe dư = 0,1 mol và 64.0,2x + 108.0,2y = 40,8 (1)
→ B T : e 0 , 2 . 3 + 2 . 0 , 2 - 0 , 1 = 0 , 2 x . 2 + 0 , 2 y 2
Từ (1), (2) suy ra: x = 1,5
Câu 1: Cho 10,5 gam hỗn hợp hai kim loại Cu, Zn vào dung dịch H₂SO₄ loãng dư, người ta thu được 2,24 lít khí (đktc). Tính khối lượng chất rắn còn lại trong dung dịch sau phản ứng. Câu 2: Hòa tan 12 gam hỗn hợp gồm Al, Ag vào dung dịch H₂SO₄ loãng, dư. Phản ứng kết thúc thu được 13,44 lít khí H₂ (đktc). Tính phần trăm khối lượng mỗi kim loại trong hỗn hợp. Câu 3: Hòa tan 25,8 gam hỗn hợp gồm bột Al và Al₂O₃ trong dung dịch HCl dư. Sau phản ứng người ta thu được 0,6 gam khí H₂. Tính khối lượng muối AlCl₃ thu được.
Câu 2:
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ n_{H_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\\ n_{Al}=\dfrac{2.0,6}{3}=0,4\left(mol\right)\\ \%m_{Al}=\dfrac{0,4.27}{12}.100\%=90\%\Rightarrow\%m_{Ag}=100\%-90\%=10\%\)
Câu 3:
\(n_{H_2}=\dfrac{0,6}{2}=0,3\left(mol\right)\\ 2Al+6HCl\rightarrow2AlCl_3+3H_2\\ Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\\ n_{Al}=\dfrac{2}{3}.0,3=0,2\left(mol\right)\\ n_{Al_2O_3}=\dfrac{25,8-0,2.27}{102}=0,2\left(mol\right)\\ n_{AlCl_3}=n_{Al}+2n_{Al_2O_3}=0,2+2.0,2=0,6\left(mol\right)\\ m_{AlCl_3}=133,5.0,6=80,1\left(g\right)\)
Câu 1:
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\\ n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ n_{Zn}=n_{H_2}=0,1\left(mol\right)\\ m_{Zn}=0,1.65=6,5\left(g\right)\\ m_{rắn}=m_{hhCu,Zn}-m_{Zn}=10,5-6,5=4\left(g\right)\)
Cho 8,3 gam hỗn hợp (X) gồm Al, Fe (nAl=nFe) vào 100 ml dung dịch Y gồm Cu(NO3)2 và AgNO3. sau khi phản ứng kết thúc thu dduwwojc chất rắn A gồm 3 kim loại. Hòa tan A vào dung dịch HCl dư thấy có 1,12 lít khí thoát ra (đktc) và còn lại 28 gam chất rắn không tan B. Nồng độ CM của Cu(NO3)2 và AgNO3 là?
Ta có: $n_{Al}=n_{Fe}=0,1(mol)$
Sau phản ứng thì Al hết, Fe chưa phản ứng hoặc còn dư
Gọi số mol $Cu(NO_3)_2 và $AgNO_3$ lần lượt là a;b
Ta có: $64a+108b=28$
Bảo toàn e toàn bộ quá trình ta có: $2a+b=0,4$
Giải hệ ta được $a=0,1;b=0,2$
$\Rightarrow [Cu(NO_3)_2]=1M;[AgNO_3]=2M$
\(n_{H_2}=\dfrac{1.12}{22.4}=0.05\left(mol\right)\)
\(\Rightarrow n_{Fe\left(dư\right)}=0.05\left(mol\right)\)
\(n_{Al}=n_{Fe}=a\left(mol\right)\)
\(\Rightarrow a=\dfrac{8.3}{27+56}=0.1\)
\(n_{AgNO_3}=x\left(mol\right),n_{Cu\left(NO_3\right)_2}=y\left(mol\right)\)
\(m_{cr}=108x+64y=28\left(1\right)\)
Bảo toàn e :
\(x+2y=0.4\left(2\right)\)
\(\left(1\right),\left(2\right):x=0.2,y=0.1\)
\(C_{M_{AgNO_3}}=\dfrac{0.2}{0.1}=2\left(M\right)\)
\(C_{M_{Cu\left(NO_3\right)_2}}=\dfrac{0.1}{0.1}=1\left(M\right)\)
Nung nóng 3,72g hỗn hợp bột các kim loại Zn và Fe trong bột S dư. Chất rắn thu được sau phản ứng được hòa tan hoàn toàn bằng dung dịch H2SO4 loãng, nhận thấy có 1,344 lít khí (đktc) thoát ra. Xác định khối lượng mỗi kim loại trong hỗn hợp ban đầu.
Đặt nZn = x mol; nFe = y mol.
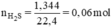
Ta có hệ phương trình: 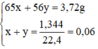
Giải hệ phương trình trên ta được:
x = 0,04 mol, y = 0,02 mol.
mZn = 65 × 0,04 = 2,6g
mFe = 56 × 0,02 = 1,12g
Cho 8,30 gam hỗn hợp X gồm Al, Fe (tỉ lệ mol 1:1) vào 100 ml dung dịch Y gồm Cu(NO3)2 và AgNO3. Sau khi phản ứng kết thúc, thu được chất rắn Z gồm ba kim loại. Hòa tan hoàn toàn Z vào dung dịch HCl dư, thu được 1,12 lít khí (đktc) và còn lại 28,0 gam chất rắn không tan. Nồng độ mol/l của Cu(NO3)2 và AgNO3 trong Y lần lượt là:
A. 2,0M và 1,0M.
B. 1,0M và 2,0M.
C. 0,2M và 0,1M.
D. 0,1M và 0,2M.
Chọn đáp án B
Do Al3+/Al > Fe2+/Fe > Cu2+/Cu > Fe3+/Fe2+ > Ag+/Ag ||⇒ Z gồm Fedư, Cu và Ag.
⇒ nFe dư = nH2 = 0,05 mol ||► Trong X có nAl = nFe = 8,3 ÷ (27 + 56) = 0,1 mol.
⇒ dung dịch sau phản ứng chứa 0,05 mol Fe(NO3)2 và 0,1 mol Al(NO3)3.
Đặt nCu(NO3)2 = x; nAgNO3 = y ⇒ ∑nNO3– = 2x + y = 0,05 × 2 + 0,1 × 3.
mrắn không tan = 64x + 108y = 28(g) ||⇒ Giải hệ có: x = 0,1 mol; y = 0,2 mol.
⇒ [Cu(NO3)2] = 1M; [AgNO3] = 2M ⇒ chọn B.