Cho a ( g) hỗn hợp gồm Feo , Fe2o3 và Fe3o4 tác dụng với Co dư sau phản ứng thu được 3.92 g Fe . Sản phẩm khi sinh ra cho qua dung dịch ca (oh) 2 dư thu được 7 (g) kết tủa . Tính a 

Những câu hỏi liên quan
Cho luồng khí CO dư đi qua 5,64 gam hỗn hợp gồm Fe, FeO, Fe2O3, Fe3O4 rồi nung nóng. Khí sinh ra sau phản ứng cho qua dung dịch nước vôi trong dư có 8 gam kết tủa. Khối lượng Fe thu được sau phản ứng là A. 4,63 g B. 4,0 g C. 4,36 g D. 4,2 g
Đọc tiếp
Cho luồng khí CO dư đi qua 5,64 gam hỗn hợp gồm Fe, FeO, Fe2O3, Fe3O4 rồi nung nóng. Khí sinh ra sau phản ứng cho qua dung dịch nước vôi trong dư có 8 gam kết tủa. Khối lượng Fe thu được sau phản ứng là
A. 4,63 g
B. 4,0 g
C. 4,36 g
D. 4,2 g
Cho luồng khí CO dư đi qua 5,64 gam hỗn hợp gồm Fe, FeO, Fe2O3, Fe3O4 rồi nung nóng. Khí sinh ra sau phản ứng cho qua dung dịch nước vôi trong dư có 8 gam kết tủa. Khối lượng Fe thu được sau phản ứng là A. 4,63 g B. 4,0 g C. 4,36 g D. 4,2 g
Đọc tiếp
Cho luồng khí CO dư đi qua 5,64 gam hỗn hợp gồm Fe, FeO, Fe2O3, Fe3O4 rồi nung nóng. Khí sinh ra sau phản ứng cho qua dung dịch nước vôi trong dư có 8 gam kết tủa. Khối lượng Fe thu được sau phản ứng là
A. 4,63 g
B. 4,0 g
C. 4,36 g
D. 4,2 g
Cho a gam bột sắt tác dụng với oxi trong điều kiện thích hợp thu được hỗn hợp B gồm (Fe, FeO, Fe2O3 , Fe3O4 ) có khối lượng là 21,6 gam. Cho hỗn hợp B tác dụng với dung dịch HNO3 loãng dư sau khi phản ứng kết thúc thu được 2,24 NO là sản phẩm khử duy nhất .Tính a
Quy đổi hỗn hợp B gồm Fe (x mol) và O (y mol)
Ta có: \(56x+16y=21,6\) (1)
Bảo toàn electron: \(3x=2y+3n_{NO}=2y+0,3\) (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,3\\y=0,3\end{matrix}\right.\) \(\Rightarrow m_{Fe}=0,3\cdot56=16,8\left(g\right)\)
Đúng 1
Bình luận (2)
Cho m gam Fe tác dụng với khí O2, sau một thời gian thu được 9,6 gam hỗn hợp X gồm Fe3O4, Fe2O3, FeO và Fe. Hòa tan hoàn toàn 9,6 gam X trong 200 ml dung dịch HNO3 3M (dư) đun nóng, thu được dung dịch Y và V lít khí NO (ở đktc, sản phẩm khử duy nhất). Cho 175 ml dung dịch Ba(OH)2 1M vào dung dịch Y, sau khi các phản ứng xảy ra hoàn toàn thu được 10,7 gam kết tủa. Giá trị của V là A. 2,24 B. 3,36 C. 1,12 D. 4,48.
Đọc tiếp
Cho m gam Fe tác dụng với khí O2, sau một thời gian thu được 9,6 gam hỗn hợp X gồm Fe3O4, Fe2O3, FeO và Fe. Hòa tan hoàn toàn 9,6 gam X trong 200 ml dung dịch HNO3 3M (dư) đun nóng, thu được dung dịch Y và V lít khí NO (ở đktc, sản phẩm khử duy nhất). Cho 175 ml dung dịch Ba(OH)2 1M vào dung dịch Y, sau khi các phản ứng xảy ra hoàn toàn thu được 10,7 gam kết tủa. Giá trị của V là
A. 2,24
B. 3,36
C. 1,12
D. 4,48.
Đáp án : A
nFe(OH)3 = 0,1 mol = nFe bđ => mO(X) = 4g
Qui X về 0,1 mol Fe và 0,25 mol O
Bảo toàn e : 3nFe = 2nO + 3nNO
=> nNO < 0 (Vô lý)
=> Fe3+ còn dư so với OH-
=> nOH- = nHNO3 dư + 3nFe(OH)3 => nHNO3 dư = 0,05 mol
=> nHNO3 pứ = 0,6 – 0,05 = 0,55 mol
Bảo toàn e : 3nFe = 2nO + 3nNO ; nHNO3 = 3nFe + nNO
Lại có : 56nFe + 16nO = 9,6g
=> nFe = 0,15 ; nO = 0,075 mol => nNO = 0,1 mol
=> V= 2,24 lit
Đúng 0
Bình luận (0)
Cho hỗn hợp A gồm ba oxit của sắt là Fe2O3, Fe3O4 và FeO với số mol bằng nhau. Lấy m1 gam A cho vào một ống sứ chịu nhiệt, nung nóng rồi cho một luồng khí CO đi qua ống. CO phản ứng hết, toàn bộ khí CO2 ra khỏi ống được hấp thụ hết vào bình đựng lượng dư dung dịch Ba(OH)2 thu được m2 gam kết tủa trắng. Chất còn lại trong ống sứ sau phản ứng có khối lượng là 19,20 gam gồm Fe, FeO và Fe3O4. Cho hỗn hợp này tác dụng hết với dung dịch HNO3 dư, đun nóng thì thu được 2,24 lít khí NO (sản phẩm khử duy...
Đọc tiếp
Cho hỗn hợp A gồm ba oxit của sắt là Fe2O3, Fe3O4 và FeO với số mol bằng nhau. Lấy m1 gam A cho vào một ống sứ chịu nhiệt, nung nóng rồi cho một luồng khí CO đi qua ống. CO phản ứng hết, toàn bộ khí CO2 ra khỏi ống được hấp thụ hết vào bình đựng lượng dư dung dịch Ba(OH)2 thu được m2 gam kết tủa trắng. Chất còn lại trong ống sứ sau phản ứng có khối lượng là 19,20 gam gồm Fe, FeO và Fe3O4. Cho hỗn hợp này tác dụng hết với dung dịch HNO3 dư, đun nóng thì thu được 2,24 lít khí NO (sản phẩm khử duy nhất của N+5, đo ở đktc). Giá trị m1, m2 và số mol của HNO3 phản ứng lần lượt là:
A. 18,560; 19,700 và 0,91 mol.
B. 20,880; 19,700 và 0,81 mol.
C. 18,560; 20,685 và 0,81 mol.
D. 20,880; 20,685 và 0,91 mol.
Cho hỗn hợp A gồm ba oxit của sắt là Fe2O3, Fe3O4 và FeO với số mol bằng nhau. Lấy
m
1
gam A cho vào một ống sứ chịu nhiệt, nung nóng rồi cho một luồng khí CO đi qua ống. CO phản ứng hết, toàn bộ khí CO2 ra khỏi ống được hấp thụ hết vào bình đựng lượng dư dung dịch Ba(OH)2 thu được m2 gam kết tủa trắng. Chất còn lại trong ống sứ sau phản ứng có khối lượng là 19,20 gam gồm Fe, FeO và Fe3O4. Cho hỗn hợp này tác dụ...
Đọc tiếp
Cho hỗn hợp A gồm ba oxit của sắt là Fe2O3, Fe3O4 và FeO với số mol bằng nhau. Lấy m 1 gam A cho vào một ống sứ chịu nhiệt, nung nóng rồi cho một luồng khí CO đi qua ống. CO phản ứng hết, toàn bộ khí CO2 ra khỏi ống được hấp thụ hết vào bình đựng lượng dư dung dịch Ba(OH)2 thu được m2 gam kết tủa trắng. Chất còn lại trong ống sứ sau phản ứng có khối lượng là 19,20 gam gồm Fe, FeO và Fe3O4. Cho hỗn hợp này tác dụng hết với dung dịch HNO3 dư, đun nóng thì thu được 2,24 lít khí NO (sản phẩm khử duy nhất của N + 5 , đo ở đktc). Giá trị m1, m2 và số mol của HNO3 phản ứng lần lượt là
A. 18,560; 19,700 và 0,91
B. 20,880; 19,700 và 0,81
C. 18,560; 20,685 và 0,81
D. 20,880; 20,685 và 0,91
Đáp án D
Quy đổi A chỉ gồm Fe3O4 + CO → 19,2 gam (Fe : x mol + O : y mol) + CO2
19,2 gam (Fe : x mol + O : y mol) + HNO3 → Fe(NO3)3 + NO + H2O
Ta có hệ phương trình
(1) 56x + 16y = 19,2
(2) ĐLBT mol e : 3x = 2y + 0,1*3
→ x = 0,27 ; y = 0,255 → n(Fe3O4) = 0,09 mol → m1 = 20,880 gam
→ n(CO2) = n(CaCO3) = 0,09*4 – 0,255 = 0,105 → m2 = 20,685 gam
n(HNO3) = 0,27*3 + 0,1 = 0,91 mol
Đúng 0
Bình luận (0)
Cho hỗn hợp A gồm ba oxit của sắt là Fe2O3, Fe3O4 và FeO với số mol bằng nhau. Lấy m1 gam A cho vào một ống sứ chịu nhiệt, nung nóng rồi cho một luồng khí CO đi qua ống. CO phản ứng hết, toàn bộ khí CO2 ra khỏi ống được hấp thụ hết vào bình đựng lượng dư dung dịch Ba(OH)2 thu được m2 gam kết tủa trắng. Chất còn lại trong ống sứ sau phản ứng có khối lượng là 19,20 gam gồm Fe, FeO và Fe3O4. Cho hỗn hợp này tác dụng hết với dung dịch HNO3 dư, đun nóng thì thu được 2,24 lít khí NO (sản phẩm khử duy...
Đọc tiếp
Cho hỗn hợp A gồm ba oxit của sắt là Fe2O3, Fe3O4 và FeO với số mol bằng nhau. Lấy m1 gam A cho vào một ống sứ chịu nhiệt, nung nóng rồi cho một luồng khí CO đi qua ống. CO phản ứng hết, toàn bộ khí CO2 ra khỏi ống được hấp thụ hết vào bình đựng lượng dư dung dịch Ba(OH)2 thu được m2 gam kết tủa trắng. Chất còn lại trong ống sứ sau phản ứng có khối lượng là 19,20 gam gồm Fe, FeO và Fe3O4. Cho hỗn hợp này tác dụng hết với dung dịch HNO3 dư, đun nóng thì thu được 2,24 lít khí NO (sản phẩm khử duy nhất của N+5, đo ở đktc). Giá trị m1, m2 và số mol của HNO3 phản ứng lần lượt là:
A. 18,560; 19,700 và 0,91 mol.
B. 20,880; 19,700 và 0,81 mol.
C. 18,560; 20,685 và 0,81 mol.
D. 20,880; 20,685 và 0,91 mol.
Cho hỗn hợp A gồm ba oxit của sắt là Fe2O3, Fe3O4 và FeO với số mol bằng nhau. Lấy m1 gam A cho vào một ống sứ chịu nhiệt, nung nóng rồi cho một luồng khí CO đi qua ống. CO phản ứng hết, toàn bộ khí CO2 ra khỏi ống được hấp thụ hết vào bình đựng lượng dư dung dịch Ba(OH)2 thu được m2 gam kết tủa trắng. Chất còn lại trong ống sứ sau phản ứng có khối lượng là 19,20 gam gồm Fe, FeO và Fe3O4. Cho hỗn hợp này tác dụng hết với dung dịch HNO3 dư, đun nóng thì thu được 2,24 lít khí NO (sản phẩm khử duy...
Đọc tiếp
Cho hỗn hợp A gồm ba oxit của sắt là Fe2O3, Fe3O4 và FeO với số mol bằng nhau. Lấy m1 gam A cho vào một ống sứ chịu nhiệt, nung nóng rồi cho một luồng khí CO đi qua ống. CO phản ứng hết, toàn bộ khí CO2 ra khỏi ống được hấp thụ hết vào bình đựng lượng dư dung dịch Ba(OH)2 thu được m2 gam kết tủa trắng. Chất còn lại trong ống sứ sau phản ứng có khối lượng là 19,20 gam gồm Fe, FeO và Fe3O4. Cho hỗn hợp này tác dụng hết với dung dịch HNO3 dư, đun nóng thì thu được 2,24 lít khí NO (sản phẩm khử duy nhất của N+5, đo ở đktc). Giá trị m1, m2 và số mol của HNO3 phản ứng lần lượt là:
A. 18,560; 19,700 và 0,91 mol.
B. 20,880; 19,700 và 0,81 mol.
C. 18,560; 20,685 và 0,81 mol.
D. 20,880; 20,685 và 0,91 mol.
Đáp án là D.
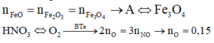
![]()
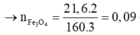
![]()
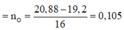
=> m 2 = 20,865 gam
![]()
= 3,3.0,09 + 0,1 = 0,91 mol
Đúng 0
Bình luận (0)
Cho hỗn hợp A gồm ba oxit của sắt là Fe2O3, Fe3O4 và FeO với số mol bằng nhau. Lấy m1 gam A cho vào một ống sứ chịu nhiệt, nung nóng rồi cho một luồng khí CO đi qua ống. CO phản ứng hết, toàn bộ khí CO2 ra khỏi ống được hấp thụ hết vào bình đựng lượng dư dung dịch Ba(OH)2 thu được m2 gam kết tủa trắng. Chất còn lại trong ống sứ sau phản ứng có khối lượng là 19,20 gam gồm Fe, FeO và Fe3O4. Cho hỗn hợp này tác dụng hết với dung dịch HNO3 dư, đun nóng thì thu được 2,24 lít khí NO (sản phẩm khử duy...
Đọc tiếp
Cho hỗn hợp A gồm ba oxit của sắt là Fe2O3, Fe3O4 và FeO với số mol bằng nhau. Lấy m1 gam A cho vào một ống sứ chịu nhiệt, nung nóng rồi cho một luồng khí CO đi qua ống. CO phản ứng hết, toàn bộ khí CO2 ra khỏi ống được hấp thụ hết vào bình đựng lượng dư dung dịch Ba(OH)2 thu được m2 gam kết tủa trắng. Chất còn lại trong ống sứ sau phản ứng có khối lượng là 19,20 gam gồm Fe, FeO và Fe3O4. Cho hỗn hợp này tác dụng hết với dung dịch HNO3 dư, đun nóng thì thu được 2,24 lít khí NO (sản phẩm khử duy nhất của N+5, đo ở đktc). Giá trị m1, m2 và số mol của HNO3 phản ứng lần lượt là
A. 18,560; 19,700 và 0,91
B. 20,880; 19,700 và 0,81
C. 18,560; 20,685 và 0,81
D. 20,880; 20,685 và 0,91
Quy đổi A chỉ gồm Fe3O4 + CO → 19,2 gam (Fe : x mol + O : y mol) + CO2
19,2 gam (Fe : x mol + O : y mol) + HNO3 → Fe(NO3)3 + NO + H2O
Ta có hệ phương trình
(1) 56x + 16y = 19,2
(2) ĐLBT mol e : 3x = 2y + 0,1*3
→ x = 0,27 ; y = 0,255 → n(Fe3O4) = 0,09 mol → m1 = 20,880 gam
→ n(CO2) = n(CaCO3) = 0,09*4 – 0,255 = 0,105 → m2 = 20,685 gam
n(HNO3) = 0,27*3 + 0,1 = 0,91 mol → Đáp án D.
Đúng 0
Bình luận (0)