1, cho 150ml ZNSO4 0,2M tác dụng với 400ml dd KOH 0,2M. Sau khi phản ứng hoàn toàn thu được bao nhiêu g kết tủa.
2, tính thể tích dd NaOH 0,5 M cần dùng để phản ứng 100ml Al2(SO4)3 0,2 M tạo kết tủa tối đa
Cho 100ml dd Al2(SO4)3 0,05M phản ứng với V ml dd NaOH 0,2M, sau phản ứng thu được 0,78 gam kết tủa. Tính giá trị của V
Al2(SO4)3 +6NaOH---->2Al(OH)3 +3Na2SO4(1)
Al(OH)3 +NaOH----->NaAlO2 +2H2O(2)
Ta có
n\(_{Al2\left(SO4\right)3}=0,05.0,1=0,005\left(mol\right)\)
Theo pthh1
n\(_{Al\left(OH\right)3}=2n_{Al2\left(SO4\right)3}=0,01\left(mol\right)\)
Mà n\(_{Al\left(OH\right)3}=\frac{0,78}{78}=0,01\left(mol\right)\)
=> NaOH dư
Theo pthh
n\(_{NaOH}=6n_{Al2\left(SO4\right)3}=0,06\left(mol\right)\)
V\(_{NaOH}=\frac{0,06}{0,2}=0,3\left(M\right)\)
Chúc bạn học tốt
Trộn 100ml dd X chứa Cuso4 0,1M và Mgcl2 0,3M tác dụng với 400 dd Y gồm Ba(oh)2 0,05M và Koh 0,2M .Tính kết tủa thu được sau phản ứng?
Cho 2.7 gam al phản ứng với 450ml dd HCl 1M tạo dd A . Cho A tác dụng vs 500 ml dd NaOH 1M thu được kết tủa . khối lượng kết tủa là?
đang cần gấp ai lm đc gúp em trong chiều nay đc ko ạ cảm ơn nhìu nhìu
Cho 250 ml dd NaOH 1M tác dụng với dd CuSO4 0,5 M thu được kết tủa và nước lọc. Lọc kết tủa nung đến khối lượng không đổi. a) Viết Các PTHH . b) Tính khối lượng chất rắn thu được sau khi nung? c) Tính thể tích dd CuSO4 0,5 M cần phản ứng? d) Tính khối lượng chất tan có trong nước lọc? (Cho Cu= 64, H = 1 , S = 32, O = 16,Na = 23)
Cho V lít dd NaOH 1M vào 150ml dd Al2(SO4)3 0,5 M. Sau phản ứng xảy ra hoàn toàn, lọc kết tủa nung đến khối lượng không đổi được 5,1 g chất rắn. Tính V (Giải chi tiết cho mình nhé và làm ơn cho mình hỏi dạng bài này tên gì và cách làm như thế nào vậy?)
cho hỗn hợp gồm 1,12g Fe và 1,93g Cu vào 400ml dd chứa hh gồm H2SO4 0,5M và NaNO3 0,2M Sau khi các phản ứng xảy ra hoàn toàn , thu được dd X và khí NO.Cho V ml dd NaOH vào dd X thì lượng kết tủa thu được lớn nhất.Giá trị tối thiểu của V là bao nhiêu?
Số mol Fe và Cu lần lượt là 0,02 và 0,03 mol.
3Cu + 8H+ + 2NO3- ---> 3Cu2+ + 2NO + 4H2O
Fe + 4H+ + NO3- ---> Fe3+ + NO + 2H2O
Ta tính được số mol H+ dư là 0,24 mol
Số mol NO3- dư là 0,04 mol.
Vậy trong dung dịch X lúc này có
0,02 mol Fe3+
0,03 mol Cu2+
0,24 mol H+
Vậy lượng NaOH cần dùng là 0,02*3 + 0,03*2 + 0,24*1 = 0,36 mol
Vì không có nồng độ của dung dịch NaOH nên tiếp theo thì... chịu ^^
1) Trộn 250ml dd chứa Ba(OH)2 0,01M va KOH 0,02 M với 250 ml dd H2SO4 a mol/l thu được b gam kết tủa và 500 ml dd có pH= 2. Tính a,b
2) Cho 100ml dd Al2(SO4)3 0,05M phản ứng với V ml dd NaOH 0,2M, sau phản ứng thu được 0,78 gam kết tủa. Tính giá trị của V
1.
\(nOH^-=2nBa\left(OH\right)_2+nKOH=2.0,25.0,01+0,25.0,02=0,01mol\)\(nH^+=2nH_2SO_4=0,5a\left(mol\right)\)
Dung dịch sau phản ứng là môi trường axit.
\(pH=2\Rightarrow\left[H^+\right]=10^{-2}M\)
\(\frac{nH^+-nOH^-}{V}=\left[H^+\right]\)
\(\Leftrightarrow\frac{0,5a-0,01}{0,5}=10^{-2}\)
\(\Leftrightarrow a=0,03M\)
\(nBa^{2+}=2,5.10^{-3}mol\)
\(nSO_4^{2-}=7,5.10^{-3}mol\)
\(Ba^{2+}+SO_4^{2-}\rightarrow BaSO_4\)
Chất sản phẩm tính theo nBa2+
\(b=2,5.10^{-3}.233=0,5825g\)
Không biết có đúng hay không.
2.Gọi A là thể tích dd NaOH (lít)
\(nAl^{3+}=2nAl_2\left(SO_4\right)_3=2.0,1.0,05=0,01mol\)
\(nOH^-=nNaOH=0,2A\left(mol\right)\)
\(nAl\left(OH\right)_3=\frac{0,78}{78}=0,01mol\)
\(Al^{3+}+3OH^-\rightarrow Al\left(OH\right)_3\)
\(0,01-0,6A---0,01--mol\)
Ta có:
\(\frac{nAl^{3+}}{1}=\frac{nOH^-}{3}\)
\(\Leftrightarrow0,01=\frac{0,6A}{3}\)
\(\Leftrightarrow A=0,05=50ml\)
Cho m gam Na tan hết trong 100ml dung dịch Al2(SO4)3 0,2M. Sau phản ứng thu được 0,78 gam kết tủa. Giá trị của m là
A. 0,69
B. 0,69 hoặc 3,45
C. 0,69 hoặc 3,68
D. 0,69 hoặc 2,76
Đáp án B
• m gam Na + 0,02 mol Al2(SO4)3 → 0,01 mol ↓
• TH1: NaOH hết
2Na + 2H2O → 2NaOH + H2↑
6NaOH + Al2(SO4)3 → 2Al(OH)3↓ + 3Na2SO4
nNa = nNaOH = 0,01 × 3 = 0,03 mol
→ mNa = 0,03 × 23 = 0,69 gam.
• TH2: NaOH dư
2Na + 2H2O → 2NaOH + H2↑ (*)
6NaOH + Al2(SO4)3 → 2Al(OH)3↓ + 3Na2SO4 (**)
NaOH + Al(OH)3 → NaAlO2 + 2H2O (***)
Theo (**) nNaOH = 0,02 × 6 = 0,12 mol; nAl(OH)3 = 0,02 × 2 = 0,04 mol.
Theo (***) nAl(OH)3 phản ứng = 0,04 - 0,01 = 0,03 mol
→ nNaOH = 0,03 mol
→ ∑nNaOH = 0,03 + 0,12 = 0,15 mol → nNa = 0,15 mol
→ mNa = 0,15 × 23 = 3,45 gam
cho V lit dd NaOH 2M vào dd chứa 0,1 mol Al2(SO4)3 và 0,1 mol H2SO4 đến khi phản ứng hoàn toàn thu đc 7,8 g kết tủa . Giá trị lớn nhất của V để thu đc lượng kết tủa trên là
Ta có: \(n_{Al\left(OH\right)_3}=\dfrac{7,8}{78}=0,1\left(mol\right)\)
PTHH: \(2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
0,2______0,1 (mol)
\(6NaOH+Al_2\left(SO_4\right)_3\rightarrow3Na_2SO_4+2Al\left(OH\right)_3\downarrow\)
0,3________0,05___________________0,1 (mol)
Ta có: \(n_{NaOH}=0,5\left(mol\right)\) \(\Rightarrow V_{ddNaOH}=\dfrac{0,5}{2}=0,25\left(l\right)\)
Cho 200 ml dung dịch chứa KOH 0,9M và Ba(OH)2 0,2M vào 100 ml dung dịch H2SO4 0,3M và Al2(SO4)3 0,3M. Sau khi các phản ứng xảy ra hoàn toàn, khối lượng kết tủa thu được là
A. 9,32
B. 10,88
C. 14,00
D. 12,44
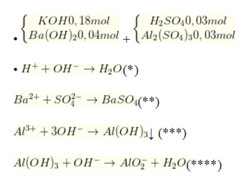
n O H - = n H + = 0 , 06 m o l T h e o ( * * ) n B a S O 4 = n B a 2 + = 0 , 04 m o l T h e o ( * * * ) n O H - = 3 x 0 , 03 x 2 = 0 , 18 m o l ; n A l ( O H ) 3 = 0 , 03 x 2 = 0 , 06 m o l T h e o ( * * * * ) n O H - = 0 , 18 + 0 , 04 x 2 - 0 , 06 - 0 , 18 = 0 , 02 m o l n A l ( O H ) 3 d ư = 0 , 06 - 0 , 02 = 0 , 04 m o l .
→ m↓ = mAl(OH)3 + mBaSO4 = 0,04 × 78 + 0,04 × 233 = 12,44 gam
→ Đáp án đúng là đáp án D