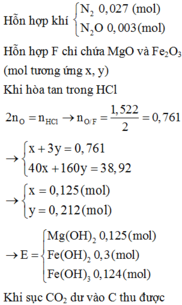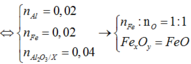Một Hydrat sắt (III) Clorua có khối lượng là 10,82gam phản ứng với dung dịch NaOH dư thu được kết tủa màu nâu đỏ . Khối lượng chất rắn sau khi nung nóng kết tủa thu được làm khô là 3,2gam . Hãy xác định công thưucs phân tử của hydrat đó

Những câu hỏi liên quan
cho 16,25 gam FeCl3 tác dụng với 0,4 mol NaOH ta thu được 1 kết quả màu đỏ nâu
a} viết PTHH. Xác định loại phản ứng
b} tính khối lượng chất kết tủa
c} lọc kết tủa đen nung đến khối lượng không đổi thu được chất rắn X .Tính khối lượng chất rắn thu được sau khi nung
a.
\(n_{FeCl_3}\) = \(\frac{n}{M}=\frac{16,25}{162,5}=0,1\left(mol\right)\)
PTHH FeCl3 + 3NaOH → Fe(OH)3 ↓ + 3NaCl (là phản ứng trao đổi)
mol 0,1 0,4
ta có:
\(n_{FeCl_3}=\frac{0,1}{1}=0,1\) < \(n_{NaOH}=\frac{0,4}{3}\approx0,13\)
Vậy FeCl3 phản ứng hết, NaOH phản ứng dư
Ta có phương trình sau:
FeCl3 + 3NaOH → Fe(OH)3 ↓ + NaCl
mol 0,1 → 0,3 0,1 0,3
\(m_{Fe\left(OH\right)_3}=n.M=0,1.107=10,7\left(g\right)\)
b. Ta có phương trình
2Fe(OH)3 \(\underrightarrow{t^o}\) Fe2O3 + H2O
mol 0,1 0,05
\(m_{Fe\left(OH\right)_3}=n.M=0,05.160=8\left(g\right)\)
Đúng 0
Bình luận (2)
a/ PTHH : FeCl3 + 3NaOH ===> Fe(OH)3 + 3NaCl
=> Đây là phản ứng trao đổi
b/ nFeCl3 = 16,25 / 162,5 = 0,1 mol
Lập tỉ lệ số mol theo phương trình => FeCl3 hết, NaOH dư
=> nFe(OH)3 = nFeCl3 = 0,1 mol
=> mFe(OH)3 = 0,1 x 107 = 10,7 gam
c/ PTHH : 2Fe(OH)3 ===>(nhiệt độ) Fe2O3 + 3H2O
Theo PT, nFe2O3 = 0,5nFe(OH)3 = 0,5 x 0,1 = 0,05 mol
=> mFe2O3 = 0,05 x 160 = 8 gam
Chúc bạn học tốt!!!
Đúng 0
Bình luận (1)
Cho một lượng dung dịch FeCl3 phản ứng vừa đủ với dung dịch NaOH. Sau phản ứng thu được 10,7 g chất kết tủa đỏ nâu. Đem nung lượng kết tủa này đến khối lượng không đổi thu được chất rắn X. Tính khối lượng chất rắn X.
FeCl3+3NaOH-->Fe(OH)3+3NaCl
nFe(OH)3=10,7\107=0,1 mol
2Fe(OH)3-to->Fe2O3+3H2O
0,1-------------------0,05 mol
=>mFe2O3=0,05.160=8 g
Đúng 0
Bình luận (0)
Bài 7: Cho 200 ml dung dịch CuCl2 2M phản ứng vừa đủ với 100 gam dung dịch NaOH. Khi phản ứng kết thúc thu được kết tủa X và dung dịch Y. Lọc kết tủa rồi đem nung kết tủa đến khối lượng không đổi.
a. Tính khối lượng của chất rắn thu được sau khi nung.
b. Tính nồng độ phần trăm của dung dịch thu được. Biết 𝐷𝐶𝑢𝐶𝑙2= 1,35 g/ml
Bài 7 :
200ml = 0,2l
\(n_{CuCl2}=2.0,2=0,4\left(mol\right)\)
Pt : \(CuCl_2+2NaOH\rightarrow Cu\left(OH\right)_2+2NaCl|\)
1 2 1 2
0,4 0,8 0,4 0,8
\(Cu\left(OH\right)_2\underrightarrow{t^o}CuO+H_2O|\)
1 1 1
0,4 0,4
a) \(n_{CuO}=\dfrac{0,4.1}{1}=0,4\left(mol\right)\)
⇒ \(m_{CuO}=0,4.40=32\left(g\right)\)
b) \(n_{NaCl}=\dfrac{0,4.2}{1}=0,8\left(mol\right)\)
⇒ \(m_{NaCl}=0,8.58,5=46,8\left(g\right)\)
\(m_{ddCuCl2}=1,35.200=270\left(g\right)\)
\(m_{ddspu}=270+100=370\left(g\right)\)
\(C_{NaCl}=\dfrac{46,8.100}{370}=12,65\)0/0
Chúc bạn học tốt
Đúng 1
Bình luận (1)
Sục khí NH3 dư vào 200 ml dung dịch hỗn hợp chứa AlCl3 1M và CuCl2 0,5M sau khi phản ứng xảy ra hoàn toàn thu được kết tủa, lọc kết tủa đem nung nóng đến khối lượng không đổi thì thu được chất rắn có khối lượng là bao nhiêu? A. 10,2 gam B. 20,4 gam C. 18,2 gam D. 28,4 gam
Đọc tiếp
Sục khí NH3 dư vào 200 ml dung dịch hỗn hợp chứa AlCl3 1M và CuCl2 0,5M sau khi phản ứng xảy ra hoàn toàn thu được kết tủa, lọc kết tủa đem nung nóng đến khối lượng không đổi thì thu được chất rắn có khối lượng là bao nhiêu?
A. 10,2 gam
B. 20,4 gam
C. 18,2 gam
D. 28,4 gam
Đáp án A
3NH3+ AlCl3+ 3H2O → 2Al(OH)3+3 NH4Cl (1)
2NH3+ CuCl2+ 2H2O → Cu(OH)2+2 NH4Cl (2)
4NH3+ Cu(OH)2 → [Cu(NH3)4](OH)2 (3)
Do NH3 dư nên sau phản ứng chỉ thu được kết tủa Al(OH)3
2Al(OH)3 → t o Al2O3+ 3H2O (3)
Có: nAl(OH)3= nAlCl3= 0,2 mol → nAl2O3= 0,1 mol
→ mAl2O3= 0,1.102=10,2 gam
Đúng 0
Bình luận (0)
Cho 100ml dung dịch FeCL2 1M tác dụng vừa đủ với dung dịch NaOH 0,5M trong không khí, được kết tủa màu nâu đỏ. Lọc lấy kết tủa, nung đến khối lượng không đổi thì thu được chất rắn A.
a) Viết PTHH
b) Tính khối lượng của chất rắn A
c) Tính thể tích dung dịch NaOH cần dùng
Tiến hành phản ứng nhiệt nhôm hỗn hợp gồm Al và FexOy thu được hỗn hợp chất rắn X. Cho X tác dụng với dung dịch NaOH dư thu được dung dịch Y, phần không tan Z và 0,672 lít khí H2. Cho dung dịch HCl vào Y đến khi được lượng kết tủa lớn nhất, lọc kết tủa, nung tới khối lượng không đổi thu được 5,1 gam chất rắn. Cho Z tác dụng với dung dịch H2SO4 đặc nóng, sau phản ứng chỉ thu được dung dịch E chứa một muối sắt duy nhất và 2,688 lít khí SO2. Biết các khí đều đo ở đktc, các phản ứng xảy ra hoàn toàn...
Đọc tiếp
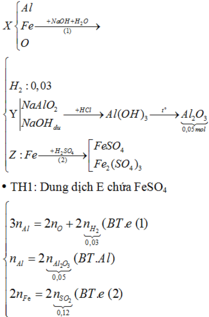
Tiến hành phản ứng nhiệt nhôm hỗn hợp gồm Al và FexOy thu được hỗn hợp chất rắn X. Cho X tác dụng với dung dịch NaOH dư thu được dung dịch Y, phần không tan Z và 0,672 lít khí H2. Cho dung dịch HCl vào Y đến khi được lượng kết tủa lớn nhất, lọc kết tủa, nung tới khối lượng không đổi thu được 5,1 gam chất rắn. Cho Z tác dụng với dung dịch H2SO4 đặc nóng, sau phản ứng chỉ thu được dung dịch E chứa một muối sắt duy nhất và 2,688 lít khí SO2. Biết các khí đều đo ở đktc, các phản ứng xảy ra hoàn toàn. Công thức phân tử của sắt oxit là
A. FeO hoặc Fe2O3
B. FeO hoặc Fe3O4
C. Fe2O3 hoặc Fe3O4
D. Fe2O3
Hòa tan hoàn toàn m gam hỗn hợp rắn A gồm Al, Mg và Fe2O3 trong V lít dung dịch HNO3 0,5M. Sau phản ứng thu được dung dịch B và 0,672 lít (đktc) hỗn hợp khí D gồm 2 khí không màu, không hóa nâu trong không khí có tỉ khối so với H2 là 14,8. Đem dung dịch B tác dụng với NaOH dư thu được dung dịch C và kết tủa E nặng 47,518 gam. Đem lọc kết tủa E nung trong không khí đến khối lượng không đổi thu được 38,92 gam chất rắn F. Để hòa tan hết F cần dùng 1,522 lít dung dịch HCl 1M. Sục CO2 dư vào dung dịc...
Đọc tiếp
Hòa tan hoàn toàn m gam hỗn hợp rắn A gồm Al, Mg và Fe2O3 trong V lít dung dịch HNO3 0,5M. Sau phản ứng thu được dung dịch B và 0,672 lít (đktc) hỗn hợp khí D gồm 2 khí không màu, không hóa nâu trong không khí có tỉ khối so với H2 là 14,8. Đem dung dịch B tác dụng với NaOH dư thu được dung dịch C và kết tủa E nặng 47,518 gam. Đem lọc kết tủa E nung trong không khí đến khối lượng không đổi thu được 38,92 gam chất rắn F. Để hòa tan hết F cần dùng 1,522 lít dung dịch HCl 1M. Sục CO2 dư vào dung dịch C thu được 13,884 gam kết tủa trắng. Khối lượng muối có trong B là
A. 148,234
B. 167,479
C. 128,325
D. 142,322
Tiến hành phản ứng nhiệt nhôm m gam hỗn hợp gồm Al và FexOy thu được hỗn hợp chất rắn X. Cho X tác dụng với dung dịch NaOH dư thu được dung dịch Y, phần không tan Z và 0,672 lít khí H2. Cho dung dịch HCl vào Y đến khi được lượng kết tủa lớn nhất, lọc kết tủa, nung tới khối lượng không đổi thu được 5,1 gam chất rắn. Cho Z tác dụng với dung dịch H2SO4 đặc nóng (lượng ít nhất) sau phản ứng chỉ thu được dung dịch E chứa một muối sắt duy nhất và 2,688 lít khí SO2. Biết các khí đều đo ở đktc, các phả...
Đọc tiếp
Tiến hành phản ứng nhiệt nhôm m gam hỗn hợp gồm Al và FexOy thu được hỗn hợp chất rắn X. Cho X tác dụng với dung dịch NaOH dư thu được dung dịch Y, phần không tan Z và 0,672 lít khí H2. Cho dung dịch HCl vào Y đến khi được lượng kết tủa lớn nhất, lọc kết tủa, nung tới khối lượng không đổi thu được 5,1 gam chất rắn. Cho Z tác dụng với dung dịch H2SO4 đặc nóng (lượng ít nhất) sau phản ứng chỉ thu được dung dịch E chứa một muối sắt duy nhất và 2,688 lít khí SO2. Biết các khí đều đo ở đktc, các phản ứng xảy ra hoàn toàn. Công thức phân tử của oxit sắt và phần trăm khối lượng của nó trong m gam hỗn hợp ban đầu là
A. FeO và 76,19%
B. FeO và 94,23%
C. Fe2O3 và 70,33%
D. Fe2O3 và 80,07%
Câu 9:Trộn 1,35g CuCl2 với 28g dung dịch KOH 10% thu được kết tủa và nước lọc. Lọc kết tủa, nung kết tủa đến khối lượng không đổi thu được chất rắn màu đen.
a. Viết phương trình phản ứng xảy ra?
b. Tính khối lượng chất rắn thu được sau phản ứng?
c. Tính C% các chất có trong nước lọc sau phản ứng?
\(n_{CuCl_2}=\dfrac{1,35}{135}=0,01(mol)\\ n_{KOH}=\dfrac{28.10}{100.56}=0,05(mol)\\ a,CuCl_2+2KOH\to Cu(OH)_2\downarrow+2KCl\\ Cu(OH)_2\xrightarrow{t^o}CuO+H_2O\\ \dfrac{n_{CuCl_2}}{1}<\dfrac{n_{KOH}}{2}\Rightarrow KOH\text{ dư}\\ b,n_{CuO}=n_{Cu(OH)_2}=0,01(mol)\\ \Rightarrow m_{CuO}=0,01.80=0,8(g)\)
\(c,n_{KCl}=0,02(mol);n_{KOH(dư)}=0,05-0,01.2=0,03(mol)\\ \Rightarrow m_{Cu(OH)_2}=0,01.98=0,98(g);m_{KCl}=0,02.74,9=1,49(g)\\ \Rightarrow \begin{cases} C\%_{KCl}=\dfrac{1,49}{1,35+28-0,98}.100\%=5,25\%\\ C\%_{KOH(dư)}=\dfrac{0,03.56}{1,35+28-0,98}.100=5,92\% \end{cases}\)
Đúng 1
Bình luận (0)