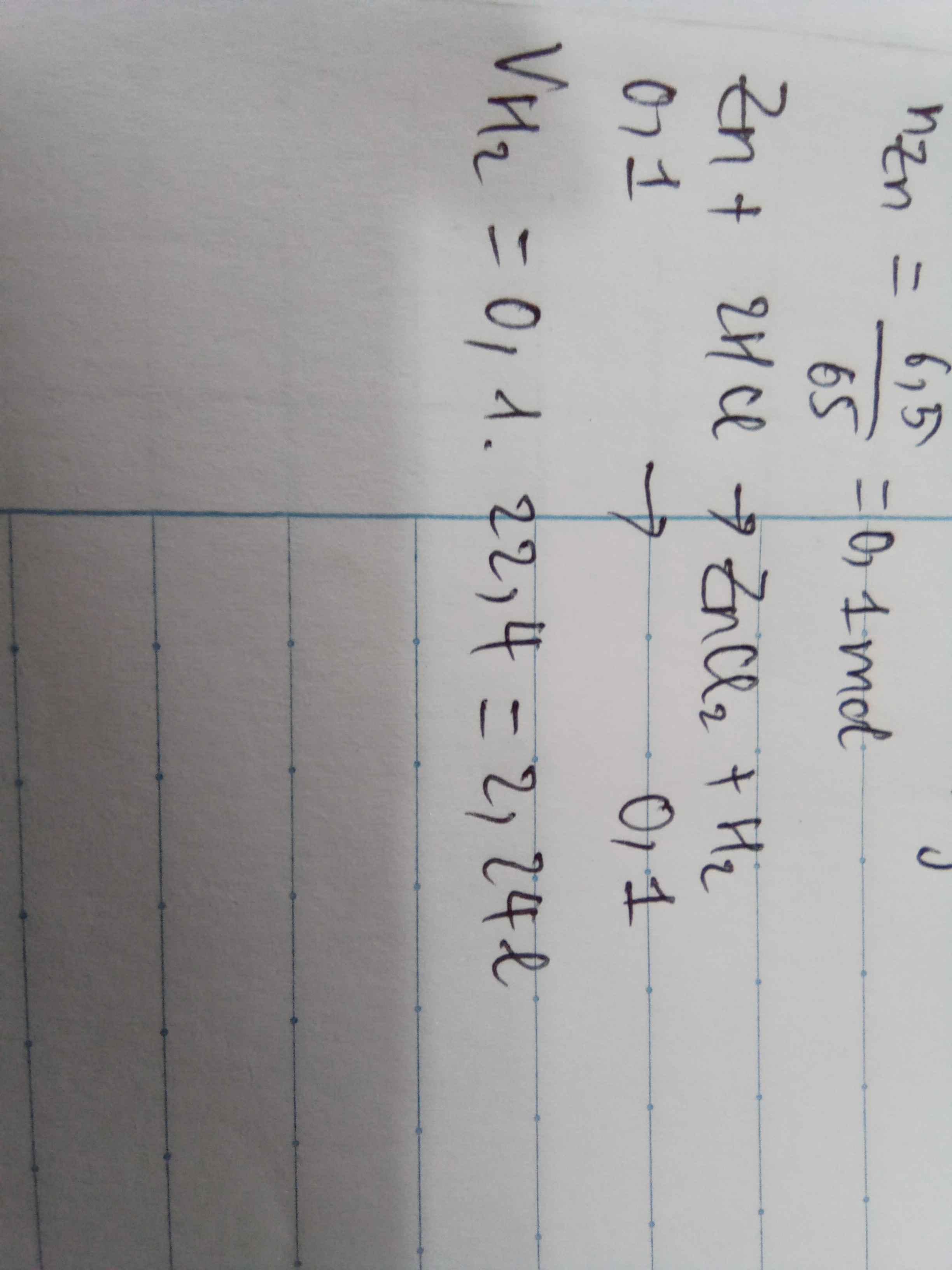Cho 3,25 gam Zn tác dụng vừa đủ với 200ml dung dịch HCl, thu được muối ZnCl2 và V lít H2 (đktc) thoát ra. a) Viết PTHH xảy ra. b) Tính V. c) Tính nồng độ mol/l của dung dịch HCl cần dùng.

Những câu hỏi liên quan
Cho 6,5 gam Zn tác dụng hết với dung dịch axit HCl thu được muối ZnCl2 và thoát ra V lít khí H2 (đktc).
a) Viết phương trình hóa học xảy ra.
b) Tính thể tích khí H2 (đktc)
\(n_{Zn}=\dfrac{6,5}{65}=0,1mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,2 0,1 0,1
\(V_{H_2}=0,1\cdot22,4=2,24l\)
Đúng 2
Bình luận (0)
Hòa tan hoàn toàn 13 gam Zn cần dùng vừa đủ dung dịch axit HCl 7,3% thu được dung dịch muối X và thấy thoát ra V lít khí H2 (ở đktc) a. Tính giá trị của V? b. Tính khối lượng dung dịch axit HCl đã phản ứng? c. Tính nồng độ phần trăm của muối trong X?
a)
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
0,2-->0,4----->0,2--->0,2
=> VH2 = 0,2.22,4 = 4,48 (l)
b) mHCl = 0,4.36,5 = 14,6 (g)
=> \(m_{dd.HCl}=\dfrac{14,6.100}{7,3}=200\left(g\right)\)
c)
mdd sau pư = 13 + 200 - 0,2.2 = 212,6 (g)
mZnCl2 = 0,2.136 = 27,2 (g)
=> \(C\%=\dfrac{27,2}{212,6}.100\%=12,8\%\)
Đúng 2
Bình luận (0)
Cho 6,5 gam Zn tác dụng hết với dung dịch axit HCl thu được muối ZnCl2 và thoát ra V lít khí H2 (đktc).a) Viết phương trình hóa học xảy ra.b) Tính thể tích khí H2 (đktc)
Hòa tan hoàn toàn 13 gam Zn cần dùng vừa đủ dung dịch HCl 7,3 % thu được dung dịch X và thấy thoát ra V lít khí H2 (ở đktc)
a. Viết phương trình phản ứng hóa học?
b. Tính giá trị của V?
c. Tính khối lượng muối thu được?
d. Tính nồng độ phần trăm muối trong X?
Đọc tiếp
Hòa tan hoàn toàn 13 gam Zn cần dùng vừa đủ dung dịch HCl 7,3 % thu được dung dịch X và thấy thoát ra V lít khí H2 (ở đktc)
a. Viết phương trình phản ứng hóa học?
b. Tính giá trị của V?
c. Tính khối lượng muối thu được?
d. Tính nồng độ phần trăm muối trong X?
a, \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
b, \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Zn}=0,2\left(mol\right)\Rightarrow V_{H_2}=0,2.22,4=4,48\left(l\right)\)
c, \(n_{ZnCl_2}=n_{Zn}=0,2\left(mol\right)\Rightarrow m_{ZnCl_2}=0,2.136=27,2\left(g\right)\)
d, \(n_{HCl}=2n_{Zn}=0,4\left(mol\right)\Rightarrow m_{HCl}=0,4.36,5=14,6\left(g\right)\)
\(\Rightarrow m_{ddHCl}=\dfrac{14,6}{7,3\%}=200\left(g\right)\)
⇒ m dd sau pư = 13 + 200 - 0,2.2 = 212,6 (g)
\(\Rightarrow C\%_{ZnCl_2}=\dfrac{27,2}{212,6}.100\%\approx12,79\%\)
Đúng 3
Bình luận (0)
Cho 6,5 gam Zn tác dụng hết với dung dịch axit HCl thu được muối ZnCl2 và thoát ra V lít khí H2 (đktc).
a) Viết phương trình hóa học xảy ra.
b) Tính thể tích khí H2 (đktc)
Đánh máy giúm nha
a, \(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
PTHH: Zn + 2HCl ----> ZnCl2 + H2
Mol: 0,1 0,1
b, \(V_{H_2}=0,1.22,4=2,24\left(l\right)\)
Đúng 1
Bình luận (0)
Cho 150gam CaCO3 tác dụng vừa đủ với dung dịch HCl,sau phản ứng thu được 500ml dung dịch X và V lít khí CO2(đktc) a)Viết PTHH xảy ra và tính V b)Tính nồng độ mol của chất có trong dung dịch X
\(n_{CaCO_3}=\dfrac{150}{100}=1.5\left(mol\right)\)
\(CaCO_3+2HCl\rightarrow CaCl_2+CO_2+H_2O\)
\(n_{CaCl_2}=n_{CO_2}=n_{CaCO_3}=1.5\left(mol\right)\)
\(V_{CO_2}=1.5\cdot22.4=33.6\left(l\right)\)
\(C_{M_{CaCl_2}}=\dfrac{1.5}{0.5}=3\left(M\right)\)
Đúng 3
Bình luận (0)
Hoà tan 8,1 gam Al cần dùng vừa đủ dung dịch HCl 7,3% thu được dung dịch X và thấy thoát ra V lít khí H2 (ở đktc) a,viết phương trình phản ứng hoá học b,tính giá trị của V c,tính khối lượng muối thu được ? d,tính nồng độ phần trăm muối trong X?
a) $2Al + 6HCl \to 2AlCl_3 + 3H_2$
b) n Al = 8,1/27 = 0,3(mol)
Theo PTHH :
n H2 = 3/2 n Al = 0,45(mol)
V H2 = 0,45.22,4 = 10,08(lít)
c) n AlCl3 = n Al = 0,3(mol)
m AlCl3 = 0,3.133,5 = 40,05(gam)
d) n HCl = 3n Al = 0,9(mol)
m dd HCl = 0,9.36,5/7,3% = 450(gam)
Sau phản ứng :
m dd = 8,1 + 450 -0,45.2 = 457,2(gam)
C% AlCl3 = 40,05/457,2 .100% = 8,76%
Đúng 2
Bình luận (0)
Cho 6,5g Zn tác dụng vừa đủ với 200ml dung dịch HCl thoát thấy ra V lít khí H2(đktc). Cô cạn dung dịch sau PƯ thu được m gam muối FeCl2 khan.
Câu 44: Hòa tan hoàn toàn 2,8 gam Fe cần dùng vừa đủ dung dịch axit HCl 7,3% thu được dung dịch muối X và thấy thoát ra V lít khí H2 (ở đktc)
a. Tính giá trị của V?
c. Tính khối lượng dung dịch axit HCl đã phản ứng?
c. Tính nồng độ phần trăm của muối trong X?
d. Lượng Hiđro thu được ở trên cho tác dụng 16 gam oxit của kim loại R(II). Xác định tên kim loại R?
Đọc tiếp
Câu 44: Hòa tan hoàn toàn 2,8 gam Fe cần dùng vừa đủ dung dịch axit HCl 7,3% thu được dung dịch muối X và thấy thoát ra V lít khí H2 (ở đktc)
a. Tính giá trị của V?
c. Tính khối lượng dung dịch axit HCl đã phản ứng?
c. Tính nồng độ phần trăm của muối trong X?
d. Lượng Hiđro thu được ở trên cho tác dụng 16 gam oxit của kim loại R(II). Xác định tên kim loại R?