cần bao nhiêu gam H2SO4 để pha chế 200ml dung dịch có pH =3

Những câu hỏi liên quan
Cần bao nhiêu gam NaOH để pha chế 250 ml dung dịch có pH = 10 ?
Khi pH = 10 thì [H+] = 1.10-10M và
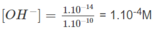
nghĩa là cần có 1. 10 - 4 mol NaOH trong 1 lít dung dịch.
Vậy trong 250 ml (0,25 lít) dung dịch cần có 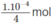 NaOH hoà tan, nghĩa là cần có
NaOH hoà tan, nghĩa là cần có
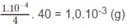 NaOH
NaOH
Đúng 0
Bình luận (0)
Cần bao nhiêu gam HCl để pha chế 400 ml dung dịch có pH=2?
A. 0,146 gam
B. 0,292 gam
C. 0,438 gam
D. 0,219 gam
Đáp án A
nHCl= nH+= 0,4.10-2 (mol), mHCl= 0,146 gam
Đúng 0
Bình luận (0)
Cần bao nhiêu gam NaOH để pha chế 300,0 ml dung dịch có pH = 10,0?
\(pH=14+log\left[OH^-\right]=10\)
\(\Rightarrow\left[OH^-\right]=10^{-4}\)
\(n_{NaOH}=10^{-4}\cdot0.3=3\cdot10^{-5}\left(mol\right)\)
\(m_{NaOH}=3\cdot10^{-5}\cdot40=1.2\cdot10^{-3}\left(g\right)\)
Đúng 2
Bình luận (0)
\([H^+] = 10^{-pH} = 10^{-10} M\\ \Rightarrow C_{M_{NaOH}} = [OH^-] = \dfrac{10^{-14}}{10^{-10}}= 10^{-4}M\\ \Rightarrow n_{NaOH} = 10^{-4}.0,3 = 3.10^{-5}(mol)\\ m_{NaOH} = 3.10^{-5}.40 = 1,2.10^{-3}(gam)\)
Đúng 2
Bình luận (0)
Cần thêm bao nhiêu ml dung dịch H2SO4 có pH 3 vào 200ml dung dịch HNO3 0,04M để thu được dung dịch có pH 2,5? A. 3,407 lít B. 4,407 lít C. 2,407 lít D. 2,050 lít
Đọc tiếp
Cần thêm bao nhiêu ml dung dịch H2SO4 có pH = 3 vào 200ml dung dịch HNO3 0,04M để thu được dung dịch có pH = 2,5?
A. 3,407 lít
B. 4,407 lít
C. 2,407 lít
D. 2,050 lít
Đáp án A
Gọi thể tích dung dịch H2SO4 cần thêm là V lít
nH+ = V.10-3 + 0,2.0,04 (mol)
[H+] = nH+/ Vdd = ( V.10-3 + 0,2.0,04)/ (V+ 0,2) = 10-2,5
Giải ra V = 3,407 lít
Đúng 0
Bình luận (0)
Tính khối lượng dung dịch H2SO4 40% cần dùng để pha chế được 200ml dung dịch H2SO4 2M
Theo đề bài ta có
Vdd=200ml=0,2 l
Số mol của dung dịch H2SO4 có hòa tan trong 200ml dung dịch H2SO4 2M là :
nH2SO4=CM.V=2.0,2=0,4 mol
\(\Rightarrow\) mct=mH2SO4=0,4.98=39,2 g
\(\Rightarrow\) Khối lượng dung dịch H2SO4 40% cần dùng là :
mdd=\(\dfrac{mct.100\%}{C\%}=\dfrac{39,2.100\%}{40\%}=98g\)
Vậy cần 98g dung dịch H2SO4 40% để pha chế được 200ml dung dịch H2SO4 2M
Đúng 0
Bình luận (0)
Ta có: \(V_{ddH_2SO_4}=200\left(ml\right)=0,2\left(l\right)\)
=> \(n_{H_2SO_4}=V_{ddH_2SO_4}.C_{MddH_2SO_4}=0,2.2=0,4\left(mol\right)\)
=> \(m_{H_2SO_4}=0,4.98=39,2\left(g\right)\)
Đúng 0
Bình luận (1)
Cần lấy bao nhiêu gam dung dịch NaCl 4% và bao nhiêu gam dung dịch NaCl 12% để pha chế 100g dung dịch NaCl 10%
Gọi: a, b lần lượt là khối lượng dung dịch NaCl (4%) và NaCl (12%)
Ta có :
\(m_{dd_{NaCl\left(10\%\right)}}=a+b=100\left(g\right)\left(1\right)\)
\(m_{NaCl\left(10\%\right)}=100\cdot10\%=10\left(g\right)\)
\(m_{NaCl\left(4\%\right)}=0.04a\left(g\right)\)
\(m_{NaCl\left(12\%\right)}=0.12b\left(g\right)\)
\(\Rightarrow0.04a+0.12b=10\left(2\right)\)
\(\left(1\right),\left(2\right):a=25,b=75\)
Đúng 2
Bình luận (0)
cần lấy bao nhiêu dung dịch H2SO4 74% ( d= 1,664g/ml) để pha chế thành 250 gam dung dich H2SO4 20%
\(n_{H_2SO_4}=\dfrac{250.20\%}{98.1005}\approx0,51\left(mol\right)\)
\(m_{H_2SO_4}=0,51.98=49,98\left(g\right)\)
\(m_{dd\left(bd\right)}=\dfrac{49,98.100\%}{74\%}=67,54\left(g\right)\)
\(V_{dd\left(bd\right)}=\dfrac{67,54}{1,664}\approx40,58\left(ml\right)\)
Đúng 0
Bình luận (0)
Để pha chế 500g dung dịch CuSO4 16% cần phải lấy bao nhiêu gam dung dịch CuSO4 8% và bao nhiêu gam tinh thể CuSO4 5H2O
mCuSO4=16%.500= 80(g)
Gọi x,y là KL dd CuSO4 8% và tinh thế CuSO4.5H2O cần lấy (x>0)
m(CuSO4)= 0,08x+ 16/25y
<=>0,08x+ 0,64y= 80 (1)
Mặt khác vì KL dung dịch CuSO4 16% là 500 gam nên: x+y=500 (2)
Từ (1), (2) ta có hpt:
\(\left\{{}\begin{matrix}0,08x+0,64y=80\\x+y=500\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=\dfrac{3000}{7}\\y=\dfrac{500}{7}\end{matrix}\right.\)
Vậy để pha chế 500 gam dd CuSO4 16% thì cần 3000/7 (g) dd CuSO4 8% và 500/7 (g) tinh thể CuSO4.5H2O.
Đúng 2
Bình luận (1)
Cần lấy bao nhiêu gam kali clorua và bao nhiêu gam dung dịch kali clorua 4% để pha chế thành 480gam dung dịch kali clorua 20%.

















