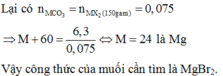a) Hòa tan một lượng muối CO3 của một kim loại hóa trị II bằng dung dịch H2SO4 14,7%. Sau khi kết thúc phản ứng, khí không còn thoát ra nữa thì còn lại dung dịch 175 muối sunfat. Xác định nguyên tử khối của kim loại.
b) Lấy 40g dung dịch bão hòa của muối FeCl2, thêm vào đó 10g muối FeCl2 khan. Đun nóng để hòa tan hết. Khi để nguội đến khối lượng ban đầu thì lắng xuống 23,4g muối tinh thể hidrat. Xác định công thức của tinh thể biết rằng dung dịch bão hòa chứa 38,5% muối khan.
















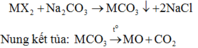
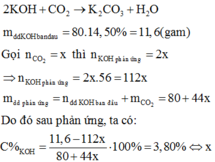 = 0,75
= 0,75