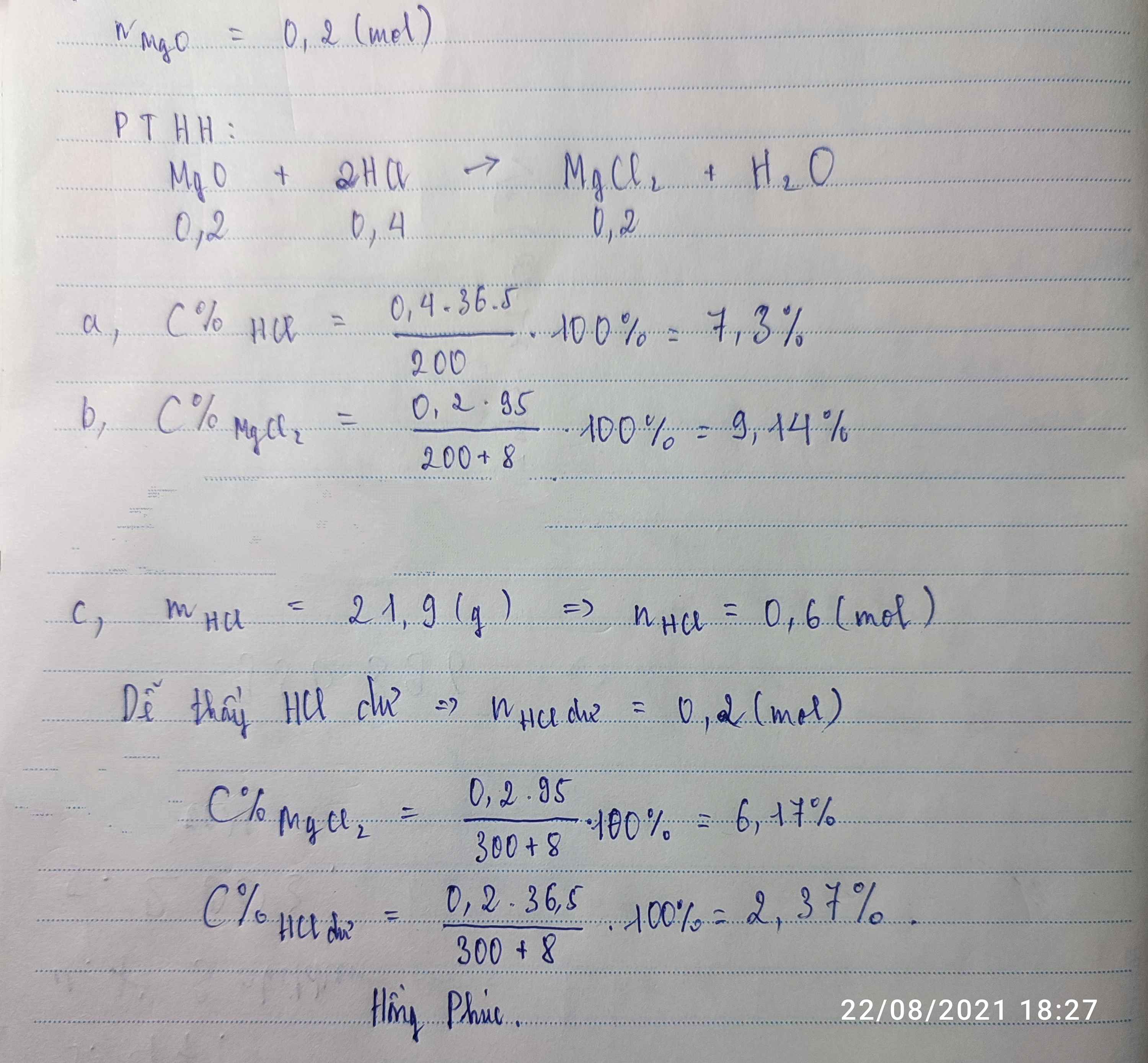Hòa tan 16 g sắt (III) oxit vào 400 g dd HCl 7,3%. Tính nồng độ của chất tan trong dung dịch sau phản ứng.

Những câu hỏi liên quan
Hòa tan 16 g sắt (III) oxit vào 400 g dd HCl 7,3%. Tính nồng độ của chất tan trong dung dịch sau phản ứng.VIẾT PTPU.CÁC BẠN GHI RÕ GIÚP MÌNH.
\(n_{Fe2O3}=\dfrac{16}{160}=0,1\left(mol\right)\)
\(m_{ct}=\dfrac{7,3.400}{100}=29,2\left(g\right)\)
\(n_{HCl}=\dfrac{29,2}{36,5}=0,8\left(mol\right)\)
Pt : \(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O|\)
1 6 2 3
0,1 0,8 0,2
Lập tỉ số so sánh : \(\dfrac{0,1}{1}< \dfrac{0,8}{6}\)
⇒ Fe2O3 phản ứng hết , HCl dư
⇒ Tính toán dựa vào số mol của Fe2O3
\(n_{FeCl3}=\dfrac{0,1.2}{1}=0,2\left(mol\right)\)
⇒ \(m_{FeCl3}=0,2.162,5=32,5\left(g\right)\)
\(n_{HCl\left(dư\right)}=0,8-\left(0,1.6\right)=0,2\left(mol\right)\)
⇒ \(m_{HCl\left(dư\right)}=0,2.36,5=7,3\left(g\right)\)
\(m_{ddspu}=16+400=416\left(g\right)\)
\(C_{FeCl3}=\dfrac{32,5.100}{416}=7,8125\)0/0
\(C_{HCl\left(dư\right)}=\dfrac{7,3.100}{416}=1,75\)0/0
Chúc bạn học tốt
Đúng 1
Bình luận (0)
11. Hòa tan hoàn toàn 8 gam sắt (III) oxit trong 150ml dung dịch HCl 2M. Tính nồng độ mol chất tan có trong dung dịch sau phản ứng (giả sử thể tích dd sau phản ứng không đổi).
$n_{CuO} = \dfrac{8}{80} = 0,1(mol) ; n_{HCl} = 0,15.2 = 0,3(mol)$
$CuO + 2HCl \to CuCl_2 + H_2O$
Ta thấy :
$n_{CuO} : 1 < n_{HCl} : 2$ nên HCl dư
$n_{CuCl_2} = n_{CuO} = 0,1(mol)$
$n_{HCl\ pư} = 2n_{CuO} = 0,2(mol) \Rightarrow n_{HCl\ dư} = 0,3 - 0,2 = 0,1(mol)$
$C_{M_{CuCl_2}} = \dfrac{0,1}{0,15} = 0,67M$
$C_{M_{HCl}} = \dfrac{0,1}{0,15} = 0,67M$
Đúng 2
Bình luận (1)
Hòa tan hoàn toàn 16g sắt (III) oxit trong m (g)
dung dịch HCl 7,3%.
a)Tính khối lượng dung dịch HCl đã phản ứng.
b) Tính C% muối trong dung dịch sau phản ứng.
\(n_{Fe2O3}=\dfrac{16}{160}=0,1\left(mol\right)\)
Pt : \(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O|\)
1 6 2 3
0,1 0,6 0,2
a) \(n_{HCl}=\dfrac{0,1.6}{1}=0,6\left(mol\right)\)
\(m_{HCl}=0,6.36,5=21,9\left(g\right)\)
\(m_{ddHCl}=\dfrac{21,9.100}{7,3}=300\left(g\right)\)
b) \(n_{FeCl3}=\dfrac{0,6.2}{6}=0,2\left(mol\right)\)
⇒ \(m_{FeCl3}=0,2.162,5=32,5\left(g\right)\)
\(m_{ddspu}=16+300=316\left(g\right)\)
\(C_{FeCl3}=\dfrac{32,5.100}{316}=10,28\)0/0
Đúng 3
Bình luận (0)
Thả 11,2 gam sắt vào dung dịch HCl 7,3%. a. Tính khối lượng dung dịch axit tối thiểu cần dùng để hòa tan hết lượng sắt trên b. Tính khối lượng muối tạo thành sau phản ứng. c.Tính nồng độ phần trăm của dung dịch muối sau phản ứng nếu lượng axit tham gia phản ứng vừa đủ. d. Cho 11,2 gam sắt vào 300 gam dung dịch HCl 7,3%. Hỏi sau phản ứng, dung dịch có những chất gì? Nồng độ phần trăm của mỗi chất là bao nhiêu?
Đọc tiếp
Thả 11,2 gam sắt vào dung dịch HCl 7,3%.
a. Tính khối lượng dung dịch axit tối thiểu cần dùng để hòa tan hết lượng sắt trên
b. Tính khối lượng muối tạo thành sau phản ứng.
c.Tính nồng độ phần trăm của dung dịch muối sau phản ứng nếu lượng axit tham gia phản ứng vừa đủ.
d. Cho 11,2 gam sắt vào 300 gam dung dịch HCl 7,3%. Hỏi sau phản ứng, dung dịch có những chất gì? Nồng độ phần trăm của mỗi chất là bao nhiêu?
Thả 11,2 gam sắt vào dung dịch HCl 7,3%. a. Tính khối lượng dung dịch axit tối thiểu cần dùng để hòa tan hết lượng sắt trên b. Tính khối lượng muối tạo thành sau phản ứng. c.Tính nồng độ phần trăm của dung dịch muối sau phản ứng nếu lượng axit tham gia phản ứng vừa đủ. d. Cho 11,2 gam sắt vào 300 gam dung dịch HCl 7,3%. Hỏi sau phản ứng, dung dịch có những chất gì? Nồng độ phần trăm của mỗi chất là bao nhiêu?
Đọc tiếp
Thả 11,2 gam sắt vào dung dịch HCl 7,3%.
a. Tính khối lượng dung dịch axit tối thiểu cần dùng để hòa tan hết lượng sắt trên
b. Tính khối lượng muối tạo thành sau phản ứng.
c.Tính nồng độ phần trăm của dung dịch muối sau phản ứng nếu lượng axit tham gia phản ứng vừa đủ.
d. Cho 11,2 gam sắt vào 300 gam dung dịch HCl 7,3%. Hỏi sau phản ứng, dung dịch có những chất gì? Nồng độ phần trăm của mỗi chất là bao nhiêu?
Số mol của sắt
nFe = \(\dfrac{m_{Fe}}{M_{Fe}}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
Pt : Fe + 2HCl → FeCl2 + H2\(|\)
1 2 1 1
0,2 0,4 0,2 0,2
a) Số mol của axit clohidric
nHCl = \(\dfrac{0,2.2}{1}=0,4\left(mol\right)\)
Khối lượng của axit clohidric
mHCl= nHCl . MHCl
= 0,4 . 36,5
= 14,6 (g)
Khối lượng của dung dịch axit clohidric cần dùng
C0/0HCl = \(\dfrac{m_{ct}.100}{m_{dd}}\Rightarrow m_{dd}=\dfrac{m_{ct}.100}{C}=\dfrac{14,6.100}{7,3}=200\left(g\right)\)
b) Số mol của muối sắt (II) clorua
nFeCl2 = \(\dfrac{0,4.1}{2}=0,2\left(mol\right)\)
Khối lượng của sắt (II) clorua
mFeCl2= nFeCl2 . MFeCl2
= 0,2 . 127
= 25,4 (g)
Khối lượng của dung dịch sau phản ứng
mdung dịch sau phản ứng = mFe + mHCl - mH2
= 11,2 + 200 - ( 0,2 .2)
= 210,8 (g)
c) Nồng độ phần trăm của muối sắt (II) clorua
C0/0FeCl2 = \(\dfrac{m_{ct}.100}{m_{dd}}=\dfrac{25,4.100}{210,8}=12,05\)0/0
d) Số mol của sắt
nFe = \(\dfrac{m_{Fe}}{M_{Fe}}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
Khối lượng của axit clohidric
C0/0HCl = \(\dfrac{m_{ct}.100}{m_{dd}}\Rightarrow m_{ct}=\dfrac{C.m_{dd}}{100}=\dfrac{7,3.300}{100}=21,9\left(g\right)\)
Số mol của axit clohidric
nHCl = \(\dfrac{m_{HCl}}{M_{HCl}}=\dfrac{21,9}{36,5}=0,6\left(mol\right)\)
Pt : Fe + 2HCl → FeCl2 + H2\(|\)
1 2 1 1
0,2 0,6 0,3 0,3
Lập tỉ số so sánh : \(\dfrac{0,2}{1}< \dfrac{0,6}{2}\)
⇒ Fe phản ứng hết , HCl dư
⇒ Tính toán dựa vào số mol của Fe
Sau phản ứng thu được muối FeCl2 và dung dịch HCl còn dư
Số mol của sắt (II) clorua
nFeCl2 = \(\dfrac{0,6.1}{2}=0,3\left(mol\right)\)
Khối lượng của sắt (II) clorua
mFeCl2 = nFeCl2 . MFeCl2
= 0,3 . 127
= 38,1 (g)
Số mol dư của dung dịch axit clohidric
ndư = nban đầu - nmol
= 0,6 - (0,2 . 2)
= 0,2 (mol)
Khối lượng dư của dung dịch axit clohidric
mdư = ndư. MHCl
= 0,2 . 36,5
= 7,3 (g)
Khối lượng của dung dịch sau phản ứng
mdung dịch sau phản ứng = mFe + mHCl - mH2
= 11,2 + 300 - (0,3 . 2)
= 310,6 (g)
Nồng độ phần trăm của sắt (II) clorua
C0/0FeCl2 = \(\dfrac{m_{ct}.100}{m_{dd}}=\dfrac{38,1.100}{310,6}=12,27\)0/0
Nồng độ phần trăm của dung dịch axit clohdric
C0/0HCl = \(\dfrac{m_{ct}.100}{m_{dd}}=\dfrac{7,3.100}{310,6}=2,35\)0/0
Chúc bạn học tốt
Đúng 1
Bình luận (0)
Hòa tan 32g sắt (III) oxit vào 218g dd HCl 30%. Tính nồng độ C% của các chất trong dd sau pư
Số mol của sắt (III) oxit
nFe2O3 = \(\dfrac{m_{Fe2O3}}{M_{Fe2O3}}=\dfrac{32}{160}=0,2\left(mol\right)\)
Khối lượng của axit clohidric
C0/0HCl = \(\dfrac{m_{ct}.100}{m_{dd}}\Rightarrow m_{ct}=\dfrac{C.m_{dd}}{100}=\dfrac{30.218}{100}=65,4\left(g\right)\)
Số mol của axit clohidric
nHCl = \(\dfrac{m_{HCl}}{M_{HCl}}=\dfrac{65,4}{36,5}=1,8\left(mol\right)\)
Pt : Fe2O3 + 6HCl → 2FeCl3 + 3H2O\(|\)
1 6 2 3
0,2 1,8 0,4
Lập tỉ số so sánh : \(\dfrac{0,2}{1}< \dfrac{1,8}{6}\)
⇒ Fe2O3 phản ứng hết , HCl dư
⇒ Tính toán dựa vào số mol của Fe2O3
Số mol của sắt (III) clorua
nFeCl3 = \(\dfrac{0,2.2}{1}=0,4\left(mol\right)\)
Khối lượng của sắt (III) clorua
mFeCl3 = nFeCl3 . MFeCl3
= 0,4. 162,5
= 65 (g)
Số mol dư của dung dịch axit clohidric
ndư= nban đầu -nmol
= 1,8 - \(\left(\dfrac{0,2.6}{1}\right)\)
= 0,6 (mol)
Khối lượng dư của dung dịch axit clohidric
mdư = ndư . MHCl
= 0,6 . 36,5
= 21,9 (g)
Khối lượng của dung dịch sau hản ứng
mdung dịch sau phản ứng = mFe2O3 + mHCl
= 32 + 218
= 250 (g)
Nồng độ phần trăm của sắt (III) clorua
C0/0FeCl3 = \(\dfrac{m_{ct}.100}{m_{dd}}=\dfrac{65.100}{250}=26\)0/0
Nồng độ phần trăm của dung dịch axit clohidric
C0/0HCl = \(\dfrac{m_{ct}.100}{m_{dd}}=\dfrac{21,9.100}{250}=8,76\)0/0
Chúc bạn học tốt
Đúng 1
Bình luận (0)
Hòa tan 35,3g hỗn hợp MgO, Al½O3 vào 950g dung dịch HCl 7,3% thu được dung dịch A. Tính a/ Phần trăm khối lượng mỗi oxit? b/ Nồng độ % các chất sau phản ứng?
a) \(\%m_{MgO}=56,66\%\)
\(\%m_{Al_2O_3}=43,34\%\)
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn 8g MgO vào 200 g dd HCl vừa đủ tạo dd A.a)Tính C% của dd HCl đã dùng. b)Tính C% của dd tạo thành sau phản ứng.c)Nếu đem hòa tan lượng MgO ở trên trong 300g dung dịch HCl 7,3%. Tìm C% của các chất có trong dung dịch A.Hòa tan hoàn toàn 8g MgO vào 200 g dd HCl vừa đủ tạo dd A.a)Tính C% của dd HCl đã dùng. b)Tính C% của dd tạo thành sau phản ứng.c)Nếu đem hòa tan lượng MgO ở trên trong 300g dung dịch HCl 7,3%. Tìm C% của các chất có trong dung dịch A.
Đọc tiếp
Hòa tan hoàn toàn 8g MgO vào 200 g dd HCl vừa đủ tạo dd A.
a)Tính C% của dd HCl đã dùng. b)Tính C% của dd tạo thành sau phản ứng.
c)Nếu đem hòa tan lượng MgO ở trên trong 300g dung dịch HCl 7,3%. Tìm C% của các chất có trong dung dịch A.Hòa tan hoàn toàn 8g MgO vào 200 g dd HCl vừa đủ tạo dd A.
a)Tính C% của dd HCl đã dùng. b)Tính C% của dd tạo thành sau phản ứng.
c)Nếu đem hòa tan lượng MgO ở trên trong 300g dung dịch HCl 7,3%. Tìm C% của các chất có trong dung dịch A.
Cho 16 g sắt (III) oxit vào 73 g dd axit clohiđric 10% thu được dung dịch A.
a. Tính khối lượng muối sắt được tạo thành.
b. Dung dịch A có chất tan gì? Tính nồng độ phần trăm của dung dịch A.
\(n_{Fe_2O_3}=\dfrac{16}{160}=0,1\left(mol\right)\\ n_{HCl}=\dfrac{73.10\%}{36,5}=0,2\left(mol\right)\\ Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\\ Vì:\dfrac{0,1}{1}>\dfrac{0,2}{6}\\ \Rightarrow Fe_2O_3dư\\ a.Muối.tạo.thành:FeCl_3\\ n_{FeCl_3}=\dfrac{2}{6}.0,2=\dfrac{1}{15}\left(mol\right)\\ m_{FeCl_3}=\dfrac{1}{15}.162,5=\dfrac{65}{6}\left(g\right)\\ b.Chất.tan.ddA:FeCl_3\\ m_{ddFeCl_3}=m_{Fe_2O_3\left(p.ứ\right)}+m_{ddHCl}=\dfrac{1}{6}.0,2.160+73=\dfrac{235}{3}\left(g\right)\\ C\%_{ddFeCl_3}=\dfrac{\dfrac{65}{6}}{\dfrac{235}{3}}.100=13,83\%\)
Đúng 1
Bình luận (0)