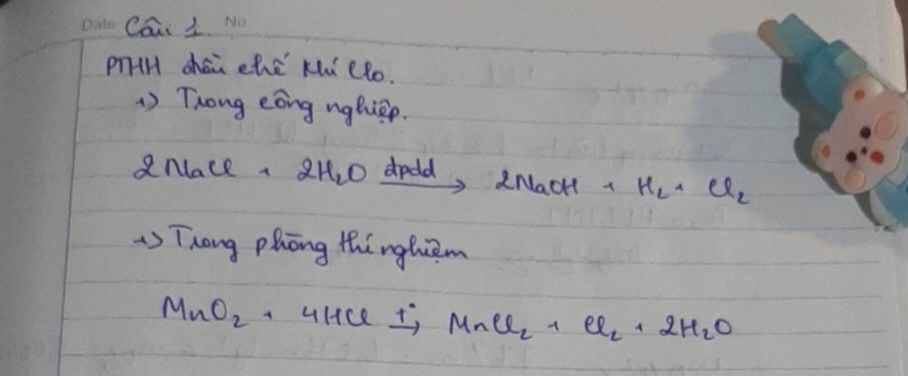Phương pháp điều chế khí Clo....PTHH minh họa

Những câu hỏi liên quan
Nêu phương pháp và vẽ hình mô tả quá trình điều chế khí clo trong phòng thí nghiệm? Viết phương trình hóa học minh họa và giải thích quá trình để thu được khí clo tinh khiết.
- Phương pháp điều chế clo trong phòng thí nghiệm: Đun nóng nhẹ dung dịch HCl đậm đặc với chất oxi hóa mạnh như MnO2 (hoặc KMnO4).
MnO2 + 4HCl \(\underrightarrow{t^o}\) MnCl2 + Cl2 + 2H2O
Để thu được khí clo tinh khiết:
- Bình H2SO4 đặc có tác dụng làm khô khí clo.
- Clo nặng hơn không khí Þ Thu bằng cách đẩy không khí.
- Bông tẩm xút: tránh để clo độc bay ra ngoài.
Đúng 0
Bình luận (0)
Làm sao để điều chế Clo. Viết 3 PTHH minh họa !!!
2NaCl + 2H2O \(\underrightarrow{đpddcmn}\) 2NaOH + H2 + Cl2
2NaCl \(\underrightarrow{đpnc}\) 2Na + Cl2
MnO2 + 4HCl \(\rightarrow\) MnCl2 + 2H2O + Cl2
Đúng 0
Bình luận (0)
Chúng ta có thể điều chế clo bằng cách cho những chất có tính oxi hóa mạnh tác dụng với hợp chất của clo
VD: 6HCl+KClO3→3Cl2+3H2O+KCl
4HCl+MnO2→Cl2+2H2O+MnCl2
16HCl+2KMnO4→5Cl2+8H2O+2KCl+2MnCl2
Đúng 0
Bình luận (0)
Nêu nguyên tắn điều chế khí clo trog phòng TN . Viết PTHH điều chế khí clo trong phòng TN ( ghi rõ điều kiện ) để minh họa .
Phương pháp điều chế khí clo trong công nghiệp là
A. điện phân dung dịch NaCl có màng ngăn xốp
B. điện phân dung dịch NaCl
C. điện phân dung dịch KCl có màng ngăn
D. cho HCl tác dụng với chất oxi hóa mạnh
Phương pháp điều chế khí clo trong công nghiệp là A. Cho HCl tác dụng với chất oxi hóa mạnh B. Nhiệt phân muối clorua kém bền C. Điện phân dung dịch NaCl, màng ngăn xốp D. Điện phân nóng chảy muối clorua
Đọc tiếp
Phương pháp điều chế khí clo trong công nghiệp là
A. Cho HCl tác dụng với chất oxi hóa mạnh
B. Nhiệt phân muối clorua kém bền
C. Điện phân dung dịch NaCl, màng ngăn xốp
D. Điện phân nóng chảy muối clorua
Phương pháp điều chế Cl2 trong công nghiệp: Điện phân dung dịch NaCl màng ngăn xốp:
2NaCl + 2H2O → 2NaOH + Cl2 + H2.
Đúng 0
Bình luận (0)
Nêu nguyên liệu vào PTHH điều chế hidro trong PTN? phương pháp thu khí Hidro?
Nguyên liệu: kim loại Al, Zn, Mg, Pb,... và ddaxit HCl, H2SO4 loãng
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\\ Zn+2HCl\rightarrow ZnCl_2+H_2\\ Mg+H_2SO_4\rightarrow MgSO_4+H_2\\ Pb+H_2SO_4\rightarrow PbSO_4+H_2\)
Đúng 4
Bình luận (0)
Viết PTHH điều chế khí Clo trong công nghiệp và trong phòng thí nghiệm
Nêu nguyên liệu dùng để điều chế oxi, hidro trong phòng thí nghiệm. Viết pthh minh họa? Nguyên liệu dùng để điều chế oxi trong phòng thí nghiệm phải có đặc điểm gì? Không khí có thành phần như thế nào? Có thể thu khí oxi và hidro bằng những cách nào, tại sao?
Đọc tiếp
Nêu nguyên liệu dùng để điều chế oxi, hidro trong phòng thí nghiệm. Viết pthh minh họa? Nguyên liệu dùng để điều chế oxi trong phòng thí nghiệm phải có đặc điểm gì? Không khí có thành phần như thế nào? Có thể thu khí oxi và hidro bằng những cách nào, tại sao?
Câu 1. Trình bày tính chất vật lý, ứng dụng, tính chất hóa học của Oxi và viết PTHH minh họa.Câu 2. Trình bày phương pháp điều chế (nguyên tắc, PTHH) và thu khí oxi trong PTN.Câu 3. Cho biết công thức tổng quát, phân loại và cách gọi tên Oxit.Câu 4. Trình bày tính chất vật lý, ứng dụng, tính chất hóa học của hiđro và viết PTHH minh họa.Câu 5. Trình bày phương pháp điều chế (nguyên tắc, PTHH) và thu khí hidro trong PTN.Câu 6. Thế nào là phản ứng phân hủy? Phản ứng hóa hợp? Phản ứng thế? Viết phươ...
Đọc tiếp
Câu 1. Trình bày tính chất vật lý, ứng dụng, tính chất hóa học của Oxi và viết PTHH minh họa.
Câu 2. Trình bày phương pháp điều chế (nguyên tắc, PTHH) và thu khí oxi trong PTN.
Câu 3. Cho biết công thức tổng quát, phân loại và cách gọi tên Oxit.
Câu 4. Trình bày tính chất vật lý, ứng dụng, tính chất hóa học của hiđro và viết PTHH minh họa.
Câu 5. Trình bày phương pháp điều chế (nguyên tắc, PTHH) và thu khí hidro trong PTN.
Câu 6. Thế nào là phản ứng phân hủy? Phản ứng hóa hợp? Phản ứng thế? Viết phương trình hóa học minh họa.
Câu 1 tính chất vật lý : ko màu ko mù vị , ít tan trong nước , nặng hơn kk
. hóa lỏng ở -183oC có màu xanh nhạt
tính chất hóa học : rất hoát động ở nhiệt độ cao . có thể tác dụng với phi kim , kim loại và hợp chất
VD :td với phi kim S+O2 -t--> SO2
VD :td với kim loại 3Fe+ 2O2 -t---> Fe3O4
bài 2 :
- thu khí O2 ở bằng cách đun nóng nhuengx hợp chất giàu O2 và dễ bị phân hủy như KMnO4 . KClO3
pthh : 2KMnO4 --t--> K2MnO4 + MnO2 + O2
- thu khí oxi bằng cách đẩy kk và đẩy nước
bài 3
dạng tổng quát : M2Ox ( M là đơn chất )
- cách gọi tên : tên nguyên tố +oxit
Đúng 3
Bình luận (0)
Câu 1 tính chất vật lý : ko màu ko mù vị , ít tan trong nước , nặng hơn kk
. hóa lỏng ở -183oC có màu xanh nhạt
tính chất hóa học : rất hoát động ở nhiệt độ cao . có thể tác dụng với phi kim , kim loại và hợp chất
VD :td với phi kim S+O2 -t--> SO2
VD :td với kim loại 3Fe+ 2O2 -t---> Fe3O4
bài 2 :
- thu khí O2 ở bằng cách đun nóng nhuengx hợp chất giàu O2 và dễ bị phân hủy như KMnO4 . KClO3
pthh : 2KMnO4 --t--> K2MnO4 + MnO2 + O2
- thu khí oxi bằng cách đẩy kk và đẩy nước
bài 3
dạng tổng quát : M2Ox ( M là đơn chất )
- cách gọi tên : tên nguyên tố +oxit
Đúng 0
Bình luận (0)