hòa tan hỗn hợp kim loại gồm Mg và Al có khối lượng bằng nhau vào dd HCl (lấy dư) sau phản ứng thu được 19,6 lít khí Hiđro (đktc). Xác định khối lượng hỗn hợp kim loại đã hòa tan vào dd HCl.

Những câu hỏi liên quan
Hòa tan hoàn toàn 1,04 gam hỗn hợp A gồm hai kim loại Fe, Mg bằng một lượng vừa đủ dung dịch HCl 0,1M. Sau phản ứng thu được 0,672 lít khí H2 (đktc) a. Tính khối lượng mỗi kim loại trong hỗn hợp A b.Tính thể tích dung dịch HCl đã dùng (biết dùng dư 10%).
Đọc tiếp
Hòa tan hoàn toàn 1,04 gam hỗn hợp A gồm hai kim loại Fe, Mg bằng một lượng vừa đủ dung dịch HCl 0,1M. Sau phản ứng thu được 0,672 lít khí H2 (đktc)
a. Tính khối lượng mỗi kim loại trong hỗn hợp A
b.Tính thể tích dung dịch HCl đã dùng (biết dùng dư 10%).
a) Gọi số mol Fe, Mg là a, b (mol)
=> 56a + 24b = 1,04 (1)
\(n_{H_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
a--->2a-------------->a
Mg + 2HCl --> MgCl2 + H2
b---->2b------------->b
=> a + b = 0,03 (2)
(1)(2) => a = 0,01 (mol); b = 0,02 (mol)
mFe = 0,01.56 = 0,56 (g)
mMg = 0,02.24 = 0,48 (g)
b) nHCl(lý thuyết) = 2a + 2b = 0,06 (mol)
=> \(n_{HCl\left(tt\right)}=\dfrac{0,06.110}{100}=0,066\left(mol\right)\)
=> \(V_{dd.HCl\left(tt\right)}=\dfrac{0,066}{0,1}=0,66\left(l\right)\)
Đúng 1
Bình luận (0)
khi hòa tan 6g hỗn hợp các kim loại gồm đồng ,sắt,nhôm trong axit clohidric dư thì tạo thành 3,024l hidro (đktc) và còn lại 1,86g kim loại không tan .Biết đồng không tham gia phản ứnga) viết pt phản ứngb)xác định thành phần % khối lượng mỗi kim loại trong hỗn hợpc) tính khối lượng axit đã tham gia phản ứng và khối lượng của các muối clorua tạo thành
Đọc tiếp
khi hòa tan 6g hỗn hợp các kim loại gồm đồng ,sắt,nhôm trong axit clohidric dư thì tạo thành 3,024l hidro (đktc) và còn lại 1,86g kim loại không tan .Biết đồng không tham gia phản ứng
a) viết pt phản ứng
b)xác định thành phần % khối lượng mỗi kim loại trong hỗn hợp
c) tính khối lượng axit đã tham gia phản ứng và khối lượng của các muối clorua tạo thành
số mol của HCl là 2x và 3y sao bạn ko nhân cho 2 và 3
Đúng 0
Bình luận (0)
) Hòa tan hoàn toàn 10,2 gam hỗn hợp A gồm hai kim loại Fe, Mg bằng một lượng vừa đủ dung dịch HCl 0.1M. Sau phản ứng thu được 7,84 lít khí H2 (đktc)
a. Tính khối lượng mỗi kim loại trong hỗn hợp A
b.Tính thể tích dung dịch HCl đã dùng.
Fe+2HCl->Fecl2+H2
x-----2x-----------------x
Mg+2Hcl->MgCl2+h2
y-------2y----------------y
a)
ta có :\(\left\{{}\begin{matrix}56x+24y=10,2\\x+y=0,35\end{matrix}\right.\)
=>x=0,05625 , y=0,29375
=>m Fe=0,05625.56=3,15g
=>m Mg=7,05g
=>VHCl=\(\dfrac{0,05625.2+0,29375.2}{0,1}\)=7l=7000ml
Đúng 1
Bình luận (0)
Hỗn hợp A gồm các kim loại Mg, Al, Fe.Lấy 14,7 gam hỗn hợp A cho tác dụng với dung dịch NaOH dư, sinh ra 3,36 lít khí (đktc). Mặt khác cũng lấy 14,7 gam hỗn hợp A cho tác dụng với dung dịch HCl dư, sinh ra 10,08 lít khí (đktc) và dung dịch B. Cho dung dịch B tác dụng với dung dịch NaOH dư, lọc kết tủa tạo thành và nung nóng trong không khí đến khối lượng không đổi thu được m gam chất rắn. Tính m và tính % theo khối lượng của mỗi kim loại tron...
Đọc tiếp
Hỗn hợp A gồm các kim loại Mg, Al, Fe.
Lấy 14,7 gam hỗn hợp A cho tác dụng với dung dịch NaOH dư, sinh ra 3,36 lít khí (đktc). Mặt khác cũng lấy 14,7 gam hỗn hợp A cho tác dụng với dung dịch HCl dư, sinh ra 10,08 lít khí (đktc) và dung dịch B. Cho dung dịch B tác dụng với dung dịch NaOH dư, lọc kết tủa tạo thành và nung nóng trong không khí đến khối lượng không đổi thu được m gam chất rắn. Tính m và tính % theo khối lượng của mỗi kim loại trong hỗn hợp A.Cho hỗn hợp A tác dụng với dung dịch CuSO4 dư, sau khi phản ứng kết thúc, lọc lấy chất rắn đem hòa tan hết chất rắn trong dung dịch HNO3 loãng dư, thu được 26,88 lít khí NO (đktc). Tính khối lượng hỗn hợp A.1.1. Al + NaOH + H2O ==> NaAlO2 + 3/2H2
nH2(1)=3,36/22,4=0.15(mol)
=> nAl(1)= nH2(1):3/2= 0.15:3/2= 0.1(mol)
2.Mg + 2HCl ==> MgCl2 + H2
3.2Al + 6HCl ==> 2AlCl3 + 3H2
4.Fe + 2HCl ==> FeCl2 + H2
=> \(n_{H_2\left(2,3,4\right)}=\) 10.08/22.4= 0.45(mol)
=> nH2(3)=0.1*3/2=0.15(mol)
MgCl2 + 2NaOH ==> Mg(OH)2 + 2NaCl
AlCl3 + 3NaOH ==> Al(OH)3 + 3NaCl
FeCl2 + 2NaOH ==> Fe(OH)2 + 2NaCl
Đúng 0
Bình luận (0)
Hòa tan 16,6 gam hỗn hợp kim lọai Fe và Al cần dùng 300g dung dịch HCl, sau phản ứng thu được 11,2 lít khí H2 ở đktc
a. Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu
b. Tính nồng độ phần tram của dung dịch HCl đã dùng
a, Gọi \(\left\{{}\begin{matrix}n_{Fe}=a\left(mol\right)\\n_{Al}=b\left(mol\right)\end{matrix}\right.\)
\(n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
PTHH:
Fe + 2HCl ---> FeCl2 + H2
a--->2a------------------>a
2Al + 6HCl ---> 2AlCl3 + 3H2
b---->3b-------------------->1,5b
=> \(\left\{{}\begin{matrix}56a+27b=16,6\\a+1,5b=0,5\end{matrix}\right.\Leftrightarrow a=b=0,2\left(mol\right)\)
=> \(\left\{{}\begin{matrix}m_{Fe}=0,2.56=11,2\left(g\right)\\m_{Al}=0,2.27=5,4\left(g\right)\end{matrix}\right.\)
b) \(C\%_{HCl}=\dfrac{\left(0,2.2+0,2.3\right).36,5}{300}.100\%=12,167\%\)
Đúng 2
Bình luận (0)
\(n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
gọi nFe : a , nAl: b (a,b>0) => 56a + 27b = 16,6 (g)
\(pthh:Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
a a
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
b \(\dfrac{3b}{2}\)
=> \(a+\dfrac{3b}{2}=0,5\)
ta có hệ pt
\(\left\{{}\begin{matrix}56a+27b=16,6\\a+\dfrac{3b}{2}=0,5\end{matrix}\right.\)
=> a= 0,2 , b = 0,2
\(\left\{{}\begin{matrix}m_{Fe}=0,2.56=11,2\left(g\right)\\m_{Al}=16,6-11,2=5,4\left(g\right)\end{matrix}\right.\)
\(pthh:Fe+2HCl\rightarrow FeCl_2+H_2\)
0,2 0,4
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,2 0,6
=> \(m_{HCl}=\left(0,4+0,6\right).36,5=36,5\left(g\right)\)
=> \(C\%=\dfrac{36,5}{200}.100\%=18,25\%\)
Đúng 0
Bình luận (1)
Hỗn hợp A gồm kim loại R (hóa trị I) và kim loại X (hóa trị II). Hòa tan 23,6 gam A vào dung dịch chứa
H
N
O
3
và
H
2
S
O
4
thu được 20,2 gam hỗn hợp khí B gồm
N
O
2
và
S
O
2
(không còn sản phẩm khử khác). Biết
V
B
8,96 lít (đ...
Đọc tiếp
Hỗn hợp A gồm kim loại R (hóa trị I) và kim loại X (hóa trị II). Hòa tan 23,6 gam A vào dung dịch chứa H N O 3 và H 2 S O 4 thu được 20,2 gam hỗn hợp khí B gồm N O 2 và S O 2 (không còn sản phẩm khử khác). Biết V B = 8,96 lít (đktc). Khối lượng muối thu được là:
A. 25,9 gam
B. 51,8 gam
C. 61,4 gam
D. 5,18 gam
Hòa tan 14,8 gam hỗn hợp gồm Fe và Cu vào lượng dư dung dịch hỗn hợp HNO3 và H2SO4 đặc nóng. Sau phản ứng thu được 10,08 lít NO2 (đktc) và 2,24 lít SO2 (đktc). Khối lượng Fe trong hỗn hợp ban đầu là:
A. 5,6
B. 8,4
C. 18
D. 18,2
Đáp án B
Gọi a, b lần lượt là số mol của Fe, Cu
56a + 64b = 14,8 (1)
Quá trình nhường electron:
Fe - 3e → Fe
a 3a
Cu - 2e → Cu
b 2b
→ ∑ne nhường = (3a + 2b) mol
Quá trình nhận electron:
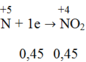
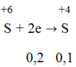
→ ∑ne nhận = 0,45 + 0,2 = 0,65 mol
Áp dụng định luật bảo toàn electron:
3a + 2b = 0,65 → a = 0,15 và b = 0,1 → mFe = 8,4 g
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 26.05g hỗn hợp Mg, Al, Fe trong dung dịch HXl dư thu được 13,44 lít khí H2 (đktc) và m gam muối . Cũng hỗn hợp trên tác dụng với clo thì thấy thể tích clo cần dùng là 17,36 lít
A. Tính khối lượng muối của từng kim loại trong hỗn hợp
B. Xác định m
\(Mg\left(x\right)+2HCl\rightarrow MgCl_2+H_2\left(x\right)\)
\(2Al\left(y\right)+6HCl\rightarrow2AlCl_3+3H_2\left(1,5y\right)\)
\(Fe\left(z\right)+2HCl\rightarrow FeCl_2+H_2\left(z\right)\)
\(Mg\left(x\right)+Cl_2\left(x\right)\rightarrow MgCl_2\)
\(2Al\left(y\right)+3Cl_2\left(1,5y\right)\rightarrow2AlCl_3\)
\(2Fe\left(z\right)+3Cl_2\left(1,5z\right)\rightarrow2FeCl_3\)
Gọi số mol của Mg, Al, Fe trong hỗn hợp lần lược là x, y, z ta có
\(24x+27y+56z=26,05\left(1\right)\)
Số mol H2: \(\frac{13,44}{22,4}=0,6\)
\(\Rightarrow x+1,5y+z=0,6\left(2\right)\)
Số mol Cl2 là: \(\frac{17,36}{22,4}=0,775\)
\(\Rightarrow x+1,5y+1,5z=0,775\left(3\right)\)
Từ (1), (2), (3) ta có hệ: \(\left\{\begin{matrix}24x+27y+56z=26,05\\x+1,5y+z=0,6\\x+1,5y+1,5z=0,775\end{matrix}\right.\)
M ra đáp số âm không biết có phải do đề sai không
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn 26.05g hỗn hợp Mg, Al, Fe trong dung dịch HXl dư thu được 13,44 lít khí H2 (đktc) và m gam muối . Cũng hỗn hợp trên tác dụng với clo thì thấy thể tích clo cần dùng là 17,36 lít
A. Tính khối lượng muối của từng kim loại trong hỗn hợp
B. Xác định m
























