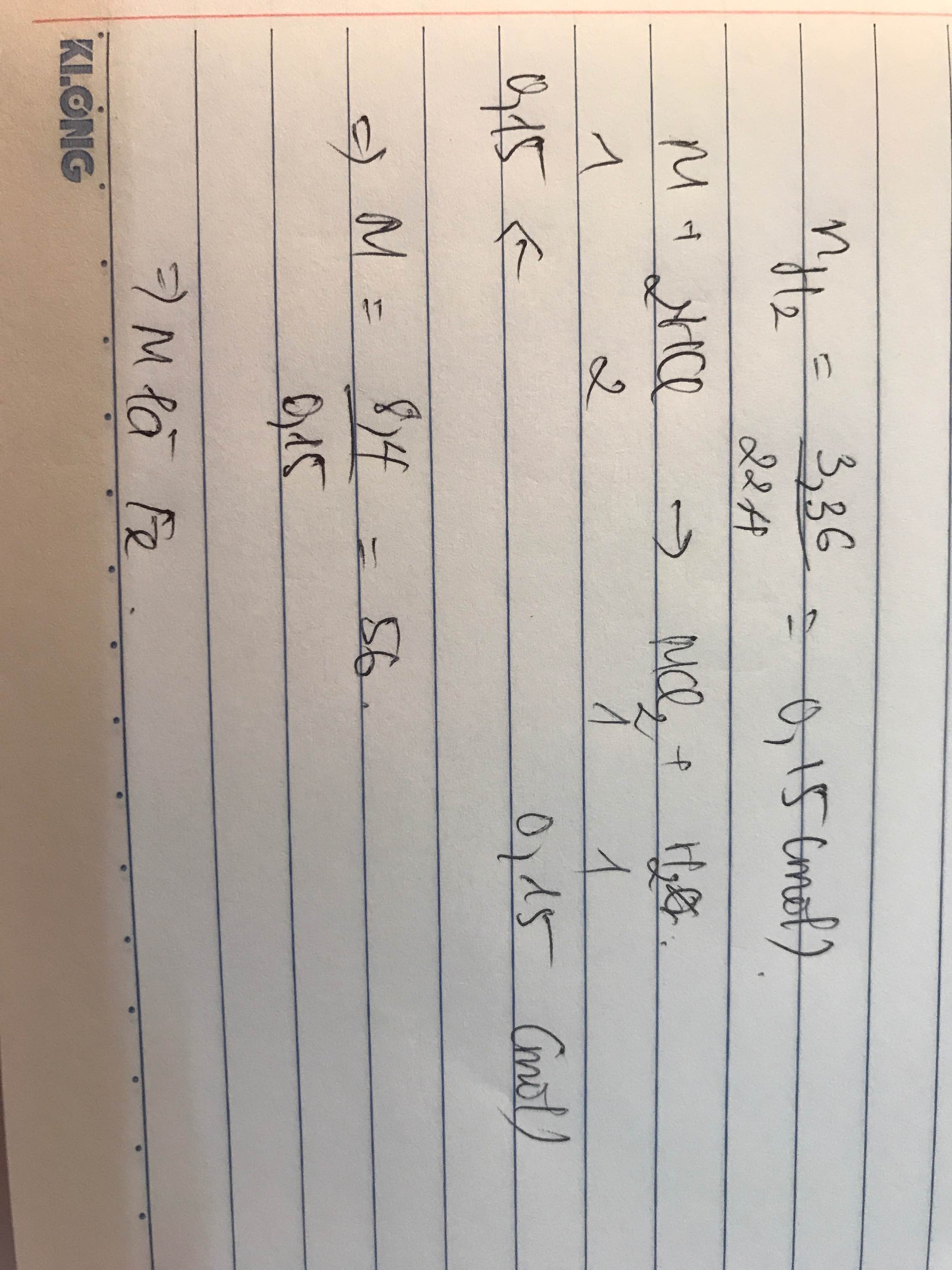Hòa tan hoàn toàn 7,2 gam kim loại R có hóa trị II vào dung dịch HCL dư. Sau phản ứng thu được dung dịch muố và 6,72lits khí H2 ở đktc. Em hãy cho biết kim loại R là kim loại nào?

Những câu hỏi liên quan
bài 1:cho 7,2g kim loại hóa trị II phản ứng hoàn toàn 100ml dung dịch HCL 6M. Xác định tên kim loại đã dùng
baì 2: hòa tan hoàn toàn 7,56g kim loại R có hóa trị III vào dung dịch axit HCL thu được 9,408 lít H2 (đktc). Tìm kim loại R
Giúp mik vs ạ ! Cảm ơn
Bài 1:
Gọi KL cần tìm là A.
PT: \(A+2HCl\rightarrow ACl_2+H_2\)
Ta có: \(n_{HCl}=0,1.6=0,6\left(mol\right)\)
Theo PT: \(n_A=\dfrac{1}{2}n_{HCl}=0,3\left(mol\right)\)
\(\Rightarrow M_A=\dfrac{7,2}{0,3}=24\left(g/mol\right)\)
Vậy: KL cần tìm là Mg.
Đúng 1
Bình luận (0)
Bài 2:
PT: \(2R+6HCl\rightarrow2RCl_3+3H_2\)
Ta có: \(n_{H_2}=\dfrac{9,408}{22,4}=0,42\left(mol\right)\)
Theo PT: \(n_R=\dfrac{2}{3}n_{H_2}=0,28\left(mol\right)\)
\(\Rightarrow M_R=\dfrac{7,56}{0,28}=27\left(g/mol\right)\)
Vậy: R là Al.
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn 6 gam một kim loại M hóa trị II vào dung dịch HCl, sau phản ứng thu được 3,36 lit khí H 2 (đktc). Kim loại M là:
A. Zn (65)
B. Mg (24)
C. Fe (56)
D. Ca (40)
Chọn D
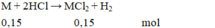
M M = 6 : 0 , 15 = 40 .
Vậy kim loại M là Ca.
Đúng 0
Bình luận (0)
cho 8,4 gam một kim loại M hóa trị II vào dung dịch HCl 10% dư. Sau khi kim loại hòa tan hoàn toàn thu được 3,36 lít khí đo ở đktc và dung dịch A.
a. Xác định kim loại M
b.Để phản ứng hết dung dịch A cần 500ml dung dịch NaOH 1M. Tính nồng độ phần trăm các chất trong dung dịch A
dạ em làm xong câu B rồi mọi người khỏi cần trả lời nữa ạ
Đúng 0
Bình luận (2)
Câu 10 : Hòa tan hoàn toàn 7,68 gam kim loại R (hóa trị II) bằng dung dịch axit sunfuric loãng lấy dư. Sau phản ứng thu được 7,168 lít H2(đktc). Cho biết tên, KHHH của kim loại M.
Đọc tiếp
Câu 10 : Hòa tan hoàn toàn 7,68 gam kim loại R (hóa trị II) bằng dung dịch axit sunfuric loãng lấy dư. Sau phản ứng thu được 7,168 lít H2(đktc). Cho biết tên, KHHH của kim loại M.
\(R+H_2SO_4\rightarrow RSO_4+H_2\\ n_{H_2}=\dfrac{7,168}{22,4}=0,32\left(mol\right)\\ n_R=n_{H_2}=0,32\left(mol\right)\\ M_R=\dfrac{7,68}{0,32}=24\left(\dfrac{g}{mol}\right)\\ \Rightarrow R\left(II\right):Magie\left(Mg=24\right)\)
Đúng 3
Bình luận (0)
Cho 18,6 gam hỗn hợp gồm Fe và kim loại R (hoá trị II không đổi) vào dung dịch chứa H2SO4 dư, kết thúc phản ứng thu được 6,72 lít khí (đktc). Nếu cho 4,95 gam kim loại R vào dung dịch chứa 5,475 gam HCl, sau phản ứng hoàn toàn vẫn còn dư kim loại. Xác định kim loại R?
- Cho 4,95 (g) R pư với HCl, thấy kim loại dư.
Ta có: \(n_{HCl}=\dfrac{5,475}{36,5}=0,15\left(mol\right)\)
PT: \(R+2HCl\rightarrow RCl_2+H_2\)
\(n_{R\left(pư\right)}=\dfrac{1}{2}n_{HCl}=0,075\left(mol\right)\)
\(n_{R\left(banđau\right)}>0,075\Rightarrow\dfrac{4,95}{M_R}>0,075\Rightarrow M_R< 66\left(g/mol\right)\) (1)
- Cho 18,6 (g) hh Fe và R pư với H2SO4 dư.
PT: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(R+H_2SO_4\rightarrow RSO_4+H_2\)
Ta có: \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Theo PT: \(n_{hh}=n_{Fe}+n_R=n_{H_2}=0,3\left(mol\right)\)
\(\Rightarrow\overline{M_{hh}}=\dfrac{18,6}{0,3}=62\left(g/mol\right)\)
Mà: MFe < 62 (g/mol) → MR > 62 (g/mol) (2)
Từ (1) và (2) ⇒ 62 < MR < 66
→ R là Zn (65 g/mol)
Đúng 2
Bình luận (0)
Hòa tan hoàn toàn 4,8 gam một kim loại R có hóa trị II vào 100 ml dung dịch HCl 5M. Sau phản ứng thu được 4,48 lít khí (đktc) và dung dịch A. Xác định R và tính nồng độ mol/lít các chất có trong dung dịch A.
PTHH: R + 2HCl ---> RCl2 + H2 (1)
Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
\(n_{HCl}=\dfrac{100}{1000}.5=0,5\left(mol\right)\)
Ta thấy: \(\dfrac{0,2}{1}< \dfrac{0,5}{2}\)
Vậy HCl dư.
Theo PT(1): \(n_R=n_{H_2}=0,2\left(mol\right)\)
=> \(M_R=\dfrac{4,8}{0,2}=24\left(g\right)\)
Vậy R là magie (Mg)
PT: Mg + 2HCl ---> MgCl2 + H2 (2)
Ta có: \(m_{dd_{MgCl_2}}=4,8+\dfrac{100}{1000}-0,2.2=4,5\left(lít\right)\)
Theo PT(2): \(n_{MgCl_2}=n_{H_2}=0,2\left(mol\right)\)
=> \(C_{M_{MgCl_2}}=\dfrac{0,2}{4,5}=\dfrac{2}{45}M\)
Đúng 0
Bình luận (0)
Hòa tan 14,4 gam kim loại R hóa trị II trong dung dịch HCl 29,2%. Sau khi phản ứng hoàn toàn thu được dung dịch mới có nồng độ HCl 5,456% và nồng độ muối clorua là 28,401%. Xác định kim loại R.
1,Khi hòa tan 7,2 gam một kim loại R hóa trị II vào dung dịch H2SO4 loãng dư sinh 6,72 lít khí H2 ở đktc. Tìm tên kim loại R.
Xem chi tiết
\(N_{H_2}=\dfrac{6,72}{22,4}=0,3mol\)
\(R+H_2SO_4\rightarrow RSO_4+H_2\)
Bảo toàn e ta có:
\(\dfrac{7,2}{M_R}.n=0,3.2=0,6\)
\(\Rightarrow7,2n=0,6.M_R\Leftrightarrow12n=M_R\)
Nếu n =1 => M = 12 ( loại)
Nếu n = 2 => M = 24 (Mg)
Đúng 3
Bình luận (0)
Hòa tan hoàn toàn 5,85 gam hỗn hợp gồm một kim loại hóa trị II và một kim loại hóa trị III vào dung dịch HCl dư thu được 3,024 lít H2 (đktc).
a/ Cô cạn dung dịch thu được bao nhiêu gam muối khan?
b/ Tính thể tích H2 thoát ra ở đktc.
c/ Nếu biết kim loại hóa trị III là Al và số mol bằng 1/3 lần số mol kim loại hóa trị II. Tìm kim loại hóa trị II.
a) \(n_{H_2}=\dfrac{3,024}{22,4}=0,135\left(mol\right)\)
=> nHCl = 0,27 (mol)
Theo ĐLBTKL: mkim loại + mHCl = mmuối + mH2
=> mmuối = 5,85 + 0,27.36,5 - 0,135.2 = 15,435 (g)
b) VH2 = 3,024 (l) (Theo đề bài)
c)
Hỗn hợp kim loại gồm \(\left\{{}\begin{matrix}Al:a\left(mol\right)\\X:3a\left(mol\right)\end{matrix}\right.\)
=> 27a + MX.3a = 5,85
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
a----------------------->1,5a
X + 2HCl --> XCl2 + H2
3a------------------->3a
=> 1,5a + 3a = 0,135
=> a = 0,03 (mol)
=> MX = 56 (g/mol)
=> X là Fe
Đúng 2
Bình luận (0)