Cho 13g Zn tác dụng với 182.5 g dd HCl 10% .
a ) Xác định chất nào còn dư .
b) Tính VH2 sinh ra.
Cho 13g Zn tác dụng với 182,5g dung dịch HCl 10% a.Chất nào còn dư b.Tính V và m khí H2 sinh ra c.Dung dịch sau phản ứng có những chất ran nào? Tính Nồng đọn % dung dịch các chất đó
nZn = 13/65 = 0,2 (mol)
mHCl = 182,5 . 10% = 18,25 (g)
nHCl = 18,25/36,5 = 0,25 (mol)
PTHH: Zn + 2HCl -> ZnCl2 + H2
LTL: 0,2 < 0,5/2 => HCl dư
nH2 = nZnCl2 = nZn = 0,2 (mol)
VH2 = 0,2 . 22,4 = 4,48 (l)
mH2 = 0,2 . 2 = 0,4 (g)
Chất tan: ZnCl2 và HCl dư
nHCl (p/ư) = 0,2 . 2 = 0,4 (mol)
mHCl (dư) = (0,5 - 0,4) . 36,5 = 3,65 (g)
mZnCl2 = 136 . 0,2 = 27,2 (g)
mdd (sau p/ư) = 182,5 + 13 - 0,4 = 195,1 (g)
C%HCl = 3,65/195,1 = 1,87%
C%ZnCl2 = 27,2/195,1 = 13,94%
cho 13g zn tác dụng với dung dịch hcl 10% tính vh2 thu được và tính c% dd sau phản ứng
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\\Zn+2HCl\rightarrow ZnCl_2+H_2\\ n_{HCl}=0,2.2=0,4\left(mol\right)\\ m_{ddHCl}=\dfrac{0,4.36,5.100}{10}=146\left(g\right)\\ n_{H_2}=n_{ZnCl_2}=n_{Zn}=0,2\left(mol\right)\\ V_{H_2\left(đktc\right)}=0,2.22,4=4,48\left(l\right)\\ C\%_{ddZnCl_2}=\dfrac{136.0,2}{13+146-0,2.2}.100\approx17,15\%\)
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PTHH: Zn + 2HCl → ZnCl2 + H2
Mol: 0,2 0,4 0,2 0,2
\(V_{H_2}=0,2.22,4=4,48\left(l\right)\)
\(m_{ddHCl}=\dfrac{0,4.36,5.100}{10}=146\left(g\right)\)
mdd sau pứ = 13+146-0,2.2 = 158,6 (g)
\(C\%_{ddZnCl_2}=\dfrac{0,2.136.100\%}{158,6}=17,15\%\)
7/ Cho 13g Zn tác dụng với dd HCl có chứa14,6g.
a/ Tính thể tích H2 thu được (đktc)?
b/ Chất nào còn dư và dư bao nhiêu g?
8/ Có một cốc đựng dd H2SO4 (l) . Lúc đầu người ta cho một lương bột nhôm vào dd axit , PƯ xong thu được 6,72(l) H2 (ơ đktc). Sau đó thêm tiếp vào dd đó một lượng bột kẽm dư , PƯ xong thu them được 4,48(l) H2 nữa.
a/ Viết phương trình hóa học của phản ứng?
b/ Tính khối lượng bột nhôm, bột kẽm PƯ?
c/ Tính khối lượng axit H2SO4 có trong dd ban đầu?
c/ Hợp chất tạo thành sau PƯ trên thuộc loại nào? Khối lượng của chúng là bao nhiêu?
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
\(n_{HCl}=\dfrac{14,6}{36,5}=0,4\left(mol\right)\)
\(pthh:Zn+2HCl->ZnCl_2+H_2\)
LTL :
\(\dfrac{0,2}{1}=\dfrac{0,4}{2}\)
=> ko chất nào dư
theo pthh : \(n_{H_2}=n_{Zn}=0,2\left(mol\right)\\
=>V_{H_2}=0,2.22,4=4,48\left(l\right)\)
Bài 8 (bài 7 bạn ở trên làm rồi)
\(n_{H_2\left(Al\right)}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\ n_{H_2\left(Zn\right)}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH:
2Al + 3H2SO4 ---> Al2(SO4)3 + 3H2
0,2 0,3 0,1 0,3
Zn + H2SO4 ---> ZnSO4 + H2
0,3 0,3 0,3 0,3
\(a,\left\{{}\begin{matrix}m_{Al}=0,3.27=8,1\left(g\right)\\m_{Zn}=0,3.65=19,5\left(g\right)\end{matrix}\right.\\ b,m_{H_2SO_4}=\left(0,3+0,3\right).98=58,8\left(g\right)\)
c, Hợp chất tạo thành thuộc loại muối trung hoà
mmuôí = 0,1.342 + 0,3.161 = 82,5 (g)
\(pthh:\left\{{}\begin{matrix}Al+3H_2SO_4->Al_2\left(SO_{\text{4}}\right)_3+3H_2\left(1\right)\\Zn+H_2SO_4->ZnSO_4+H_2\left(2\right)\end{matrix}\right.\)
\(n_{H_2\left(1\right)}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\
n_{H_2\left(2\right)}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
=>\(m_{Al}=0,3.27=8,1\left(mol\right)\\
n_{Zn}=0,2.65=13\left(g\right)\)
\(\Sigma n_{H_2SO_4}=0,3+0,2=0,5\left(mol\right)\\
=>\Sigma m_{H_2SO_4}=0,5.98=49\left(g\right)\)
=>\(\left\{{}\begin{matrix}m_{Al_2\left(SO\right)_4}=342.0,1=34,2\left(G\right)\left(mu\text{ối}\right)\\m_{ZnSO_4}=0,2.161=32,2\left(g\right)\left(mu\text{ối}\right)\end{matrix}\right.\)
Cho 13(g) Zn tác dụng với 182,5g) dung dịch Hcl 10% .
a,Chất nào còn dư sau phản ứng?tính khối lượng chất dư ?
b, Tính thể tích khí H2 sinh ra (ĐKTC)?
c, Dung dịch sau phản ứng có những chất tan nào? Tính nồng độ phần trăm của các chất đó?
\(n_{Zn}=\dfrac{13}{65}=0.2\left(mol\right)\)
\(n_{HCl}=\dfrac{182.5\cdot10}{100\cdot36.5}=0.5\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(0.2......0.4..........0.2........0.2\)
\(n_{HCl\left(dư\right)}=0.5-0.4=0.1\left(mol\right)\)
\(m_{HCl\left(dư\right)}=0.1\cdot36.5=3.65\left(g\right)\)
\(V_{H_2}=0.2\cdot22.4=4.48\left(l\right)\)
\(m_{\text{dung dịch sau phản ứng}}=13+182.5-0.2\cdot2=195.1\left(g\right)\)
\(C\%_{HCl\left(dư\right)}=\dfrac{3.65}{195.1}\cdot100\%=1.87\%\)
\(C\%_{ZnCl_2}=\dfrac{0.2\cdot136}{195.1}\cdot100\%=13.94\%\)
Cho 13g zn tác dụng với 200g dd hcl
tinhs Vh2
tính mZnCl2
tinhs c% đ sau phản ứng
lập pthh của pư
zn+2hcl→zncl2 +h2
1mo 2mol 1mol 1mol
0,2mol 0,2mol 0,2mol
số mol zn
nzn=\(\frac{13}{65}\)=0,2 mol
thể tích khí H2
VH2 = 0,2 . 22,4 =4,48 lít
khối lượng zncl2
mzncl2= 0,2. 136=2,72 gam
nồng độ % dd zncl2
c% zncl2=\(\frac{mct}{mdd}\). 100%=\(\frac{2,72}{200}\). 100%=1,36%![]()
cho 6,5 gam kẽm tác dụng với dung dịch HCl
a/ Tính VH2 sinh ra (đktc)
b/Dẫn toàn bộ khí H2 trên qua ống nghiệm đựng 12g CuO. Chất nào dư, dư bao nhiêu? Tính khối lượng đồng sinh ra.
$n_{Zn} = \dfrac{6,5}{65} = 0,1(mol) \\ PTHH: Zn + 2HCl \to ZnCl_2 + H_2 \\$$n_{H_2} = n_{Zn} = 0,1(Mol) \\ V_{H_2} = 0,1.22,4 = 2,24l \\b) PTHH: H_2 + CuO \xrightarrow[]{t^o} Cu + H_2O \\ n_{CuO} = \dfrac{12}{64} = 0,15(mol) \\ \to CuO dư$ $\\ n_{H_2} = n_{Cu} = 0,1(mol \\ m_{Cu} = 0,1.64 = 6,4(gam)$
Zn+2HCl->ZnCl2+H2
0,1---0,2----0,1---0,1
n Zn=0,1 mol
=>VH2=0,1.22,4=2,24l
H2+CuO-to>Cu+H2O
0,15-----0,15
n CuO=0,15 mol
=>H2 dư
=>m Cu=0,15.64=9,6g
Bài 1: Đốt cháy 6,2(g) P trong bình chứa 6,72(l) khí O2 ở đktc.
a. Sau phản ứng chất nào còn dư và nếu dư thì với khối lượng bao nhiêu? b. Tính khối lượng sản phẩm thu được.
Bài 2: Cho 13g Zn tác dụng với 0,3 mol HCl sau khi kết thúc phản ứng thu được muối kẽm Clorua và khí H2.
a. Viết và cân bằng PTPƯ và cho biết sau khi kết thúc phản ứng thì chất nào còn dư và nếu dư thì dư với khối lượng bao nhiêu?.
b. Tính thể tích của H2 thu được.
Bài 3: Người ta cho 26 g kẽm tác dụng với 49 g H2SO4, sau phản ứng thu được muối ZnSO4, khí hidro và chất còn dư.
a. Viết phương trình phản ứng.
b. Tính thể tích (đktc) khí hidro sinh ra.
c. Tính khối lượng các chất còn lại sau phản ứng.
Bài 4: Nếu cho 4 gam CuO tác dụng với 2,92 g HCl.
a) Cân bằng PTHH.
b) Tính khối lượng các chất còn lại sau phản ứng.
Bài 5: Hòa tan hoàn toàn 15gam CaCO3 vào 200mL dung dịch HCl 2M.
a. Chobiếtchấtnàodưsauphảnứng.
b. Tính nồng độ mol của các chất tan có trong dung dịch thu được.
Bài 6: Hòa tan hết 4,8 gam Magie vào 200 gam dung dịch H2SO4 loãng nồng độ 20%.
a. Chobiếtchấtnàodưsauphảnứng.
b. Tính nồng độ chất tan có trong dung dịch sau phản ứng.
Bài 7: Cho 200 ml dung dịch NaOH nồng độ 2M vào 200 mL dung dịch HCl 4M.
a. Chobiếtchấtnàodưsauphảnứng.
b. Tính nồng độ mol của chất tan trong dung dịch sau phản ứng.
Bài 1:
a) nP=6,2/31=0,2(mol); nO2= 6,72/22,4=0,3(mol)
PTHH: 4P + 5 O2 -to-> 2 P2O5
Ta có: 0,2/4 < 0,3/5
=> P hết, O2 dư, tính theo nP
=> nO2(p.ứ)= 5/4. nP= 5/4. 0,2=0,25(mol)
=> mO2(dư)=0,3- 0,25=0,05(mol)
=> mO2(dư)=0,05.32=1,6(g)
b) nP2O5= nP/2= 0,2/2=0,1(mol)
=>mP2O5=0,1.142=14,2(g)
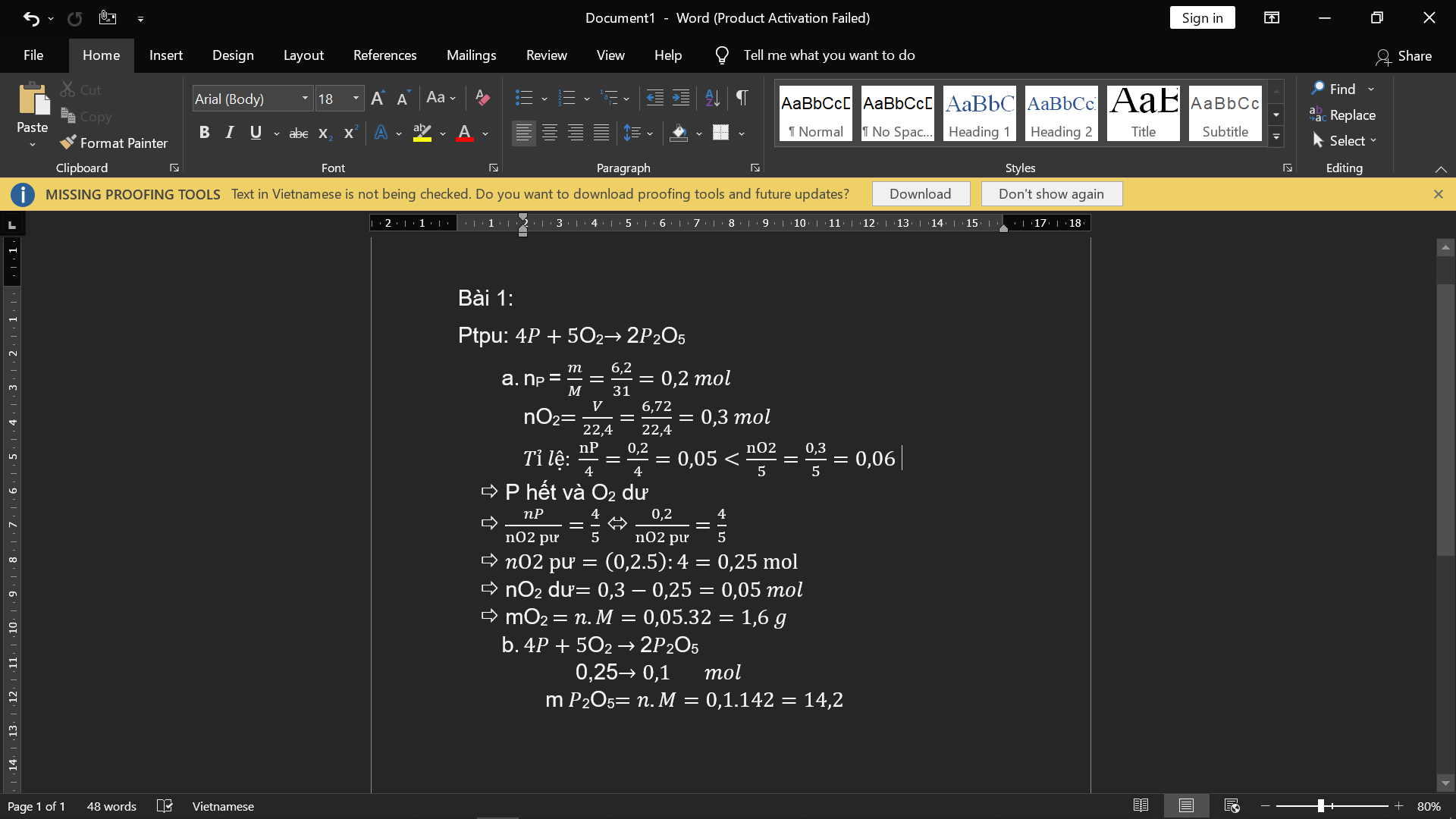
b ơi đây là bài 1 nka, tí mk làm xog sẽ gửi típ nka ![]()
cho 13g Zn tác dụng với 0,3 mol hcl sau phản ứng thu được a g zncl2 và V lít khí h2 (đktc)
a) viết phương trình phản ứng
b)sau phản ứng chất nào dư, dư bao nhiêu
c) tính a và V
\(a,PTHH:Zn+2HCl\to ZnCl_2+H_2\\ b,n_{Zn}=\dfrac{13}{65}=0,2(mol)\)
Vì \(\dfrac{n_{Zn}}{1}>\dfrac{n_{HCl}}{2}\) nên Zn dư
\(\Rightarrow n_{Zn({\text{phản ứng})}}=\dfrac{1}{2}n_{HCl}=0,15(mol)\\ \Rightarrow n_{Zn(\text{dư})}=0,2-0,15=0,05(mol)\\ \Rightarrow m_{Zn(\text{dư})}=0,05.65=3,25(g)\\ c,n_{ZnCl_2}=n_{H_2}=\dfrac{1}{2}n_{HCl}=0,15(mol)\\ \Rightarrow a=m_{ZnCl_2}=0,15.136=20,4(g)\\ V=V_{H_2}=0,15.22,4=3,36(l)\)
\(a,Zn+2HCl\rightarrow ZnCl_2+H_2\\ n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\\ Ta.c\text{ó}:\dfrac{0,2}{1}>\dfrac{0,3}{2}\Rightarrow Zn.d\text{ư}\\ b,n_{Zn\left(d\text{ư}\right)}=0,2-\dfrac{0,3}{2}=0,05\left(mol\right)\\ \Rightarrow m_{Zn\left(d\text{ư}\right)}=0,05.65=3,25\left(g\right)\\ c,a=m_{ZnCl_2}=0,15.136=20,4\left(g\right)\\ V=V_{H_2\left(\text{đ}ktc\right)}=0,15.22,4=3,36\left(l\right)\)
cho 13g Zn tác dụng với dd có chứa 14,6g HCl . a, tính H2 (đktc) b, tính khối lượng các chất có trong dd sau khi pư kết thúc
nZn = 13/65 = 0,2 (mol)
nHCl = 14,6/36,5 = 0,4 (mol)
PTHH: Zn + 2HCl -> ZnCl2 + H2
LTL: 0,2 = 0,4/2 => phản ứng đủ
nH2 = nZnCl2 = 0,2 (mol)
VH2 = 0,2 . 22,4 = 4,48 (l)
mZnCl2 = 0,1 . 136 = 27,2 (g)
mH2 = 0,2 . 2 = 0,4 (g)
\(n_{Zn}=\frac{13}{65}=0,2\left(mol\right)\)
\(n_{HCl}=\frac{14,6}{36,5}=0,4\left(mol\right)\)
\(PTHH:Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
tỉ số: \(\frac{0,2}{1}=\frac{0,4}{2}\Rightarrow\) PTHH này ko có chất dư (sau khi pứ kết thúc)
a) \(n_{H_2}=n_{Zn}=0,2\left(mol\right)\)
\(V_{H_2}=0,2.22,4=4,48\left(l\right)\)
\(n_{ZnCl_2}=n_{Zn}=0,2\left(mol\right)\)
\(m_{ZnCl_2}=0,2.136=27,2\left(g\right)\)
XONG!