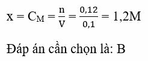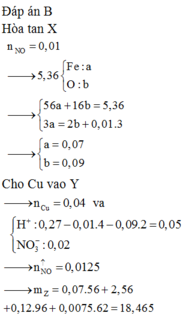Hòa tan 0.01 mol Fe2O3 và 0.02 mol Fe3O4 vào 500 ml dung dịch H2SO4 loãng 0.5 M thu được Y. Tính nồng độ mol của các chất trong Y

Những câu hỏi liên quan
Hòa tan hoàn toàn m gam hỗn hợp X gồm Cu và Fe3O4 trong 500 ml dung dịch H2SO4 nồng độ a mol /l (loãng ) , thu được dd Y. Cho Y tác dụng vừa đủ với dd chứa 1,6 mol NaOH, thu được 52g kết tủa . Tính giá trị của a và m
Hỗn hợp A gồm FeO, Fe2O3, Fe3O4 (trong đó số mol FeO bằng số mol Fe2O3). Hòa tan 4,64 gam A trong dung dịch H2SO4 loãng dư được 200 ml dung dịch X. Tính thể tích dung dịch KMnO4 0,1M cần thiết để chuẩn độ hết 100 ml dung dịch X? A. 0,1l B. 0,12l C. 0,2l D.0,24l
Đọc tiếp
Hỗn hợp A gồm FeO, Fe2O3, Fe3O4 (trong đó số mol FeO bằng số mol Fe2O3). Hòa tan 4,64 gam A trong dung dịch H2SO4 loãng dư được 200 ml dung dịch X. Tính thể tích dung dịch KMnO4 0,1M cần thiết để chuẩn độ hết 100 ml dung dịch X?
A. 0,1l
B. 0,12l
C. 0,2l
D.0,24l
Đáp án C
Vì số mol của FeO bằng số mol của Fe2O3 nên ta coi hỗn hợp là Fe3O4
Ta có:
Fe3O4 +4H2SO4 → FeSO4 +Fe2(SO4)3 +4H2O
0,02 0,02
Trong 100 ml X sẽ có 0,01 mol FeSO4 nên:
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
→ nKMnO4 = 0,02 mol → VKMnO4 = 0,02/0,1 = 0,2 l
Đúng 0
Bình luận (0)
Hỗn hợp X gồm Fe, FeO,
Fe
2
O
3
và
Fe
3
O
4
với số mol mỗi chất là 0,12 mol hoà tan hết vào dung dịch Y gồm (HCl,
H
2
SO
4
loãng) dư thu được dung dịch Z. Nhỏ từ từ 100 ml dung dịch
Cu
NO...
Đọc tiếp
Hỗn hợp X gồm Fe, FeO, Fe 2 O 3 và Fe 3 O 4 với số mol mỗi chất là 0,12 mol hoà tan hết vào dung dịch Y gồm (HCl, H 2 SO 4 loãng) dư thu được dung dịch Z. Nhỏ từ từ 100 ml dung dịch Cu NO 3 2 xM vào dung dịch Z cho tới khi ngừng thoát khí NO. Giá trị của x là
A. 0,8M
B. 1,2M
C. 1,6M
D. 2,4M
Hòa tan hết 5,36 gam hỗn hợp X gồm FeO, Fe2O3, Fe3O4 trong dung dịch chứa 0,03 mol HNO3 và 0,12 mol H2SO4 thu được dung dịch Y và 224 ml khí NO (đktc). Cho 2,56 gam Cu vào Y thu được dung dịch Z. Biết các phản ứng hoàn toàn, NO là sản phẩm khử duy nhất của N+5. Khối lượng muối trong Z là: A. 16,924 B. 18,465 C. 19,424 D. 23,176
Đọc tiếp
Hòa tan hết 5,36 gam hỗn hợp X gồm FeO, Fe2O3, Fe3O4 trong dung dịch chứa 0,03 mol HNO3 và 0,12 mol H2SO4 thu được dung dịch Y và 224 ml khí NO (đktc). Cho 2,56 gam Cu vào Y thu được dung dịch Z. Biết các phản ứng hoàn toàn, NO là sản phẩm khử duy nhất của N+5. Khối lượng muối trong Z là:
A. 16,924
B. 18,465
C. 19,424
D. 23,176
hòa tan 18, 4 g kim loại kiềm a vào 500 ml dung dịch H2so4 thu được dung dịch X và 0,8 g khí
a)tìm tên loại kim loại A
b)xác định nồng độ mol của chất tan trong dung dịch X và h2so4 ban đầu
a) \(n_{H_2}=\dfrac{0,8}{2}=0,4\left(mol\right)\)
PTHH: 2A + H2SO4 --> A2SO4 + H2
0,8<-------------------------0,4
=> \(M_A=\dfrac{18,4}{0,8}=23\left(Na\right)\)
b)
PTHH: 2Na + H2SO4 --> Na2SO4 + H2
0,4<--------0,4<----0,4
=> \(C_{M\left(ddH_2SO_4\right)}=\dfrac{0,4}{0,5}=0,8M\)
\(C_{M\left(ddNa_2SO_4\right)}=\dfrac{0,4}{0,5}=0,8M\)
Đúng 3
Bình luận (0)
Hòa tan 23,5g K2O vào nước thành 500ml dung dịch
a)Tính nồng độ mol của dung dịch thu được
b)Tính thể tính dung dịch H2So4 20% (D=1,14g/ml) cần để trung hòa dung dịch trên
c)Tính nồng độ mol của chất tan trong dung dịch sau PỨ
![]()
\(n_{K_2O}=\dfrac{23.5}{94}=0.25\left(mol\right)\)
\(K_2O+H_2O\rightarrow2KOH\)
\(0.25...................0.5\)
\(C_{M_{KOH}}=\dfrac{0.5}{0.5}=1\left(M\right)\)
\(2KOH+H_2SO_4\rightarrow K_2SO_4+H_2O\)
\(0.5............0.25............0.25\)
\(m_{dd_{H_2SO_4}}=\dfrac{0.25\cdot98}{20\%}=122.5\left(g\right)\)
\(V_{dd_{H_2SO_4}}=\dfrac{122.5}{1.14}=107.5\left(ml\right)=0.1075\left(l\right)\)
\(C_{M_{K_2SO_4}}=\dfrac{0.25}{0.1075+0.5}=0.4\left(M\right)\)
Đúng 3
Bình luận (0)
nK2O = 23,5 : 94 = 0,25 (mol)
Vdd = 500ml = 0,5l
PT K2O + H2O ==> 2KOH
TPT 1 1 2 (mol)
TĐB: 0,25 --> 0,5 (mol)
a) CM KOH = 0,5 : 0,5 = 1(M)
b) PT: H2SO4 + 2KOH ==> K2SO4 + 2H2O
TPT: 1 2 1 2 (mol)
Đúng 1
Bình luận (1)
a.
\(n_{K_2O}=\dfrac{m}{M}=\dfrac{23,5}{94}=0,25\left(mol\right)\\ PT:\\ K_2O+H_2O\rightarrow2KOH\)
Theo pt: \(n_{KOH}=2n_{K_2O}=0,5\left(mol\right)\)
\(\Rightarrow C_{M\left(KOH\right)}=\dfrac{n}{V}=\dfrac{0,5}{0,5}=1\left(M\right)\)
b.
\(PT:\\ 2KOH+H_2SO_4\rightarrow K_2SO_4+2H_2O\)(2)
Theo pt, \(n_{H_2SO_4}=\dfrac{1}{2}n_{KOH}=0,25\left(mol\right)\)
\(\Rightarrow V_{ddH_2SO_4}=\dfrac{m_{dd}}{D}=\dfrac{n.M:C\%}{D}=\dfrac{0,25.98:20\%}{1,14}=\)107,46(ml)
c.
dd spư có chất tan là K2SO4
Theo pt (2), \(n_{K_2SO_4}=\dfrac{1}{2}n_{KOH}=0,25\left(mol\right)\)
=> CM = \(\dfrac{n}{V}=\dfrac{0,25}{0,107}=2,336\left(M\right)\)
Đúng 0
Bình luận (2)
Hòa tan hết 11,2 gam kim loại M hóa trị II trong 500 ml dung dịch H2SO4 1M thu được dung dịch A và 4,48 lít H2 (đktc). a/ Xác định M. Fe b/ Tính nồng độ mol của các chất tan trong dung dịch A. 0,6 + 0,4 c/ Làm lạnh dung dịch sau phản ứng A thu được bao nhiêu gam MSO4.7H2O?
a, Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PT: \(M+H_2SO_4\rightarrow MSO_4+H_2\)
Theo PT: \(n_M=n_{H_2}=0,2\left(mol\right)\)
\(\Rightarrow M_M=\dfrac{11,2}{0,2}=56\left(g/mol\right)\)
→ M là Fe.
b, Theo PT: \(n_{FeSO_4}=n_{H_2SO_4\left(pư\right)}=n_{H_2}=0,2\left(mol\right)\)
⇒ nH2SO4 dư = 0,5.1 - 0,2 = 0,3 (mol)
\(\Rightarrow\left\{{}\begin{matrix}C_{M_{H_2SO_4\left(dư\right)}}=\dfrac{0,3}{0,5}=0,6\left(M\right)\\C_{M_{FeSO_4}}=\dfrac{0,2}{0,5}=0,4\left(M\right)\end{matrix}\right.\)
c, Ta có: \(n_{FeSO_4.7H_2O}=n_{FeSO_4}=0,2\left(mol\right)\)
\(\Rightarrow m_{FeSO_4.7H_2O}=0,2.278=55,6\left(g\right)\)
Đúng 1
Bình luận (0)
Tính nồng độ mol/lit của các ion trong các trường hợp sau? a. Hòa tan 5,85g NaCl vào 500 ml H2O. b. Hòa tan 34,2 gam Ba(OH)2 vào nước để được 500 ml dung dịch. c. Hòa tan 25 ml dung dịch H2SO4 2M vào 125ml nước.
a) Ta có: \(n_{NaCl}=\dfrac{5,85}{58,5}=0,1\left(mol\right)\)
\(\Rightarrow C_{M_{NaCl}}=\dfrac{0,1}{0,5}=0,2\left(M\right)=\left[Na^+\right]=\left[Cl^-\right]\)
b) Ta có: \(n_{Ba\left(OH\right)_2}=\dfrac{34,2}{171}=0,2\left(mol\right)\)
\(\Rightarrow C_{M_{Ba\left(OH\right)_2}}=\dfrac{0,2}{0,5}=0,4\left(M\right)\) \(\Rightarrow\left\{{}\begin{matrix}\left[Ba^{2+}\right]=0,4\left(M\right)\\\left[OH^-\right]=0,8\left(M\right)\end{matrix}\right.\)
c) Ta có: \(n_{H_2SO_4}=0,025\cdot2=0,05\left(mol\right)\)
\(\Rightarrow C_{M_{H_2SO_4}}=\dfrac{0,05}{0,125+0,025}\approx0,33\left(M\right)\) \(\Rightarrow\left\{{}\begin{matrix}\left[H^+\right]=0,66\left(M\right)\\\left[SO_4^{2-}\right]=0,33\left(M\right)\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Câu 2. Hòa tan hoàn toàn 0,2 mol NaOH vào 500 ml H20 thu được dung dịch B. Tính nồng độ %, nồng độ mol/l của dung dịch B Câu 3. Hòa tan hoàn toàn 2,8 gam KOH và 5,85 gam NaCl vào 600 ml H20 thu được dung dịch C. Tính nồng độ %, nồng độ mol/l của dung dịch C Câu 4. Hoà tan hoàn toàn 4,6 gam Na vào 100 gam H20 thu được dung dịch D. Tính nồng độ %, nồng độ mol/l của dung dịch D Câu 5. Hòa tan hoàn toàn 2,74 gam Ba vào 200 gam H2O thu được dung dịch E. Tính nồng độ %, nồng độ mol/l của dung dịch E...
Đọc tiếp
Câu 2. Hòa tan hoàn toàn 0,2 mol NaOH vào 500 ml H20 thu được dung dịch B. Tính nồng độ %, nồng độ mol/l của dung dịch B Câu 3. Hòa tan hoàn toàn 2,8 gam KOH và 5,85 gam NaCl vào 600 ml H20 thu được dung dịch C. Tính nồng độ %, nồng độ mol/l của dung dịch C Câu 4. Hoà tan hoàn toàn 4,6 gam Na vào 100 gam H20 thu được dung dịch D. Tính nồng độ %, nồng độ mol/l của dung dịch D Câu 5. Hòa tan hoàn toàn 2,74 gam Ba vào 200 gam H2O thu được dung dịch E. Tính nồng độ %, nồng độ mol/l của dung dịch E Câu 6. Hòa tan hoàn toàn 5,85 gam K và 13,7 gam Ba vào 400 ml H2O thu được dung dịch F, Tính nồng độ %, nồng độ mol/l của dung dịch