đốt cháy hoàn toàn 12g hợp chất hữu cơ A thì được 8,96 lít CO2 và 7,2g nước .xác định công thức phân tử và công thức cấu tạo của A,biết tỉ khối hơi của A với C2H6=2

Những câu hỏi liên quan
Đốt cháy hoàn toàn 5,6g chất hữu cơ A thu được 8,96 lít khí CO2 và 7,2g H2O.
a) Tìm công thức đơn giản nhất của A?
b) Tìm công thức phân tử của A? (biết tỉ khối hơi của A so với hidro là 28).
Đốt cháy hoàn toàn 5,6 gam chất hữu cơ A thu được 8,96 lít khí CO2 (đktc) và 7,2g H2O. a) Tìm công thức đơn giản nhất của A? b) Tìm công thức phân tử của A? (Biết tỉ khối hơi của A so với hiđro bằng 28).
\(n_C=n_{CO_2}=0,4\left(mol\right);n_H=2.n_{H_2O}=2.0,4=0,8\left(mol\right)\\ m_C+m_H=0,4.12+0,8.1=5,6=m_A\)
=> A là hidrocacbon: A chỉ có 2 nguyên tố là C và H
\(a,n_C:n_H=0,4:0,8=1:2\\ \Rightarrow A.có.CTĐG:CH_2\\ b,Đặt.CTTQ:\left(CH_2\right)_a\left(a:nguyên,dương\right)\\ M_{\left(CH_2\right)_a}=28\\ \Leftrightarrow14a=28\\ \Leftrightarrow a=2\\ \Rightarrow CTPT:C_2H_4\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 7,6g chất hữu cơ A thu được 13,2g CO2 và 7,2g H2O a) xác định công thức đơn nhất nhất của A b) Xác định cấu tạo phân tử và cấu tạo chứa nhóm OH của chất A . Biết tỉ khối của A so với He = 19
\(n_{CO_2}=\dfrac{13,2}{44}=0,3\left(mol\right)\)
\(m_{H_2O}=\dfrac{7,2}{18}=0,4\left(mol\right)\)
Bảo toàn C: nC = 0,3 (mol)
Bảo toàn H: nH = 0,8 (mol)
=> \(n_O=\dfrac{7,6-0,3.12-0,8.1}{16}=0,2\left(mol\right)\)
nC : nH : nO = 0,3 : 0,8 : 0,2 = 3:8:2
=> CTDGN: C3H8O2
b) CTPT: (C3H8O2)n
Mà MA = 19.4 = 76
=> n = 1
=> CTPT: C3H8O2
CTCT
(1) CH3-CH(OH)-CH2OH
(2) CH2OH - CH2 - CH2OH
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 14,4 gam hợp chất hữu cơ thu được 21,12 gam CO2 và 8,64 gam H2O Xác định công thức phân tử của chất hữu cơ biết 1 lít hơi A ở dktc nặng 2,676 gam , Biết là axit hữu cơ . Xác định công thức cấu tạo dùng của
Bảo toàn C: \(n_C=\dfrac{21,12}{44}=0,48\left(mol\right)\)
Bảo toàn H: \(n_H=2.\dfrac{8,64}{18}=0,96\left(mol\right)\)
Bảo toàn O: \(n_O=\dfrac{14,4-0,48.12-0,96}{16}=0,48\left(mol\right)\)
\(M_{hchc}=2,676.22,4=60\left(\dfrac{g}{mol}\right)\)
CTPT: CxHyOz
=> x : y : z = 0,48 : 0,96 : 0,48 = 1 : 2 : 1
=> (CH2O)n =60
=> n = 2
CTPT: C2H4O2
CTCT: CH3-COOH
Đúng 3
Bình luận (0)
Đốt hoàn toàn 12g hợp chất hữu cơ A. Sau phản ứng thu được 26,4g CO2 và 14,4g H2O a) hợp chất A có bao nhiêu nguyên tố b) xác định công thức phân tử công thức cấu tạo của A biết A có tỉ khối so với H2 và 30
a, - Đốt A thu CO2 và H2O.
→ A chứa C và H, có thể có O.
Ta có: \(n_{CO_2}=\dfrac{26,4}{44}=0,6\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{14,4}{18}=0,8\left(mol\right)\Rightarrow n_H=0,8.2=1,6\left(mol\right)\)
⇒ mC + mH = 0,6.12 + 1,6.1 = 8,8 (g) < mA
→ A gồm 3 nguyên tố: C, H và O.
⇒ mO = 12 - 8,8 = 3,2 (g) \(\Rightarrow n_O=\dfrac{3,2}{16}=0,2\left(mol\right)\)
b, Gọi CTPT của A là CxHyOz.
⇒ x:y:z = 0,6:1,6:0,2 = 3:8:1
→ A có CTPT dạng (C3H8O)n
Mà: MA = 30.2 = 60 (g/mol)
\(\Rightarrow n=\dfrac{60}{12.3+1.8+16}=1\)
Vậy: CTPT của A là C3H8O.
CTCT: CH3-CH2-CH2-OH
CH3-CH(OH)-CH3
CH3-O-CH2-CH3
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn 5.4g một hợp chất hữu cơ A thu được 8.4 lít co2 và 8.1g nước a. Tính khối lượng gam và phần trăm khối lượng nguyên tố có trong Á b. Xác định công thức đơn giản nhất của A c. Xác định công thức phân tử của A. Biết tỉ khối hơi của A so với oxi là 2.25 d. Viết các công thức cấu tạo của A
a)
\(n_{CO_2}=\dfrac{8,4}{22,4}=0,375\left(mol\right)\)
\(n_{H_2O}=\dfrac{8,1}{18}=0,45\left(mol\right)\)
Bảo toàn C: nC = 0,375 (mol)
Bảo toàn H: nH = 0,9 (mol)
mC = 0,375.12 = 4,5 (g)
mH = 0,9.1 = 0,9 (g)
=> mO = 5,4 - 4,5 - 0,9 = 0 (g)
=> \(\left\{{}\begin{matrix}\%C=\dfrac{4,5}{5,4}.100\%=83,33\%\\\%H=\dfrac{0,9}{5,4}.100\%=16,67\%\end{matrix}\right.\)
b)
nC : nH = 0,375 : 0,9 = 5 : 12
=> CTDGN: C5H12
c)
CTPT: (C5H12)n
Mà M = 2,25.32 = 72 (g/mol)
=> n = 1
=> CTPT: C5H12
Đúng 1
Bình luận (0)
Để đốt cháy hoàn toàn một lượng chất hữu cơ A phải dùng vừa hết 3,08 lít
O
2
. Sản phẩm thu được chỉ gồm có 1,80 g
H
2
O
và 2,24 lít
C
O
2
. Các thể tích khí đo ở đktc.1. Xác định công thức đơn giản nhất của A.2. Xác định công thức phân tử của A, biết rằng tỉ khối hơi của A đối với oxi là 2,25.3. Xác định công thức cấu tạo có thể có của chất A, ghi...
Đọc tiếp
Để đốt cháy hoàn toàn một lượng chất hữu cơ A phải dùng vừa hết 3,08 lít O 2 . Sản phẩm thu được chỉ gồm có 1,80 g H 2 O và 2,24 lít C O 2 . Các thể tích khí đo ở đktc.
1. Xác định công thức đơn giản nhất của A.
2. Xác định công thức phân tử của A, biết rằng tỉ khối hơi của A đối với oxi là 2,25.
3. Xác định công thức cấu tạo có thể có của chất A, ghi tên tương ứng, biết rằng A là hợp chất cacbonyl.
1. Theo định luật bảo toàn khối lượng:
m A = m C O 2 + m H 2 O − m O 2
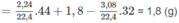
Khối lượng C trong 1,8 g A là: 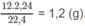
Khối lượng H trong 1,8 g A là: 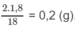
Khối lượng O trong 1,8 g A là : 1,8 - 1,2 - 0,2 = 0,4 (g).
Công thức chất A có dạng C x H y O z :
x : y : z = 0,1 : 0,2 : 0,025 = 4 : 8 : 1
CTĐGN là C 4 H 8 O
2. M A = 2,25.32 = 72 (g/mol)
⇒ CTPT trùng với CTĐGN: C 4 H 8 O .
3. Các hợp chất cacbonyl C 4 H 8 O :
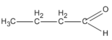 (butanal)
(butanal)
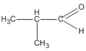 (2-metylpropanal)
(2-metylpropanal)
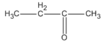 (butan-2-ol)
(butan-2-ol)
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 0,88 gam hợp chất hữu cơ X (chứa C, H, O), thu được 8,96 lít khí CO2 ở đktc và 0,72 gam H2O. Tỉ khối hơi của X so với H2 là 44. Xác định công thức phân tử của X?
Bn check lại đề chứ mình nghĩ VCO2 = 0,896 (l)
\(n_{CO_2}=\dfrac{0,896}{22,4}=0,04\left(mol\right)\)
\(n_{H_2O}=\dfrac{0,72}{18}=0,04\left(mol\right)\)
Bảo toán C: nC(X) = 0,04 (mol)
Bảo toàn H: nH(X) = 0,04.2 = 0,08 (mol)
=> \(n_{O\left(X\right)}=\dfrac{0,88-0,04.12-0,08.1}{16}=0,02\left(mol\right)\)
=> nC : nH : nO = 0,04 : 0,08 : 0,02 = 2 : 4 : 1
=> CTHH: (C2H4O)n
Mà M = 44.2 = 88(g/mol)
=> n = 2
=> CTHH: C4H8O2
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn 1,16g hợp chất hợp chất hữu cơ A thu được 3,52g CO 2 và 1,8g H 2 O. Biết tỉ khối hơi của A đối với hiđro là 29: Trong phân tử A gồm có những nguyên tố nào; Xác định công thức phân tử của A; Viết các công thức cấu tạo có thể có của hợp chất hợp chất hữu cơ.
Giúp mình với mình đang cần gấp !
Làm ơn !!!!!
Để đốt cháy hoàn toàn 2,85 g chất hữu cơ X phải dùng vừa hết 4,20 lít
O
2
(đktc). Sản phẩm cháy chỉ có
C
O
2
và
H
2
O
theo tỉ lệ 44 : 15 về khối lượng.1. Xác định công thức đơn giản nhất của chất X.2. Xác định công thức phân tử của X biết rằng tỉ khối hơi của X đối với
C
2
H
6...
Đọc tiếp
Để đốt cháy hoàn toàn 2,85 g chất hữu cơ X phải dùng vừa hết 4,20 lít O 2 (đktc). Sản phẩm cháy chỉ có C O 2 và H 2 O theo tỉ lệ 44 : 15 về khối lượng.
1. Xác định công thức đơn giản nhất của chất X.
2. Xác định công thức phân tử của X biết rằng tỉ khối hơi của X đối với C 2 H 6 là 3,80.
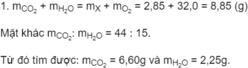
Khối lương C: 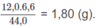
Khối lượng H: 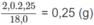
Khối lượng O: 2,85 - 1,80 - 0,25 = 0,80 (g).
Chất X có dạng CxHyOz
x : y : z = 0,150 : 0,25 : 0,050 = 3 : 5 : 1
Công thức đơn giản nhất của X là C 3 H 5 O .
2, M X = 3,80 x 30,0 = 114,0 (g/mol)
( C 3 H 5 O ) n = 114; 57n = 114 ⇒ n = 2.
Công thức phân tử C 6 H 10 O 2 .
Đúng 0
Bình luận (0)




















