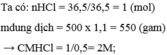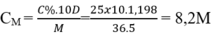Dung dịch HCL có nồng độ mol là 13,14mol và khối lượng riêng là 1,198g/ml . Tính nồng độ phần trăm của dung dịch HCL

Những câu hỏi liên quan
Hòa tan 36,5 gam HCl vào nước, thu được 500ml dung dịch có khối lượng riêng D = 1,1 g/ml. Tính nồng độ mol và nồng độ phần trăm của dung dịch thu được.
Dung dịch axit HCl trên thị trường bán có nồng độ cao nhất là 37%, khối lượng riêng D=1.19g/mol.
a) Tính nồng độ mol của dung dịch.
b) Tính nồng độ phần trăm của dd HCl 10.81 M có D=1.17g/l
Dung dịch HCl nồng độ 26% (kí hiệu là dung dịch X) có khối lượng riêng d 1,189 g/mL.a. Tính số mol HCl có trong 10 mL dung dịch X.b. Để hòa tan vừa hết 16 gam Fe2O3 cần dùng vừa hết y mL dung dịch X. Tính giá trị của y.c. Tính nồng độ mol/L của dung dịch X.d. Để hòa tan vừa hết 20 gam muối cacbonat BCO3 (Z là kim loại chưa biết) cần dùng vừa đủ 48,78 mL dung dịch X. Tìm kim loại Z.
Đọc tiếp
Dung dịch HCl nồng độ 26% (kí hiệu là dung dịch X) có khối lượng riêng d = 1,189 g/mL.
a. Tính số mol HCl có trong 10 mL dung dịch X.
b. Để hòa tan vừa hết 16 gam Fe2O3 cần dùng vừa hết y mL dung dịch X. Tính giá trị của y.
c. Tính nồng độ mol/L của dung dịch X.
d. Để hòa tan vừa hết 20 gam muối cacbonat BCO3 (Z là kim loại chưa biết) cần dùng vừa đủ 48,78 mL dung dịch X. Tìm kim loại Z.
Tính nồng độ mol của dung dịch HCl, biết dung dịch HCl 25% có khối lượng riêng bằng 1,198 g/ml.
A. 8M
B. 8,2M
C. 7,9M
D. 6,5M
Hòa tan hoàn toàn 10.6g Na2CO3 vào nước được 200ml dung dịch Na2CO3 . Tính nồng độ phần trăm và nồng độ mol của dung dịch trên. Biết khối lượng riêng của dung dịch là 1.05g/ml
\(n_{Na_2CO_3}=\dfrac{10,6}{106}=0,1\left(mol\right)\\ \rightarrow C_{M\left(Na_2CO_3\right)}=\dfrac{0,1}{0,2}=0,5M\)
Ta có: \(C\%=\dfrac{C_M.M}{10.D}\)
\(\rightarrow C\%=\dfrac{0,5.106}{10.1,05}=5,05\%\)
Đúng 1
Bình luận (0)
Biết khối lượng CuSO4 là 3 gam khối lượng riêng của dung dịch D-1,15(g/ml),nồng độ phần trăm của dung dịch là 15%.Tính khối lượng của dung dịch? Thể tích dung dịch? Nồng dộ mol của dung dịch
Ta có: \(m_{ddCuSO_4}=\dfrac{3}{15\%}=20\left(g\right)\)
\(V_{ddCuSO_4}=\dfrac{20}{1,15}\approx17,39\left(ml\right)\)
Ta có: \(n_{CuSO_4}=\dfrac{3}{160}=0,01875\left(mol\right)\)
\(\Rightarrow C_{M_{CuSO_4}}=\dfrac{0,01875}{0,01739}\approx1,08M\)
Bạn tham khảo nhé!
Đúng 1
Bình luận (0)
Trộn 150ml dung dịch HCl 10% có khối lượng riêng D=1,206 g/ml với 250 ml dung dịch HCl 2M thu được dung dịch A . Tính nồng độ mol của dung dịch A
\(m_{dd_{HCl\left(10\%\right)}}=150\cdot1.206=180.9\left(g\right)\)
\(n_{HCl}=\dfrac{180.9\cdot10\%}{36.5}\approx0.5\left(mol\right)\)
\(n_{HCl\left(2M\right)}=0.25\cdot2=0.5\left(mol\right)\)
\(n_{HCl}=0.5+0.5=1\left(mol\right)\)
\(V_{dd_{HCl}}=150+250=400\left(ml\right)=0.4\left(l\right)\)
\(C_{M_{HCl}}=\dfrac{1}{0.4}=2.5\left(M\right)\)
Đúng 4
Bình luận (0)
1. Một dung dịch CuSO4 (gọi là dung dịch X) có khối lượng riêng là 1,6 g/ml. Nếu đun nhẹ 25 ml dung dịch để làm bay hơi nước thì thu được 11,25 gam tinh thể CuSO4.5H2O. a) Tính nồng độ phần trăm và nồng độ mol của dung dịch X. b) Lấy 200 gam dung dịch X làm lạnh đến t0C thấy tách ra 5,634 gam tinh thể CuSO4.5H2O. Tính độ tan của CuSO4 ở t0C. 2. Trên hai đĩa cân để 2 cốc đựng 90 gam dung dịch HCl 7,3% (cốc 1) và 90 gam dung dịch H2SO4 14,7% (cốc 2) sao cho cân ở vị trí thăng bằng. - Thêm vào...
Đọc tiếp
1. Một dung dịch CuSO4 (gọi là dung dịch X) có khối lượng riêng là 1,6 g/ml. Nếu đun nhẹ 25 ml dung dịch để làm bay hơi nước thì thu được 11,25 gam tinh thể CuSO4.5H2O.
a) Tính nồng độ phần trăm và nồng độ mol của dung dịch X.
b) Lấy 200 gam dung dịch X làm lạnh đến t0C thấy tách ra 5,634 gam tinh thể CuSO4.5H2O. Tính độ tan của CuSO4 ở t0C.
2. Trên hai đĩa cân để 2 cốc đựng 90 gam dung dịch HCl 7,3% (cốc 1) và 90 gam dung dịch H2SO4 14,7% (cốc 2) sao cho cân ở vị trí thăng bằng.
- Thêm vào cốc thứ nhất 10 gam CaCO3.
- Thêm vào cốc thứ hai y gam Zn thấy kim loại tan hoàn toàn và thoát ra V’ lít khí hidro (đktc). a) Viết các PTHH xảy ra.
b) Sau các thí nghiệm, thấy cân vẫn thăng bằng. Tính giá trị y và V’. (Kết quả lấy 3 chữ số sau dấu phẩy)
1)
\(m_{ddCuSO_4\left(bd\right)}=1,6.25=40\left(g\right)\)
\(n_{CuSO_4.5H_2O}=\dfrac{11,25}{250}=0,045\left(mol\right)\)
=> \(n_{CuSO_4}=0,045\left(mol\right)\)
\(C_M=\dfrac{0,045}{0,025}=1,8M\)
\(C\%=\dfrac{0,045.160}{40}.100\%=18\%\)
b)
\(m_{CuSO_4}=\dfrac{200.18}{100}=36\left(g\right)\)
\(n_{CuSO_4.5H_2O}=\dfrac{5,634}{250}=0,022536\left(mol\right)\)
nCuSO4 (tách ra) = 0,022536 (mol)
=> \(m_{CuSO_4\left(dd.ở.t^o\right)}=36-0,022536.160=32,39424\left(g\right)\)
\(m_{H_2O\left(bd\right)}=200-36=164\left(g\right)\)
nH2O (tách ra) = 0,022536.5 = 0,11268 (mol)
=> \(m_{H_2O\left(dd.ở.t^o\right)}=164-0,11268.18=161,97176\left(g\right)\)
\(S_{t^oC}=\dfrac{32,39424}{161,97176}.100=20\left(g\right)\)
Đúng 2
Bình luận (0)
Hòa tan 30 g NaCl vào 170 gam nước, được dung dịch có khối lượng riêng 1,1 gam/ml. Tính nồng độ phần trăm và nồng độ mol của dung dịch thu được
\(C\%=\dfrac{30}{170}.100\%=17,647\%\)
\(V_{\text{dd}}=\left(30+170\right)1,1=220ml\)
\(n_{NaCl}=\dfrac{30}{58,5}=0,513mol\)
\(C_M=\dfrac{0,513}{0,22}=0,696M\)
\(C\%_{NaCl}=\dfrac{30}{170+30}.100\%=15\%\\ C_M=C\%.\dfrac{10D}{M}=10.\dfrac{10.1,1}{58,5}=1,88M\)
Đúng 1
Bình luận (1)