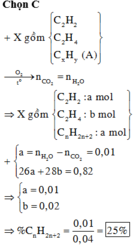Đốt cháy hoàn toàn 1 Hydro Cacbon A thu được CO2 và hơi nước H2O theo tỷ lệ khối lượng 11:3
a) Xác định công thức phân tử A. Biết dA/H2 = 20. Viết PTHH
b) Dẫn A vào dung dịch Brom dư, tính khối lượng sản phẩm

Những câu hỏi liên quan
Khi đốt cháy hoàn toàn hiđrocacbon A, thu được khí
C
O
2
và hơi nước theo tỉ lệ 77 : 18 về khối lượng. Nếu làm bay hơi hết 5,06 gam A thì thể tích hơi thu được đúng bằng thể tích của 1,76 g
O
2
ở cùng nhiệt độ và áp suất.1. Xác định công thức phân tử của chất A.2. Chất A không tác dụng với nước brom nhưng tác dụng được với dung dịch
K
M
n
O
4...
Đọc tiếp
Khi đốt cháy hoàn toàn hiđrocacbon A, thu được khí C O 2 và hơi nước theo tỉ lệ 77 : 18 về khối lượng. Nếu làm bay hơi hết 5,06 gam A thì thể tích hơi thu được đúng bằng thể tích của 1,76 g O 2 ở cùng nhiệt độ và áp suất.
1. Xác định công thức phân tử của chất A.
2. Chất A không tác dụng với nước brom nhưng tác dụng được với dung dịch K M n O 4 khi đun nóng. Viết công thức cấu tạo và tên chất A.
1. 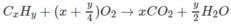
Theo đầu bài ta có: 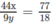
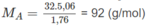
Tức là 12x + y = 92,0 ⇒ x = 7 ; y = 8
Công thức phân tử chất A là C 7 H 8 .
2. Công thức cấu tạo
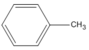 (metylbenzen (toluen))
(metylbenzen (toluen))
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn m gam chất X (chứa C, H, O) có công thức đơn giản nhất trùng công thức phân tử, (trong đó tổng khối lượng cacbon và hiđro bằng 0,46 gam) cần 0,896 lít
O
2
(đktc). Toàn bộ sản phẩm cháy dẫn vào dung dịch dư, thấy khối lượng dung dịch
Ca
(
OH
)
2
thu được sau phản ứng giảm 1,6 g so khối lượng dung dịch nước vôi trong ban đầu. Biết X...
Đọc tiếp
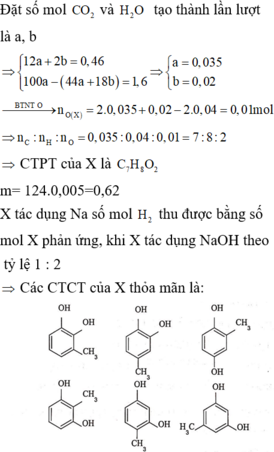
Đốt cháy hoàn toàn m gam chất X (chứa C, H, O) có công thức đơn giản nhất trùng công thức phân tử, (trong đó tổng khối lượng cacbon và hiđro bằng 0,46 gam) cần 0,896 lít O 2 (đktc). Toàn bộ sản phẩm cháy dẫn vào dung dịch dư, thấy khối lượng dung dịch Ca ( OH ) 2 thu được sau phản ứng giảm 1,6 g so khối lượng dung dịch nước vôi trong ban đầu. Biết X tác dụng Na số mol H 2 thu được bằng số mol X phản ứng, khi X tác dụng NaOH theo tỷ lệ 1 : 2. Giá trị m và đồng phân X thỏa mãn là
A. 0,6 và 4
B. 0,62 và 6
C. 0,6 và 5
D. 0,62 và 7
Đốt cháy hoàn toàn m gam chất X( C,H,O) có công thức đơn giản nhất trùng công thức phân tử, (trong đó tổng khối lượng cacbon và hiđro bằng 0,46 gam ) cần 0,896 lit O2(đktc). Toàn bộ sản phẩm cháy dẫn vào dung dịch Ca(OH)2 dư, thấy khối lượng dung dịch thu đựơc sau phản ứng giảm 1,6 g so khối lượng dung dịch nước vôi trong ban đầu. Biết X tác dụng Na số mol H2 thu được bằng số mol X phản ứng, khi X tác dụng NaOH theo tỷ lệ 1:2. Giá trị m và đồng phân X thỏa mãn là A. 0,6 và 4 B. 0,62 và 6 ...
Đọc tiếp
Đốt cháy hoàn toàn m gam chất X( C,H,O) có công thức đơn giản nhất trùng công thức phân tử, (trong đó tổng khối lượng cacbon và hiđro bằng 0,46 gam ) cần 0,896 lit O2(đktc). Toàn bộ sản phẩm cháy dẫn vào dung dịch Ca(OH)2 dư, thấy khối lượng dung dịch thu đựơc sau phản ứng giảm 1,6 g so khối lượng dung dịch nước vôi trong ban đầu. Biết X tác dụng Na số mol H2 thu được bằng số mol X phản ứng, khi X tác dụng NaOH theo tỷ lệ 1:2. Giá trị m và đồng phân X thỏa mãn là
A. 0,6 và 4
B. 0,62 và 6
C. 0,6 và 5
D. 0,62 và 7
Đáp án B
Đặt nC = x; nH = y
12x + y = 0,46 và 100x – 44x - 9y = 1,6 → x = 0,035; y = 0,04
nO = 0,035.2 + 0,04/2 – 0,04.2 = 0,01
C : H : O = 0,035 : 0,04 : 0,01 = 7 : 8 : 2 → C7H8O2
nX = nC/7 = 0,005 mol ; → mx = 0,62g
có 2 nhóm OH gắn vào vòng
o-HO-C6H4-OH có 2 vị trí gắn CH3
m- HO-C6H4-OH có 3 vị trí gắn CH3
p-HO-C6H4-OH có 1 vị trí gắn CH3
Vậy có 6 CTCT đúng
Đúng 0
Bình luận (0)
1 Dẫn 6,72 lít khí axetilen vào dung dịch brom dư. Khối lượng sản phẩm thu được là bao nhiêu? A 56,4 gamB 103,8 gamC 8,4 gamD 48 gam2 Đốt cháy hoàn toàn 2,8(g) một hiđrocacbon A trong không khí thu được 3,6 gam nước. Xác định công thức phân tử của A biết khối lượng mol của A là 28g/mol A C₂H₄B C₂H₂C CH₄D C₂H₆3 Nguyên tố có tính phi kim mạnh nhất là: A OxiB FloC CloD Nitơ4 Dãy các hợp chất nào sau đây là hợp chất hữu cơ? A C₆H₆, CH₄, C₂H₅OHB C₂H₂, C₂H₆O, CaCO₃C CH4, C₂H₆, CO₂D CH₄, C₂H₂, CO
Đọc tiếp
1 Dẫn 6,72 lít khí axetilen vào dung dịch brom dư. Khối lượng sản phẩm thu được là bao nhiêu?
A 56,4 gam
B 103,8 gam
C 8,4 gam
D 48 gam
2 Đốt cháy hoàn toàn 2,8(g) một hiđrocacbon A trong không khí thu được 3,6 gam nước. Xác định công thức phân tử của A biết khối lượng mol của A là 28g/mol
A C₂H₄
B C₂H₂
C CH₄
D C₂H₆
3 Nguyên tố có tính phi kim mạnh nhất là:
A Oxi
B Flo
C Clo
D Nitơ
4 Dãy các hợp chất nào sau đây là hợp chất hữu cơ?
A C₆H₆, CH₄, C₂H₅OH
B C₂H₂, C₂H₆O, CaCO₃
C CH4, C₂H₆, CO₂
D CH₄, C₂H₂, CO
Đốt cháy hoàn toàn 5.4g một hợp chất hữu cơ A thu được 8.4 lít co2 và 8.1g nước a. Tính khối lượng gam và phần trăm khối lượng nguyên tố có trong Á b. Xác định công thức đơn giản nhất của A c. Xác định công thức phân tử của A. Biết tỉ khối hơi của A so với oxi là 2.25 d. Viết các công thức cấu tạo của A
a)
\(n_{CO_2}=\dfrac{8,4}{22,4}=0,375\left(mol\right)\)
\(n_{H_2O}=\dfrac{8,1}{18}=0,45\left(mol\right)\)
Bảo toàn C: nC = 0,375 (mol)
Bảo toàn H: nH = 0,9 (mol)
mC = 0,375.12 = 4,5 (g)
mH = 0,9.1 = 0,9 (g)
=> mO = 5,4 - 4,5 - 0,9 = 0 (g)
=> \(\left\{{}\begin{matrix}\%C=\dfrac{4,5}{5,4}.100\%=83,33\%\\\%H=\dfrac{0,9}{5,4}.100\%=16,67\%\end{matrix}\right.\)
b)
nC : nH = 0,375 : 0,9 = 5 : 12
=> CTDGN: C5H12
c)
CTPT: (C5H12)n
Mà M = 2,25.32 = 72 (g/mol)
=> n = 1
=> CTPT: C5H12
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn m gam chất hữu cơ A cần dùng vừa đủ 15,4 lít (đktc) không khí, thu được hỗn hợp khí và hơi B chỉ gồm CO2, H2O và N2. Dẫn hỗn hợp B vào bình chứa dung dịch Ca(OH)2 dư, thu được 10 gam kết tủa. Sau thí nghiệm, khối lượng dung dịch sau phản ứng giảm 2,45 gam so với khối lượng nước vôi trong ban đầu và thấy thoát ra 12,88 lít khí (đktc). Biết phân tử khối của A nhỏ hơn 150 đvC và không khí chứa 20% O2 và 80% N2 về thể tích. a) Xác định công thức phân tử chất A. b) Xác định công th...
Đọc tiếp
Đốt cháy hoàn toàn m gam chất hữu cơ A cần dùng vừa đủ 15,4 lít (đktc) không khí, thu được hỗn hợp khí và hơi B chỉ gồm CO2, H2O và N2. Dẫn hỗn hợp B vào bình chứa dung dịch Ca(OH)2 dư, thu được 10 gam kết tủa. Sau thí nghiệm, khối lượng dung dịch sau phản ứng giảm 2,45 gam so với khối lượng nước vôi trong ban đầu và thấy thoát ra 12,88 lít khí (đktc). Biết phân tử khối của A nhỏ hơn 150 đvC và không khí chứa 20% O2 và 80% N2 về thể tích.
a) Xác định công thức phân tử chất A.
b) Xác định công thức cấu tạo thu gọn các chất: A, X, Y, Z và T, biết chúng thỏa mãn sơ đồ phản ứng sau:
A → + N a O H , t ∘ X → C a O + N a O H , t ∘ Y → 1500 ∘ C Z Z → H g S O 4 + H 2 O , 80 ∘ C T → A g N O 3 / N H 3 ; t ∘ A
a.

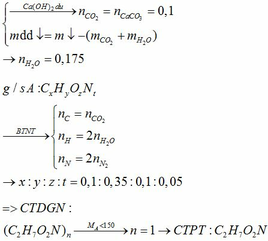
b.
Vì A pứ với NaOH nên CTCT của A là: CH3COONH4 hoặc HCOONH3CH3
Y pứ ở 15000C nên Y là: CH4
=> X: CH3COONa → A:CH3COONH4
Z: CH≡CH → T: CH3CHO
Vậy A là: CH3COONH4 (amoniaxetat)
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn hỗn hợp X gồm axetilen, etilen và hiđrocacbon A thu được CO2 và H2O theo tỉ lệ mol 1 : 1. Dẫn X đi qua bình đựng dung dịch brom dư thấy khối lượng bình tăng 0,82 gam, đốt cháy hoàn toàn khí thoát ra khỏi bình brom thu được 1,32 gam CO2 và 0,72 gam H2O. Phần trăm thể tích của A trong X là A. 50%. B. 75%. C. 25%. D. 33,33%.
Đọc tiếp
Đốt cháy hoàn toàn hỗn hợp X gồm axetilen, etilen và hiđrocacbon A thu được CO2 và H2O theo tỉ lệ mol 1 : 1. Dẫn X đi qua bình đựng dung dịch brom dư thấy khối lượng bình tăng 0,82 gam, đốt cháy hoàn toàn khí thoát ra khỏi bình brom thu được 1,32 gam CO2 và 0,72 gam H2O. Phần trăm thể tích của A trong X là
A. 50%.
B. 75%.
C. 25%.
D. 33,33%.
Cho a gam hỗn hợp X gồm hai α-aminoaxit no, hở chứa một nhóm amino, một nhóm cacboxyl tác dụng 40,15 gam dung dịch HCl 20% thu được dung dịch A. Để tác dụng hết các chất trong dung dịch A cần 140 ml dung dịch KOH 3M. Đốt cháy hoàn toàn a gam hỗn hợp X thu được sản phẩm cháy gồm CO2, H2O, N2 được dẫn qua bình đựng dung dịch Ca(OH)2 dư thấy khối lượng bình tăng 32,8 gam. Biết tỷ lệ khối lượng phân tử của chúng là 1,56. Aminoaxit có phân tử khối lớn là A. valin B. tyrosin C. lysin D. alanin
Đọc tiếp
Cho a gam hỗn hợp X gồm hai α-aminoaxit no, hở chứa một nhóm amino, một nhóm cacboxyl tác dụng 40,15 gam dung dịch HCl 20% thu được dung dịch A. Để tác dụng hết các chất trong dung dịch A cần 140 ml dung dịch KOH 3M. Đốt cháy hoàn toàn a gam hỗn hợp X thu được sản phẩm cháy gồm CO2, H2O, N2 được dẫn qua bình đựng dung dịch Ca(OH)2 dư thấy khối lượng bình tăng 32,8 gam. Biết tỷ lệ khối lượng phân tử của chúng là 1,56. Aminoaxit có phân tử khối lớn là
A. valin
B. tyrosin
C. lysin
D. alanin
Chọn đáp án A
Thực ra câu này với thủ đoạn của học sinh thời này sẽ thấy ngay
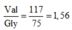
Nhưng mà mình cứ lác đác giải chi tiết ra
![]()
![]()
Vì X là
![]()
![]()
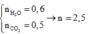
![]()
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 3,2g chất hữu cơ A thu được 8,8gam khí CO2 và 7,2 gam khí H2O a, Xác định công thức phân tử của A. Biết phân tử khối của A là 16 b, Viết phương trình hóa học đặc trưng của A c, Dẫn toàn bộ sản phẩm cháy vào bình đựng nước vôi trong dư. Tính khối lượng kết tủa tạo thành
a) Bảo toàn nguyên tố: \(\left\{{}\begin{matrix}n_C=n_{CO_2}=\dfrac{8,8}{44}=0,2\left(mol\right)\\n_H=2n_{H_2}=2\cdot\dfrac{7,2}{18}=0,8\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_C+m_H=0,2\cdot12+0,8\cdot1=3,2\left(g\right)=m_A\)
\(\Rightarrow\) Trong A không có Oxi
Xét tỉ lệ: \(n_C:n_H=2:8=1:4\)
Mà \(M_A=16\)
\(\Rightarrow\) Công thức phân tử của A là CH4 (Metan)
b) PTHH đặc trưng: \(CH_4+Cl_2\underrightarrow{a/s}CH_3Cl+HCl\)
c) Ta có: \(n_{CH_4}=\dfrac{3,2}{16}=0,2\left(mol\right)\)
Bảo toàn nguyên tố Cacbon: \(n_{CH_4}=n_{CaCO_3}=0,2\left(mol\right)\)
\(\Rightarrow m_{CaCO_3}=0,2\cdot100=20\left(g\right)\)
Đúng 3
Bình luận (0)