Giúp mình với!!!!
Đốt cháy hoàn toàn 23 gam hợp chất A sinh ra 44 gam khí CO2 và 27 gam H2O.
a) Có những nguyên tố nào cấu tạo nên hợp chất A?
b) Lập CTHH của A, biết rằng PTK của A nhỏ hơn PTK của CaO.
c) Viết PTHH của phản ứng giữa A với Oxi
đốt cháy hoàn toàn 4,6 gam chất A cần vừa đủ 6,72 lít khí Oxi (Đktc) thu được CO2 và H2O có tỉ lệ khối lượng là 44:27 . a) A tạo bởi những nguyên tố nào? b) tìm CT ĐG của A? c) Tìm CTHH của A biết dA/H2 là 23.
Ta có: \(n_{O_2}=0,3\left(mol\right)\)
Giả sử: \(\left\{{}\begin{matrix}n_{CO_2}=x\left(mol\right)\\n_{H_2O}=y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\dfrac{44x}{18y}=\dfrac{44}{27}\Leftrightarrow3x-2y=0\left(1\right)\)
Theo ĐLBT KL, có: mA + mO2 = mCO2 + mH2O.
\(\Rightarrow44x+18y=4,6+0,3.32\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=n_{CO_2}=0,2\left(mol\right)\\y=n_{H_2O}=0,3\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}n_C=0,2\left(mol\right)\\n_H=0,6\left(mol\right)\end{matrix}\right.\)
a, Vì đốt cháy A tạo CO2 và H2O nên A chắc chắn có C và H, có thể có O.
BTNT C và H, có: mC + mH = 0,2.12 + 0,6.1 = 3 (g) < mA.
Vậy: A gồm nguyên tố: C, H và O.
b, Ta có: mO = 4,6 - 3 = 1,6 (g)
\(\Rightarrow n_O=\dfrac{1,6}{16}=0,1\left(mol\right)\)
Giả sử CTPT của A là CxHyOz (x, y, z ∈ Z+)
⇒ x : y : z = 0,2 : 0,6 : 0,1 = 2 : 6 : 1
Vậy: CTĐGN của A là C2H6O.
c, Vì: dA/H2 = 23
⇒ MA = 23.2 = 46 (đvC)
Từ p/b, ta có A có dạng (C2H6O)n.
\(\Rightarrow n=\dfrac{46}{12.2+6+16}=1\)
Vậy: A là C2H6O.
Bạn tham khảo nhé!
a) BTKL mX+mO2=mCO2+mH2O
=>mCO2+mH2O=4,6+6,72/22,4.32=14,2g
b)ĐẶT nCO2=2x nH2O=3x
=>44.2x+18.3x=14,2 =>x=0,1
=>nC=nCO2=0,2 mol
nH2O=0,3 =>nH=2nH2O=2.0,3=0,6 mol
ta co 0,2.12+0,6.1=3g <4,6 => X có oxi =>mO=4,6-3=1,6g=>nO=0,1
gọi CT của X là CxHyOz
x:y:z=0,2:0,6:0,1=2:6:1
vậy CT của X là C2H6O
Đốt cháy hoàn toàn 23 gam hợp chất hữu cơ A thu được sản phẩm gồm 44 gam CO2 và 27 gam H2O.
a) Hỏi trong A có những nguyên tố nào?
b) Xác định công thức phân tử của A, biết tỉ khối của A so với hidro bằng 23.
Đốt cháy A thu được CO2 và H2O.
Vậy A chứa cacbon, hidro và có thể có oxi.
mC = 44/44 x 12 = 12 (gam)
mH = 27/18 x 2 = 3 (gam)
Theo đề bài, ta có mO = mA – mC – mH => mO = 23 – 12 – 3 = 8 (gam) Trong A có 3 nguyên tố C,H,O và có công thức CxHyOz
Theo đề bài ta có: MA/2 = 23, vậy mA = 46
Cứ 23 gam A có 12 gam cacbon 46 gam A có 12x gam cacbon
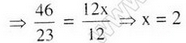
Tương tự ta có y = 6, z = 1
Vậy công thức của A là C2H6O
Đốt cháy hoàn toàn 4,2 gam hợp chất hữu cơ A, thu được 13,2g co2 và 5,4 gam H2O a) Hợp chất hữu cơ A gồm những nguyên tố nào? b) Lập công thức phân tử của A. Biết khối lượng mol của A nhỏ hơn 30g/mol. c) Hợp chất hữu cơ A có làm mất màu dung dịch Brom không, viết PTHH (nếu có
Bảo toàn C: \(n_C=n_{CO_2}=\dfrac{13,2}{44}=0,3\left(mol\right)\)
Bảo toàn H: \(n_H=2n_{H_2O}=2.\dfrac{5,4}{18}=0,6\left(mol\right)\)
\(n_O=\dfrac{4,2-\left(0,3.12+0,6\right)}{16}=0\left(mol\right)\)
`->` A gồm C và H
Đặt CTTQ A: CxHy
\(x:y=0,3:0,6=1:2\)
CT có dạng: \(\left(CH_2\right)_n< 30\)
\(\Leftrightarrow n< 2,14\)
`@` Chỉ có `n=2` thỏa mãn
`->` CTPT A: \(C_2H_4\)
CTCT: \(CH_2=CH_2\) `->` A làm mất màu dd Brom
\(CH_2=CH_2+Br_{2\left(dd\right)}\rightarrow CH_2Br-CH_2Br\)
Đốt hoàn toàn 1 dung lượng hợp chất hữu cơ AC gồm 2 nguyên tố, thu được 8,8 gam khí CO2 và 5,4 gam h2O. Hãy xác định công thức phân tử của A biết PTK của A bằng 30
A + O2 → CO2 + H2O
nCO2 = \(\dfrac{8,8}{44}\)= 0,2 mol => nC = nCO2= 0,2 mol => mC =0,2.12= 2,4 gam
nH2O = \(\dfrac{5,4}{18}\)= 0,3 mol=> nH = 2nH2O = 0,6 mol =>mH= 0,6.1 = 0,6 gam
Ta thấy mC + mH = 2,4+0,6 = 3 gam = mA
Vậy trong A chỉ chứa 2 nguyên tố là C và H
Giả sử CTĐGN của A là CxHy <=> CTPT của A là (CxHy)n
=> x : y = nC : nH = 1:3 => CTPT của A là (CH3)n
MA < 40 => 15n < 40 => n < 2,6 (n = 1,2)
n =1 => CTPT là CH3 ( vô lý )
=>n=2 và CTPT của A là C2H6
Bài 2: Đốt cháy hoàn toàn 4,4 gam hợp chất hữu cơ A thu được 13,2 gam khí CO2 và 7,2 gam nước. a) A có những nguyên tố nào? b) Tìm công thức phân tử của A biết khối lượng mol của A bằng 44 gam/mol c) Viết CTCT đầy đủ và thu gọn của A. Giúp với ạ mai e thi r
Đốt cháy hoàn toàn 2.25 gam một chất hữu cơ X thu được 3.36 lít khí co2(đo ở đktc) và 4.05 gam h2o
a)Chất X có những nguyên tố nào?
b)xác định công thức phân tử và viết công thức cấu tạo của X.Biết khối lượng mol của X nhỏ hơn 40gam/mol
a) Bảo toàn C: \(n_C=n_{CO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Bảo toàn H: \(n_H=2n_{H_2O}=2.\dfrac{4,05}{18}=0,45\left(mol\right)\)
Xét mC + mH = 0,15.12 + 0,45 = 2,25 (g)
=> X gồm C và H
b, CTPT của X có dạng CxHy
=> x : y = 0,15 : 0,45 = 1 : 3
=> (CH3)n < 40
=> n = 2
CTPT: C2H6
Bảo toàn C: \(n_C=n_{CO_2}=\dfrac{3,36}{22,4}=0,15mol\)
Bảo toàn H: \(n_H=2.n_{H_2O}=2.\dfrac{4,05}{18}=0,45mol\)
\(n_O=\dfrac{2,25-\left(0,15.12+0,45.1\right)}{16}=0mol\)
=> X chỉ có C và H
\(CTHH:C_xH_y\)
\(\rightarrow x:y=0,15:0,45=1:3\)
\(\rightarrow CTPT:CH_3\)
\(CTĐG:\left(CH_3\right)n< 40\)
\(\rightarrow n=1;2\)
\(n=1\rightarrow CTPT:CH_3\left(loại\right)\)
\(n=2\rightarrow CTPT:C_2H_6\left(nhận\right)\)
\(CTCT:CH_3-CH_3\)
\(X+O_2\underrightarrow{t^o}CO_2+H_2O\)
=> X gồm có nguyên tố C , H.
\(nCO_2=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
=> nC = 0,15(mol)
mC = 0,15 .12 = 1,8(g)
\(nH_2O=\dfrac{4,05}{18}=0,225\left(mol\right)\)
=> nH = 0,225 . 2 = 0,45(mol)
mH = 0,45 . 1 = 0,45 (g)
Vì mH + mC = 1,8 + 0,45 = 2,25 (g) = mX
=> X không có nguyên tố O.
Gọi CTHH đơn giản của X là CxHy
ta có : x : y = 0,15 : 0,45 = 1 : 3
=> CTHH đơn giản của X là CH3
ta có:
(CH3)n < 40
=> n = 2
=> CTPT của X là C2H6
CTCT của X là CH3 - CH3
đốt cháy hoàn toàn 6 gam hợp chất hữu cơ A thu được 8,8 gam khí CO2 và 3,6 gam H2O a) hợp chất chứa những nguyên tố hóa học nào ?
b)Xác định CTPT của A biết khối lượng mol của A là 60 gam
c) Viết CTCT chi tiết và thu gọn của A biết phân tử A có nhóm-COOH
d) Viết PTHH của A với dung dịch NaOH
GIÚP MÌNH VỚI Ạ MÌNH CẢM ƠN
\(n_{CO_2}=\dfrac{8,8}{44}=0,2\left(mol\right)\) -> \(n_C=0,2\)
\(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\) -> \(n_H=0,4\)
\(m_C+m_H=0,2.12+0,4=2,8\left(g\right)\)
-> Trong A có \(m_O=6-2,8=3,2\left(g\right)\)
\(n_O=\dfrac{3,2}{16}=0,2\left(mol\right)\)
Gọi CTPT của A là \(C_xH_yO_z\)
\(x:y:z=n_C:n_H:n_O=0,2:0,4:0,2=1:2:1\)
\(\Leftrightarrow\left(CH_2O\right)_n=60.\Rightarrow n=2\)
a. CTPT của A là \(C_2H_4O_2\)
b. CTCT thu gọn:
\(CH_3COOH\)
mình không gõ được CTCT chi tiết (bạn lên mạng xem nhé)
c. \(CH_3COOH+NaOH\rightarrow CH_3COONa+H_2O\)
1/ Đốt cháy hoàn toàn 9,2 gam một hợp chất hữư cơ A, sau phản ứng tạo ra 17,6 gam CO2 và 10,8 gam H2O.
a) Xác định công thức phân tử của A. Biết tỉ khối hơi của A so với khí hiđro là 23.
b) Viết các công thức cấu tạo có thể có của A.
2/ Đốt cháy hoàn toàn 1 lít khí hiđrocacbon cần 6 lít khí oxi, sinh ra 4 lít khí cacbonic. Các thể tích khí đo ở cùng nhiệt độ và áp suất.
a) Xác định công thức phân tử của hiđrocacbon.
b) Viết các công thức cấu tạo có thể có của hiđrocacbon đó.
1) Bảo toàn C: \(n_C=\dfrac{17,6}{44}=0,4\left(mol\right)\)
Bảo toàn H: \(n_H=\dfrac{10,8}{18}.2=1,2\left(mol\right)\)
Bảo toàn O: \(n_O=\dfrac{9,2-0,4.12-1,2}{16}=0,2\left(mol\right)\)
\(M_A=23.2=46\left(\dfrac{g}{mol}\right)\)
CTPT: CxHyOz
=> x : y : z = 0,4 : 1,2 : 0,2 = 2 : 6 : 1
=> (C2H6O)n = 46
=> n = 1
CTPT: C2H6O
CTCT:
(1) CH3-CH2-OH
(2) CH3-O-CH3
2) Ta có:
\(V_{C_xH_y}:V_{O_2}:V_{CO_2}=1:6:4\)
=> \(n_{C_xH_y}:n_{O_2}:n_{CO_2}=1:6:4\)
Bảo toàn C: \(x=n_C=n_{CO_2}=4\left(mol\right)\)
Bảo toàn O: \(n_{O\left(H_2O\right)}=2n_{O_2}-2n_{CO_2}=2.6-2.4=4\left(mol\right)\)
Bảo toàn H: \(n_H=2n_{H_2O}=2n_{O\left(H_2O\right)}=2.4=8\left(mol\right)\)
=> Trong 1 mol A chứa 4 mol C và 8 mol H
=> CTPT: C4H8
CTCT:
(1) CH2=CH-CH2-CH3
(2) CH3-CH=CH-CH3