Hoà tan 4g NaOH vào nước để được 400ml dung dịch:
1. Nồng độ mol của dung dịch thu được là:
2:Cần thêm bao nhiêu ml nước vào 100ml dung dịch này để được dung dịch có nồng độ 0,1M?
Trong 800ml của một dung dịch có chứa 8g NaOH.
a) Tính nồng độ mol của dung dịch này.
b) Phải thêm bao nhiêu ml nước vào 200ml dung dịch này để được dung dịch NaOH 0,1M?
a)
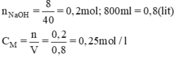
b) nNaOH có trong 200ml dung dịch NaOH 0,25M là

VH2O cần dùng để pha loãng 200ml dung dịch NaOH 0,25M để dung dịch NaOH 0,1M.
VH2O = 500 - 200 = 300ml H2O.
bài 2 :hoà tan 10g đường vào 100g nước được dung dịch nước đường . Tính nồng độ phần trăm của dung dịch nước đường thu được
bài3: hoà tan 4g NaOH vào nước được 200ml dung dịch . Tính nồng đọ mol của dung dịch thu được
Bài 2
\(C_{\%đường}=\dfrac{10}{10+100}\cdot100\%\approx9,09\%\)
Bài 3
\(n_{NaOH}=\dfrac{4}{40}=0,1mol\\ C_{M_{NaOH}}=\dfrac{0,1}{0,2}=0,5M\)
Hoà tan 4 gam NaOH vào nước để được 400 ml dung dịch. Nồng độ mol của dung dịch thu được là *
\(n_{NaOH}=\dfrac{4}{40}=0,1\left(mol\right)\\ C_{M_{NaOH}}=\dfrac{0,1}{0,4}=0,25\left(M\right)\)
n NaOH= \(\dfrac{4}{40}\)=0,1(mol)
C MnaoH=\(\dfrac{0,1}{0,4}\)=0,25(M)
Trong 400ml của một dung dich có chứa 120g NaOH
1) Hãy tính nồng độ mol của dung dịch này
2) Phải thêm bao nhiêu ml nước vào 200ml dung dịch này để được dung dịch NaOH 0,1gam/mol
1) nNaOH =120/40=3(mol)
CM(NaOH)=3/0,4=7,5 M
2) Nếu câu hỏi là NaOH 0,1 M
nNaOH=7,5.0,2=1,5(mol)
Số lít nước trong dung dịch: 1,5/0,1=15 (l)
=> Lượng nước cần thêm vào : 15 - 0,2=14,8 (l)=14800 ml
Cần thêm bao nhiêu ml nước vào 0,2 lít dung dịch NaOH 1M để được dung dịch mới nồng độ 0,1M?
n NaOH =0,2 mol
=>V dd mới =\(\dfrac{0,2}{0,1}\)=2 l
=>Thêm 1,8 lít nước
n NaOH =0,2 mol
=>V dd mới = \(\dfrac{0,2}{0,1}\) =2 l
=>Thêm 1,8 lít nước
Hòa tan 15,5g Na2O vào nước đc dung dịch A.
a)Tín nồng độ mol/l của dung dịch A.
b)tính thể tích dung dịch H2SO4 20%,khối lượng riêng là 1,14g/ml cần để trung hòa dung dịch A.
c)Tính nồng độ mol/l của chất có trong dung dịch sau khi trung hòa.
d)Hỏi phải thêm bao nhiêu lit nước vào 2l dung dịch NaOH 1M để thu được dung dịch có nồng độ 0,1M
a: hòa tan hoàn toàn 0,3 mol NaOH vào nước thu được 0,5 lít dung dịch NaOH. tính nồng độ mol của dung dịch?
b: hòa tan hoàn tàn 24 gam NaOH vào nước thu được 400ml dung dịch NaOH. tính nồng độ mol của dung dịch?
\(a,C_{M\left(NaOH\right)}=\dfrac{0,3}{0,5}=0,6M\\ b,n_{NaOH}=\dfrac{24}{40}=0,6\left(mol\right)\\ C_{M\left(NaOH\right)}=\dfrac{0,6}{0,4}=1,5M\)
Hoà tan 15,5g Na2O vào nước tạo thành 0,5 lít dung dịch. A/ tính nồng độ mol của dung dịch thu được. B/ tính thể tích dung dịch H2SO4 20% (d=1,14g/ml) cần để trung hoà dung dịch trên. C/ tính nồng độ mol của dung dịch sau phản ứng.
\(n_{Na_2O}=\dfrac{15,5}{62}=0,25\left(mol\right)\\ PTHH:Na_2O+H_2O\rightarrow2NaOH\\ n_{NaOH}=2.0,25=0,5\left(mol\right)\\ a,C_{MddNaOH}=\dfrac{0,5}{0,5}=1\left(M\right)\\ b,2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\\ n_{H_2SO_4}=n_{Na_2SO_4}=\dfrac{0,5}{2}=0,25\left(mol\right)\\ m_{H_2SO_4}=0,25.98=24,5\left(g\right)\\ m_{ddH_2SO_4}=\dfrac{24,5.100}{20}=122,5\left(g\right)\\ V_{ddH_2SO_4}=\dfrac{122,5}{1,14}\approx107,456\left(ml\right)\\ c,V_{ddsau}=V_{ddNaOH}+V_{ddH_2SO_4}\approx0,5+0,107456=0,607456\left(l\right)\\C_{MddNa_2SO_4}\approx\dfrac{ 0,25}{0,607456}\approx0,411552\left(M\right)\)
hoà tan hoàn toàn 11,2 gam KOH vào nước thu được 150 ml dung dịch .nồng độ mol của dung dịch thu được là bao nhiêu?
$n_{KOH} = \dfrac{11,2}{56} = 0,2(mol)$
$C_{M_{KOH}} = \dfrac{0,2}{0,15} = 1,33M$