Viết các phương trình hóa học.
a). Điều chế Natri Hiroxit
b) Điều chế khí clo từ dung dịch HCl đặm đặc
Từ M n O 2 , dung dịch H C l , K C l O 3 và cacbon, viết phương trình hóa học để điều chế các khí: clo, oxi, cacbon đioxit.
Viết phương trình hóa học điều chế khí clo từ M n O 2 , HCl, NaCl
Từ MnO2, dung dịch HCl, KClO3 và carbon, viết phương trình hóa học để điều chế các khí: Cl2, O2, CO2
\(MnO_2+4HCl\left(đ\right)-t^{^{ }0}->MnCl_2+Cl_2+2H_2O\\ KClO_3-t^{^0}->KCl+\dfrac{3}{2}O_2\\ C+O_2-t^{^{ }0}->CO_2\)
Trong phòng thí nghiệm hóa học có các kim loại kẽm và sắt, dung dịch HCl và axit H2SO4.
a) Viết các phương trình hóa học có thể điều chế hiđro;
b) Phải dùng bao nhiêu gam kẽm, bao nhiêu gam sắt để điều chế được 2,24 lít khí hiđro (đktc)?
Phương trình hóa học của phản ứng:
Fe + H2SO4 → FeSO4 + H2.
Zn + H2SO4 → ZnSO4 + H2.
Fe + 2HCl → FeCl2 + H2.
Zn + 2HCl → ZnCl2 + H2.
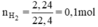
Theo phương trình (3) mFe cần dùng: 56.0,1 = 5,6g.
Theo phương trình (4) mZn cần dùng: 65.0,1 = 6,5g.
Bằng những phương pháp hóa học nào có thể điều chế Ag từ dung dịch AgNO3, điều chế Mg từ dung dịch MgCl2? Viết các phương trình hóa học.
Các phương pháp điều chế Ag từ AgNO3 là :
- Nhiệt phân :
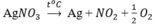
- Thủy luyện :
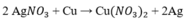
- Điện phân dung dịch :
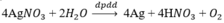
Phương pháp điều chế Mg từ MgCl2 là : điện phân nóng chảy MgCl2
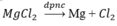
Từ Natri, không khí, nước và dung dịch sắt ( II ) clorua. Viết phương trình phản ứng hóa học điều chế sắt ( II ) hiđrôxit, sắt và sắt ( III ) clorua.
Biết rằng dụng cụ, hóa chất và điều kiện cần thiết có đầy đủ.
- Chuẩn bị và điều chế Fe(OH)2:
\(2Na+2H_2O--->2NaOH+H_2\uparrow\)
\(2NaOH+FeCl_2--->Fe\left(OH\right)_2+2NaCl\)
- Chuẩn bị và điều chế Fe(OH)3:
\(Fe\left(OH\right)_2\overset{t^o}{--->}FeO+H_2O\)
\(FeO+H_2\overset{t^o}{--->}Fe+H_2O\)
\(FeCl_2\overset{t^o}{--->}Fe+Cl_2\)
\(2FeCl_2+Cl_2\overset{t^o}{--->}2FeCl_3\)
Cho hình vẽ mô tả thí nghiệm điều chế khí Cl2 từ MnO2 và dung dịch HCl. a) Hãy viết phương trình phản ứng điều chế khí Cl2 (ghi rõ điều kiện). b) Giải thích tác dụng của bình (1) (đựng dung dịch NaCl bão hòa); bình (2) (đựng dung dịch H2SO4 đặc) và nút bông tẩm dung dịch NaOH ở bình (3)
PTHH: \(4HCl_{\left(đ\right)}+MnO_2\xrightarrow[]{t^o}MnCl_2+Cl_2\uparrow+2H_2O\)
- Bình đựng dd NaCl bão hòa để hấp thụ khí HCl
- Bình đựng dd H2SO4 đặc để hút nước
- Bông tẩm NaOH để tránh khí Clo bay ra ngoài
Viết các phương trình hoá học của phản ứng điều chế khí hiđro từ những chất sau : Zn, dung dịch HCl, dung dịch H 2 SO 4
Các phương trình hoá học điều chế khí hiđro :
Zn + 2HCl → ZnCl 2 + H2 ↑(1)
Zn + H 2 SO 4 → ZnSO 4 + H2 ↑(2)
từ các hóa chất Al, dung dịch HCl và hỗn hợp gồm CuO và Fe2O3, hãy nêu phương pháp và viết các phương trình hóa học điều chế Cu nguyên chất
Cho Al tác dụng với dung dịch HCl:
2Al + 6HCl -> 2AlCl3 + 3H2
Cho H2 khử hỗn hợp oxit:
Fe2O3 + 3H2 -> (t°) 2Fe + 3H2O
CuO + H2 -> (t°) Cu + H2O
Thả hỗn hợp kim loại vào dung dịch HCl:
Fe + 2HCl -> FeCl2 + H2
Cứ không phản ứng
Lọc lấy Cu tinh khiết.
- Hòa tan hh vào dd HCl dư, thu đc dd gồm CuCl2, FeCl3, HCldư:
\(CuO+2HCl\rightarrow CuCl_2+H_2O\)
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\)
- Thêm tiếp Al dư vào dd, thu được hh rắn gồm Cu, Fe, Aldư:
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(2Al+3CuCl_2\rightarrow2AlCl_3+3Cu\)
\(Al+FeCl_3\rightarrow AlCl_3+Fe\)
- Hòa tan hh rắn vào dd HCl dư, chất rắn không tan là Cu
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)