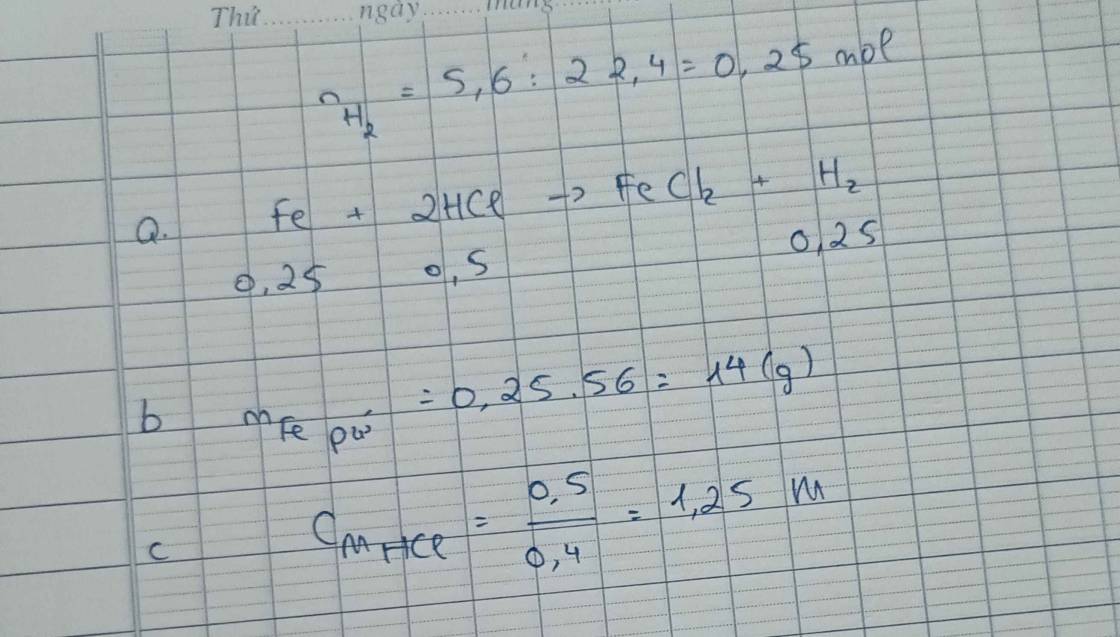Cho một lượng mạt sắt dư vào 50ml dung dịch HCL. Phản ứng xong thu được 3,36 lít khí Viết phương trình hóa học Tính khối lượng mạt sắt đã tham gia phản ứng Tìm nồng độ mol của dung dịch HCL đã dùng Giúp mình với

Những câu hỏi liên quan
Cho một khối lượng mạt sắt dư vào 50 ml dung dịch HCl .Phản ứng xong thu được 3,36 lít khí (đktc) . Viết phương trình hóa học .Tính khối lượng mạt sắt đã tham gia phản ứng Tính nồng độ mol của dung dịch HCl đã dùng .
Giải giúp mik với ạ
\(n_{H2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
a) Pt : \(Fe+2HCl\rightarrow FeCl_2+H_2|\)
1 2 1 1
0,15 0,3 0,15
b) \(n_{Fe}=\dfrac{0,15.1}{1}=0,15\left(mol\right)\)
⇒ \(m_{Fe}=0,15.56=8,4\left(g\right)\)
c) \(n_{HCl}=\dfrac{0,15.2}{1}=0,3\left(mol\right)\)
50ml = 0,05l
\(C_{M_{ddHCl}}=\dfrac{0,3}{0,05}=6\left(M\right)\)
Chúc bạn học tốt
Đúng 4
Bình luận (0)
Cho một khối lượng mạt sắt dư vào 50ml dung dịch HCl. Phản ứng xong thu được 3,36 lít khí (đktc).a) Viết phương trình hóa học.b) Tính khối lượng mạt sắt đã tham gia phản ứng.c) Tính nồng độ mol của dung dịch HCl đã dùng.d) Tính thể tích H2SO4 20% có khối lượng riêng 1,14 g/ml cần dùng để trung hoà 0,5 mol dung dịch NaOH.Biết: Fe56; H1; Cl35,5; Na23; O16; S32.
Đọc tiếp
Cho một khối lượng mạt sắt dư vào 50ml dung dịch HCl. Phản ứng xong thu được 3,36 lít khí (đktc).
a) Viết phương trình hóa học.
b) Tính khối lượng mạt sắt đã tham gia phản ứng.
c) Tính nồng độ mol của dung dịch HCl đã dùng.
d) Tính thể tích H2SO4 20% có khối lượng riêng 1,14 g/ml cần dùng để trung hoà 0,5 mol dung dịch NaOH.
Biết: Fe=56; H=1; Cl=35,5; Na=23; O=16; S=32.
a)
$Fe + 2HCl \to FeCl_2 + H_2$
b) Theo PTHH : $n_{Fe} = n_{H_2} = \dfrac{3,36}{22,4} = 0,15(mol)$
$m_{Fe} = 0,15.56 = 8,4(gam)$
c) $n_{HCl} = 2n_{H_2} = 0,3(mol)$
$\Rightarrow C_{M_{HCl}} = \dfrac{0,3}{0,05} = 6M$
d) $2NaOH + H_2SO_4 \to Na_2SO_4 + 2H_2O$
$n_{H_2SO_4} = \dfrac{1}{2}n_{NaOH} = 0,25(mol)$
$m_{dd\ H_2SO_4} = \dfrac{0,25.98}{20\%} = 122,5(gam)$
$V_{dd\ H_2SO_4} = \dfrac{122,5}{1,14} = 107,5(ml)$
Đúng 2
Bình luận (0)
: Cho một khối lượng mạt sắt dư vào 50 ml dung dịch HCl. Phản ứng xong, thu được 3,36 lít khí (đktc).
a. Tính khối lượng mạt sắt đã tham gia phản ứng.
b. Tìm nồng độ mol của dung dịch HCl đã dùng.
a) \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
____0,15<--0,3<-------------0,15
=> mFe = 0,15.56 = 8,4 (g)
b) \(C_{M\left(ddHCl\right)}=\dfrac{0,3}{0,05}=6M\)
Đúng 2
Bình luận (0)
Cho một khối lượng mạt sắt dư vào 50ml dung dịch HCl. Phản ứng xong, thu được 3,36 lít khí (đktc).
a) Viết pthh
b) tính khối lượng mạt sắt đã tham gia phản ứng.
c) tìm nồng độ mol của dd HCl đã dùng.
nH2=3.36/22.4=0.15 mol
a) PT: Fe + 2HCl ----> FeCl2 + H2
0.15 0.3 0.15
b)mFe=0.15*56=8.4g
c)CMHCl= 0.3*0.05=6 M
Chúc em học tốt!!!
Đúng 1
Bình luận (0)
Fe+2HCl->FeCl2+H2
nH2=0.15(mol)
Theo pthh nFe=nH2->nFe=0.15(mol)
mFe phản ứng:0.15*56=8.4(g)
nHCl=2nH2->nHCl=0.3(mol)
CM=0.3:0.05=6 M
Đúng 0
Bình luận (0)
a, Fe + 2HCl --> FeCl2 + H2
b, nH2=0,15 (mol)
nH2=nFe=> nFe= 0,15(mol)
=> mFe=0,15.56=8,4g
c,nH2=\(\frac{1}{2}\)nHCl => nHCl= 0,15.2=0,3 (mol)
đổi: 500lm=0,5 lit
=> CMHCl=\(\frac{0,3}{0,5}\)=0,6 M
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Câu 6: Cho một lượng mạt sắt dư vào 400 ml dung dịch HCl. Phản ứng xong, thu được 5,6 lít khí (đktc).a) Viết phương trình phản ứng.b) Tính khối lượng mạt sắt đã phản ứng.c) Tìm nồng độ mol của dung dịch HCl đã dùng.
Đọc tiếp
Câu 6: Cho một lượng mạt sắt dư vào 400 ml dung dịch HCl. Phản ứng xong, thu được 5,6 lít khí (đktc).
a) Viết phương trình phản ứng.
b) Tính khối lượng mạt sắt đã phản ứng.
c) Tìm nồng độ mol của dung dịch HCl đã dùng.
Cho 1lượng mạt sắt dư vào 250ml dung dịch HCL sau phản ứng thu được 9,9161 khí (đktc) a) viết phương trình hóa học b) tính khối lượng mạt sắt tham gia phản ứng b) tính nồng đọ mol của dung dịch đã dùng
\(Fe+2HCl\rightarrow FeCl_2+H_2\\ n_{Fe}=n_{H_2}=\dfrac{9,9161}{24,79}\approx0,4\left(mol\right)\\ b,m_{Fe}\approx0,4.56\approx22,4\left(g\right)\\ c,n_{HCl}\approx0,4.2\approx0,8\left(mol\right)\\ C_{MddHCl}\approx\dfrac{0,8}{0,25}\approx3,2\left(M\right)\)
Đúng 2
Bình luận (0)
\(a)Fe+2HCl\rightarrow FeCl_2+H_2\\ b)n_{H_2}=\dfrac{9,9161}{24,79}\approx0,4mol\\ n_{Fe}=n_{H_2}=0,4mol\\ m_{Fe}=0,4.56=22,4g\\ c)n_{HCl}=2n_{H_2}=2.0,4=0,8mol\\ 250ml=0,25l\\ C_{M_{HCl}}=\dfrac{0,8}{0,25}=3,2M\)
Đúng 0
Bình luận (0)
Cho một khối lượng mạt sắt dư vào 150mL dung dịch HCl. Sau phản ứng thu được 11,1555 lít khí (đkc)
a/ Viết PTHH. Tính khối lượng mạt sắt tham gia phản ứng
b/ Tính nồng độ mol của dung dịch HCl đã dùng
c/ Tính nồng độ mol dung dịch thu được
mọi người giúp mình với mình đang cần gấp
Bài 5. Cho một khối lượng mạt sắt dư vào 50 ml dung dịch HCl. Sau phản ứng thu được 3,36 lít khí (đktc).
b. Tính khối lượng mạt sắt tham gia phản ứng.
c. Tính nồng độ mol của dung dịch HCl đã dùng.
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
\(n_{Fe}=n_{H_2}=0,15\left(mol\right)\)
\(m_{Fe}=0,15.56=8,4\left(g\right)\)
\(n_{HCl}=2n_{H_2}=0,3\left(mol\right)\)
\(50ml=0,05l\)
\(C_{M_{ddHCl}}=\dfrac{0,3}{0,05}=6\left(M\right)\)
Đúng 1
Bình luận (0)
Cho 1 lượng mạt sắt dư vào 50 ml dung dịch HCl phản ứng thu được 3.36 lít khí h2 A tính khối lượng mạt sắt tham gia phản ứng B tính nồng độ mol dung dịch HCl đã dùng
\(n_{H_2}=\dfrac{3.36}{22.4}=0.15\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(0.15......0.3..................0.15\)
\(m_{Fe}=0.15\cdot56=8.4\left(g\right)\)
\(C_{M_{HCl}}=\dfrac{0.3}{0.05}=6\left(M\right)\)
Đúng 1
Bình luận (0)