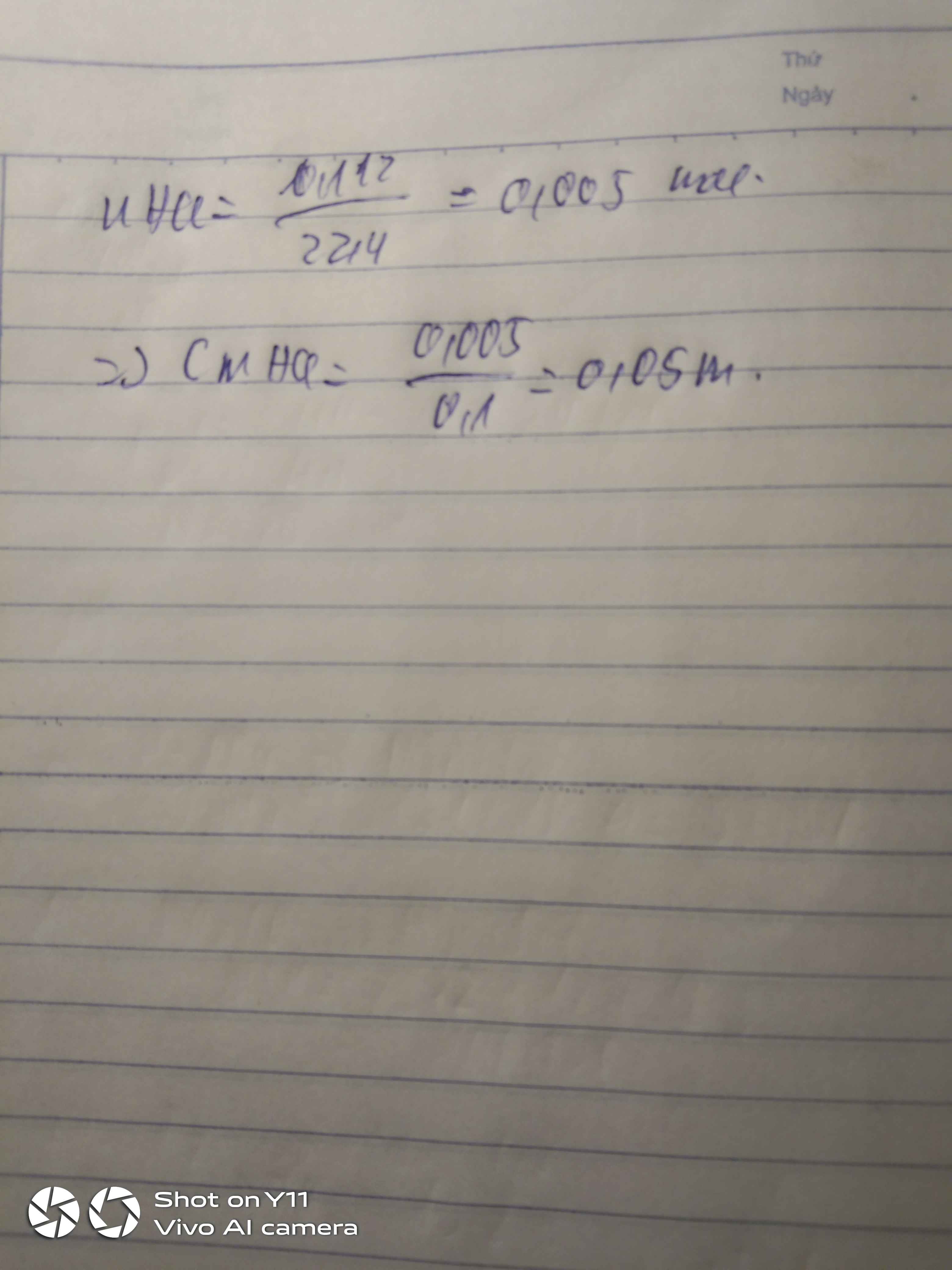CHo 4,9 gam H2SO4 vào 500 ml nước( khối lượng riêng của nước là 1g/ml )thì thu đc dd .Hãy xác định nồng độ % và nồng độ mol của dd . Biết khi cho chất tan vào thì thể tích không thay đổi đáng kể

Những câu hỏi liên quan
Hòa tan hoàn toàn 3g hỗn hợp E gồm đồng và bạc vào 500ml dd H2SO4 (d 1,84 g/ml) thu đc dd F trong đó lượng H2SO4 còn dư bằng 92,4% luoiwngj ban đầu. Đổ từ từ dd F vào 107,24 ml nước cất thì vừa đủ tạo thành 200g dd G1. XĐ thành phần % theo khối lượng của mỗi kim loại trong hỗn hợp E2. Tính nồng đọ C % các chất tan trong dd G và của dd H2SO4 ban đầu. Cho biết khối lượng riêng của nước bằng 1g/ml
Đọc tiếp
Hòa tan hoàn toàn 3g hỗn hợp E gồm đồng và bạc vào 500ml dd H2SO4 (d = 1,84 g/ml) thu đc dd F trong đó lượng H2SO4 còn dư bằng 92,4% luoiwngj ban đầu. Đổ từ từ dd F vào 107,24 ml nước cất thì vừa đủ tạo thành 200g dd G
1. XĐ thành phần % theo khối lượng của mỗi kim loại trong hỗn hợp E
2. Tính nồng đọ C % các chất tan trong dd G và của dd H2SO4 ban đầu. Cho biết khối lượng riêng của nước bằng 1g/ml
Câu 1: Tính khối lượng muối NaNO3 cần lấy để khi hòa tan vào 170 g nước thì thu được dung dịch có nồng độ 15 %
Câu 2: Hòa tan 75 g tinh thể CuSO4.5H2O vào trong nước thu được 900 ml dd CuSO4. Tính CM dd này
Câu 3: Khối lượng riêng dd CuSO4 là 1,206 g/ml. Đem cô cạn 414,594 ml dd này thu được 140,625 g tinh thể CuSO4.5H2O . Tính nồng độ mol và nồng độ % dd nói trên.
Câu 1 :
Khối lượng dung dịch là : \(m_{ct}+170\)
Gọi khối lượng muối \(NaNO_3\)cần dùng là x
Ta có :\(m_{ct}=\frac{C\%.m_{dd}}{100}\)
hay \(x=\frac{15.\left(x+170\right)}{100}\)
Ta tính được x=30 (g)
Vậy khối lượng \(NaNO_3\)cần lấy là 30 g
Đúng 1
Bình luận (0)
Câu 2 :
Số mol \(CuSO_4.5H_2O\)là :
\(n_{CuSO_4.5H_2O}=\frac{m}{M}=\frac{75}{250}=0,3\left(mol\right)\)
\(\Rightarrow n_{CuSO_4}=0,3\left(mol\right);V_{dd}=900ml=0,9l\)
\(C_{M_{dd}}=\frac{n}{V}=\frac{0,3}{0,9}=\frac{1}{3}M\)
Vậy...
Đúng 0
Bình luận (0)
Sục 4800ml (đkt) khí SO2 vào 84g dd KOH 20% (D=1,15g/ml)
a) tính khối lượng các chất thu đc sau pứ
b)DD thu đc sau pứ có nồng độ mấy mol/l ? coi thể tích dd thay đổi ko đáng kể
\(n_{SO_2}=\dfrac{3}{14}\left(mol\right);n_{KOH}=0,3\left(mol\right)\)
Lập tỉ lệ : \(\dfrac{n_{KOH}}{n_{SO_2}}=\dfrac{0,3}{\dfrac{3}{14}}=1,4\)
=> Thu được 2 muối sau phản ứng
\(SO_2+KOH\rightarrow KHSO_3\)
\(SO_2+2KOH\rightarrow K_2SO_3+H_2O\)
Gọi x,y là số mol KHSO3, K2SO3
\(\left\{{}\begin{matrix}x+y=\dfrac{3}{14}\\x+2y=0,3\end{matrix}\right.\)
=> \(x=\dfrac{9}{70};y=\dfrac{3}{35}\)
=> \(m_{KHSO_3}=\dfrac{108}{7}\left(g\right);m_{K_2SO_3}=\dfrac{474}{35}\left(g\right)\)
b) \(V=\dfrac{84}{1,15}=\dfrac{1680}{23}\left(ml\right)=\dfrac{42}{575}\left(l\right)\)
=> \(CM_{KHSO_3}=\dfrac{\dfrac{9}{70}}{\dfrac{42}{575}}=1,76M\)
\(CM_{K_2SO_3}=\dfrac{\dfrac{3}{35}}{\dfrac{42}{575}}=1,17M\)
Đúng 2
Bình luận (0)
hòa tan 112 ml khí HCl(đktc) vào trong 100ml nước biết thể tích dd thay đổi không đang kể tính nồng độ mol của dd HCl
Hòa tan hết 2.3 g kim lọai Na vào 1 cốc thủy tinh chứa 145.6g nuớc
Aviết pthh
B: tính thể tích của hiđro ở đktc
C:tính nồng độ % của dd sau khi phản ứng kết thúc
D:tính nồg độ mol của dd thu đk biết khối luợng riêq của nuớc là 1g|ml ( coi V dd thay đổi k đáng kể khi hòa tan chất rắn vào nuớc)
a) lập pthh của Pư
2Na + 2h20 → 2NaOH + H2
2mol 2mol 2mol 1mol
0,1mol 0,1mol 0,05mol
số mol của Na
nNa = \(\frac{2,3}{23}\)= 0,1mol
thể tích khí H2
Vh2 = 0,05 . 22,4 =1,12 lít
khối lượng NaOH
mNaOH = 0,1. 40= 4 gam
khối lượng dung dịch
mdd= mdm + mct = 145,6+ 4=149,6 gam
nồng độ % dd NaOH
C% = \(\frac{mct}{mdd}\). 100% =\(\frac{4}{149,6}\) .100% = 2,67%
thể tích dd NaOH
V = mddNaOH : D = 149,6 : 1 =149,6 ml
đổi 149,6 ml = 0,1496 lít
nồng độ mol dd NaOH
CM =\(\frac{n}{v}\) =\(\frac{0,1}{0,1496}\)=1,496 mol/ lít ![]()
Đúng 0
Bình luận (0)
Hòa tan 11,2 gam Fe vào 500 ml dung dịch H2 SO4
A, Tính thể tích khí H2 sinh ra (đktc)
B, Tính nồng độ mol dung dịch H2SO4 đã dùng
C,Tính nồng độ mol dung dịch muối thu được biết thể tích dung dịch thay đổi không đáng kể
\(n_{Fe}=\dfrac{11,2}{56}=0,2mol\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
0,2 0,2 0,2 0,2
a)\(V_{H_2}=0,2\cdot22,4=4,48l\)
b)\(C_{M_{H_2SO_4}}=\dfrac{0,2}{0,5}=0,4M\)
c)\(C_{M_{FeSO_4}}=\dfrac{0,2}{0,5}=0,4M\)
Đúng 1
Bình luận (0)
\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
pthh : \(Fe+H_2SO_4->FeSO_4+H_2\)
0,2 0,2
=> \(V_{H_2}=0,2.22,4=4,48\left(L\right)\)
\(m_{H_2SO_4}=\dfrac{0,5}{22,4}.98\approx2,188\left(g\right)\)
=> mdd=11,2+2,188=13,388(g)
C%=\(\dfrac{2,188}{13,388}.100\%=16,3\%\)
Đúng 2
Bình luận (0)
Hoà tan 0,5 mol CuSO4.5H2O vào 245g nước. Tính nồng độ %, nồng độ mol và suy ra khối lượng riêng của dung dịch (giả sử hoà tan không làm thay đổi thẻ tích dung dịch, Dnc = 1g/ml)
Cho 3,92g bột sắt vào 200ml đ CuSo4 10%(D=1,12g/ml)
a) Tính khối lượng kim loại mới tạo thành
b) Tính nồng độ mol của chất có trong dd sau phản ứng ( Giả thuyết cho thể tích dd thay đổi không đáng kể )
a, 4,48g
b,
Giải thích các bước giải:
mddCuSO4 = 200 . 1,12 = 224g
→ mCuSO4 = 224 . 10% = 22,4g
→ nCuSO4 = 22,4 : 160 = 0,14mol
nFe = 3,92 : 56 = 0,07 mol
Fe + CuSO4 → FeSO4 + Cu
nFe < nCuSO4 → Fe phản ứng hết, CuSO4 dư
nCu = nFe = 0,07 mol
→ mCu = 0,07 . 64 = 4,48g
Sau phản ứng thu được dung dịch gồm:
FeSO4: nFeSO4 = nFe = 0,07 mol
CuSO4 dư: nCuSO4 p.ứ = nFe = 0,07 mol → nCuSO4 dư = 0,14 - 0,07 = 0,07 mol
Đúng 0
Bình luận (0)
a, 4,48g
b,
Giải thích các bước giải:
mddCuSO4 = 200 . 1,12 = 224g
→ mCuSO4 = 224 . 10% = 22,4g
→ nCuSO4 = 22,4 : 160 = 0,14mol
nFe = 3,92 : 56 = 0,07 mol
Fe + CuSO4 → FeSO4 + Cu
nFe < nCuSO4 → Fe phản ứng hết, CuSO4 dư
nCu = nFe = 0,07 mol
→ mCu = 0,07 . 64 = 4,48g
Sau phản ứng thu được dung dịch gồm:
FeSO4: nFeSO4 = nFe = 0,07 mol
CuSO4 dư: nCuSO4 p.ứ = nFe = 0,07 mol → nCuSO4 dư = 0,14 - 0,07 = 0,07 mol
Đúng 0
Bình luận (0)
a, 4,48g
b,
Giải thích các bước giải:
mddCuSO4 = 200 . 1,12 = 224g
→ mCuSO4 = 224 . 10% = 22,4g
→ nCuSO4 = 22,4 : 160 = 0,14mol
nFe = 3,92 : 56 = 0,07 mol
Fe + CuSO4 → FeSO4 + Cu
nFe < nCuSO4 → Fe phản ứng hết, CuSO4 dư
nCu = nFe = 0,07 mol
→ mCu = 0,07 . 64 = 4,48g
Sau phản ứng thu được dung dịch gồm:
FeSO4: nFeSO4 = nFe = 0,07 mol
CuSO4 dư: nCuSO4 p.ứ = nFe = 0,07 mol → nCuSO4 dư = 0,14 - 0,07 = 0,07 mol
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Cho 3,2 gam bột sắt vào 100ml dung dịch CuSO4 10% có khối lượng riêng là 1,12g/ml
a) Viết PTHH
b) Xác định nồng độ mol của các chất trong dung dịch thu được sau p/ư. Gỉa thiết thể tshc dung dịch thay đổi không đáng kể
a/ PTHH: Fe + CuSO4 ===> FeSO4 + Cu
0,057 0,057 0,057
b/ Áp dụng công thức m = D x V
=> mdd CuSO4 = 100 x 1,12 = 112 gam
=>mCuSO4 = 112 x 10% = 11,2 gam
=> nCuSO4 = 11,2 / 160 = 0,07 mol
nFe= 3,2 / 56 = 0,057 mol
Lập tỉ lệ theo phương trình => Fe hết, CuSO4 dư
Lập các sô mol trên phương trình
=> Dung dịch thu đc chứa FeSO4 và CuSO4
=> CM(FeSO4)= 0,057 / 0,1 = 0,57M
CM(CuSO4) = \(\frac{0,07-0,057}{0,1}\) = 0,13M
Chúc bạn học tốt!!!
Đúng 1
Bình luận (0)