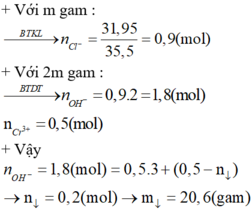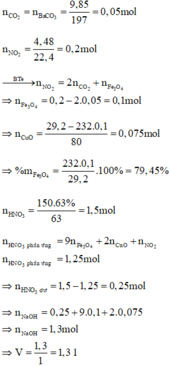Hòa tan hoàn toàn một hỗn hợp gồm CuO và ZnO cần 400ml dung dịch HCl 1M. Sau phản ứng thu được một dung dịch A. Cho V lít dung dịch NaOH vào dung dịch A thu được m (gam) kết tủa.
a/ Viết phương trình phản ứng xảy ra.
b/ Tính khối lượng mỗi oxit ban đầu.
c/ Tính V cần cho phản ứng hết các chất trong A.
d/ Tính m.