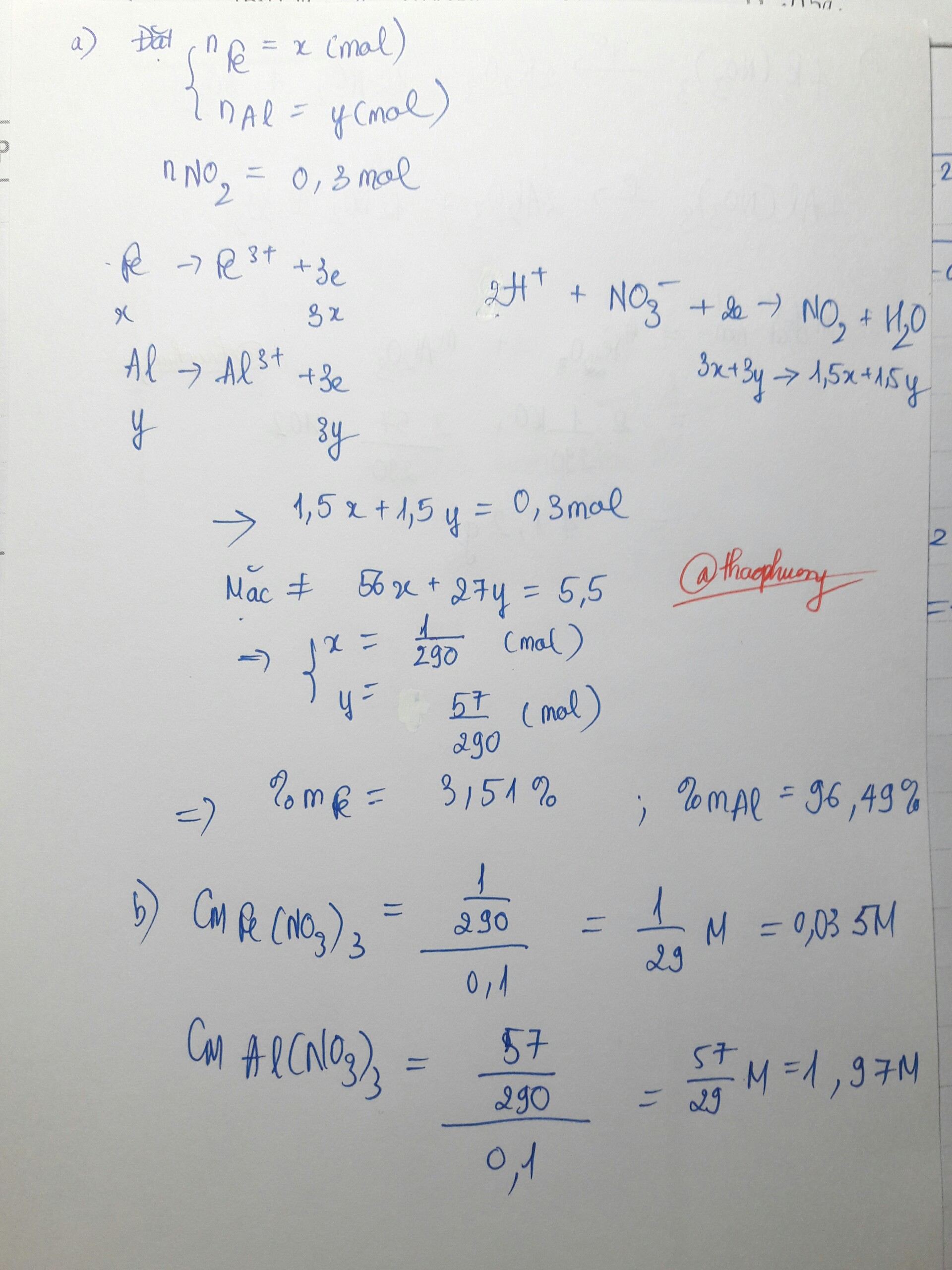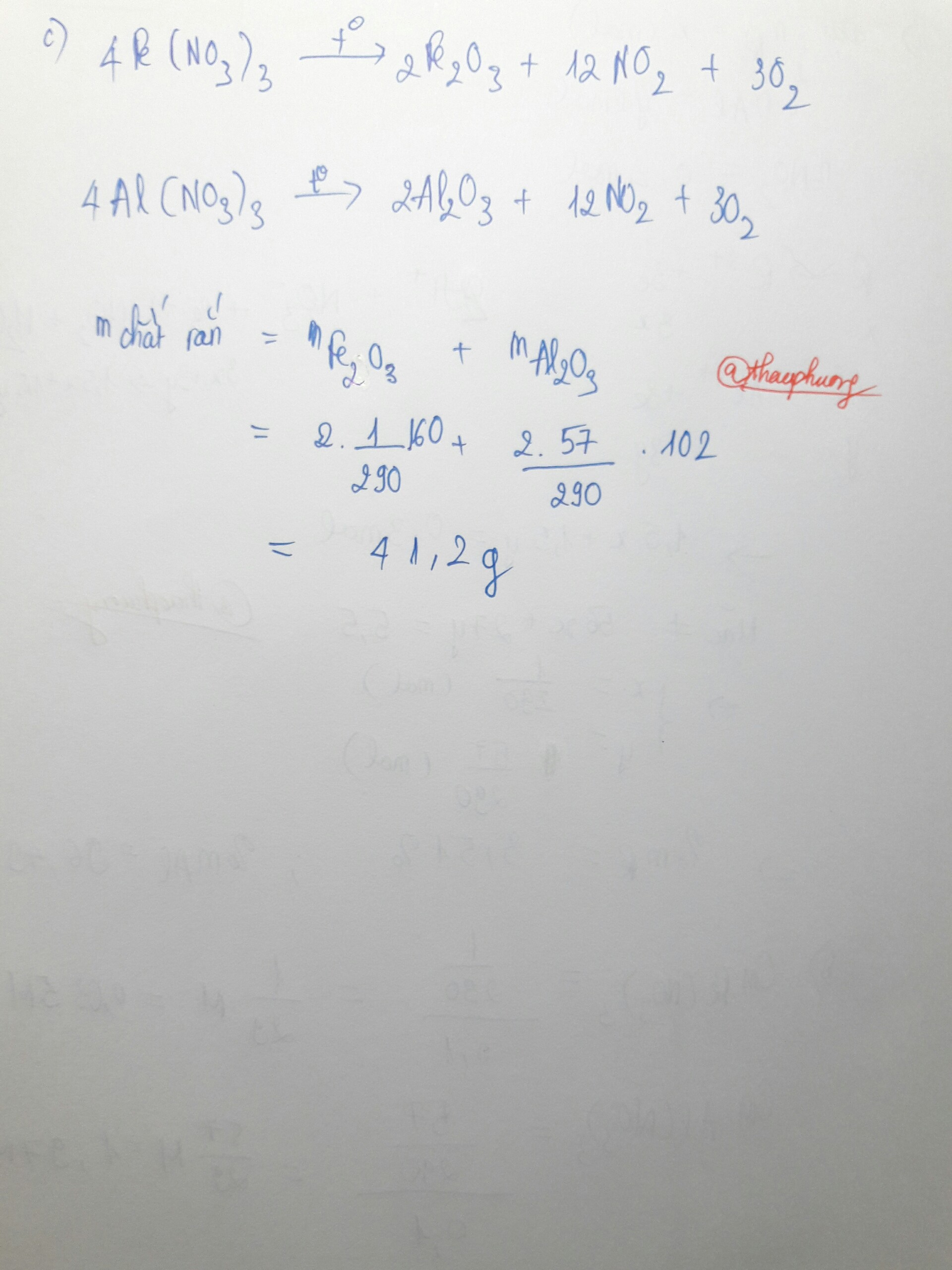hòa tan hoàn toàn 20,8g hợp kim Fe và Cu bằng dd HNO3 đặc nóng dư thu được 20,16 (l) NO2 (đktc). Xác định thành phần % theo khối lượng của mỗi kim loại ban đầu?

Những câu hỏi liên quan
Hòa tan hoàn toàn 9,10 gam hỗn hợp X ở dạng bột gồm Cu,Al bằng 400ml dung dịch HNO3 đặc nóng(vừa đủ) thu được 11,2 lít NO2 (ở đktc). a) Xác định thành phần % về khối lượng mỗi kim loại có trong hỗn hợp X b) Tính nồng độ mol của HNO3 tham gia phản ứng c) Cho dung dịch NaOH dư vào dung dịch thu được bao nhiêu gam kết tủa
Hòa tan 1,52 gam kim lọai Mg và Cu vào dd HNO3 đặc, nóng dư thu được duy nhất 1,344 lít (đktc) khí màu nâu. a. Tính thành phần % theo khối lượng của mỗi chất ban đầu. b. Tính khối lượng muối tạo thành.
a) Gọi số mol Mg, Cu là a,b
=> 24a + 64b = 1,52
\(n_{NO_2}=\dfrac{1,344}{22,4}=0,06\left(mol\right)\)
Mg0 - 2e --> Mg+2
a---->2a---->a
Cu0 - 2e --> Cu+2
b---->2b---->b
N+5 +1e--> N+4
___0,06<--0,06
Bảo toàn e: 2a + 2b = 0,06
=> \(\left\{{}\begin{matrix}a=0,01\\b=0,02\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%Mg=\dfrac{24.0,01}{1,52}.100\%=15,79\%\\\%Cu=\dfrac{64.0,02}{1,52}.100\%=84,21\%\end{matrix}\right.\)
b) \(m_{Mg\left(NO_3\right)_2}=0,01.148=1,48\left(g\right)\)
\(m_{Cu\left(NO_3\right)_2}=0,02.188=3,76\left(g\right)\)
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 7,6g hỗn hợp gồm đồng và sắt vào dung dịch HNO3 2M loãng dư thì thu được 2240ml khí thoát ra và khí này hóa nâu trong không khí (đktc).
a. Xác định thành phần phần trăm theo khối lượng của mỗi kim loại trong hỗn hợp ban đầu.
b. Tính thể tích dung dịch HNO3 đã dùng, biết rằng đã dùng dư 10% so với lượng phản ứng.
c. Tính nồng độ các chất trong dung dịch sau phản ứng (coi thể tích thay đổi không đáng kể).
Đọc tiếp
Hòa tan hoàn toàn 7,6g hỗn hợp gồm đồng và sắt vào dung dịch HNO3 2M loãng dư thì thu được 2240ml khí thoát ra và khí này hóa nâu trong không khí (đktc). a. Xác định thành phần phần trăm theo khối lượng của mỗi kim loại trong hỗn hợp ban đầu. b. Tính thể tích dung dịch HNO3 đã dùng, biết rằng đã dùng dư 10% so với lượng phản ứng. c. Tính nồng độ các chất trong dung dịch sau phản ứng (coi thể tích thay đổi không đáng kể).
Nung nóng 3,72g hỗn hợp bột các kim loại Zn và Fe trong bột S dư. Chất rắn thu được sau phản ứng được hòa tan hoàn toàn bằng dung dịch H2SO4 loãng, nhận thấy có 1,344 lít khí (đktc) thoát ra. Xác định khối lượng mỗi kim loại trong hỗn hợp ban đầu.
Đặt nZn = x mol; nFe = y mol.
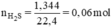
Ta có hệ phương trình: 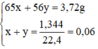
Giải hệ phương trình trên ta được:
x = 0,04 mol, y = 0,02 mol.
mZn = 65 × 0,04 = 2,6g
mFe = 56 × 0,02 = 1,12g
Đúng 1
Bình luận (0)
Hòa tan 1,5 g hỗn hợp Cu, Al, Mg vào dd HCl thu được 5,6 lít khí ở đktc và phần không tan. Cho phần không tan vào H2SO4 đặc nóng dư thu được 2,24 lít khí. Xác định khối lượng mỗi kim loại trong hỗn hợp
2Al+6HCl->2AlCL3+3H2(1)
Mg+2HCL->MgCL2+H2(2)
Cu+2H2SO4(đặc)->CuSO4+SO2+2H2O(3)
(3)=>nCu=nSO2=2,24/22,4=0,1mol
=>mCu=0,1.64=6,4g ???? lớn hơn m hỗn hợp đề chắc sai
Đúng 1
Bình luận (0)
Cho 3,68 gam hỗn hợp sắt và magie phản ứng hoàn toàn với dung dịch HNO3 đặc, nóng thu được 5,376 lít khí NO2 duy nhất (đktc). Xác định thành phần phần trăm khối lượng mỗi kim loại trong hỗn hợp và tính khối lượng axit đã phản ứng.
\(3,68g\left\{{}\begin{matrix}Fe\\Mg\end{matrix}\right.+HNO3->\left\{{}\begin{matrix}Fe\left(NO3\right)3\\Mg\left(NO3\right)2\end{matrix}\right.+5,376\left(l\right)NO2\)
Bảo toàn e :
\(3x+2y=0,24\)
Ta có :
\(\left\{{}\begin{matrix}56x+24y=3,68\\3x+2y=0,24\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,04\left(mol\right)\\y=0,06\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%mFe=\dfrac{0,04.56}{3,68}=60,87\%\\\%mMg=\dfrac{0,06.24}{3,68}=39,13\%\end{matrix}\right.\)
Bảo toàn nguyên tố Fe và Mg :
\(nFe=nFe\left(NO3\right)3=0,04\left(mol\right)\)
\(nMg=nMg\left(NO3\right)2=0,06\left(mol\right)\)
Ta có : \(nHNO3pu=0,04.3+0,06.2=0,24\left(mol\right)\)
\(\Rightarrow mHNO3=0,24.63=15,12\left(g\right)\)
Đúng 1
Bình luận (2)
Hòa tan hoàn toàn 5,5g hỗn hợp Fe và Al bằng 100ml dung dịch HNO3 đặc, nóng, dư. Sau phản ứng thu được 6,72 lit khí NO2 màu nâu đỏ (đktc).a)Tính % khối lượng mỗi kim loại trong hỗn hợp đầu.b)Tính Cm các muối trong dung dịch sau phản ứng, coi thể tích dung dịch thay đổi không đáng kể.c)Nhiệt phân hoàn toàn lượng muối thu được ở trên. Tính khối lượng chất rắn và thể tích khí (đktc) thu được sau phản ứng
Đọc tiếp
Hòa tan hoàn toàn 5,5g hỗn hợp Fe và Al bằng 100ml dung dịch HNO3 đặc, nóng, dư. Sau phản ứng thu được 6,72 lit khí NO2 màu nâu đỏ (đktc).
a)Tính % khối lượng mỗi kim loại trong hỗn hợp đầu.
b)Tính Cm các muối trong dung dịch sau phản ứng, coi thể tích dung dịch thay đổi không đáng kể.
c)Nhiệt phân hoàn toàn lượng muối thu được ở trên. Tính khối lượng chất rắn và thể tích khí (đktc) thu được sau phản ứng
Hòa tan hết 2,36 gam hỗn hợp Ag và Cu vào dung dịch HNO3 đặc, nóng (dư) thu được 1,12 lít khí NO2 duy nhất (điều kiện tiêu chuẩn).Tính % về khối lượng mỗi kim loại trong hỗn hợp ban đầu?
Ta có: \(n_{NO_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
Theo đề bài: \(108n_{Ag}+64n_{Cu}=2,36\) (1)
Bảo toàn electron: \(n_{Ag}+2n_{Cu}=n_{NO_2}=0,05\) (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Ag}=0,01\left(mol\right)\\n_{Cu}=0,02\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}\%m_{Ag}=\dfrac{108\cdot0,01}{2,36}\cdot100\%\approx45,76\%\\\%m_{Cu}=54,24\%\end{matrix}\right.\)
Đúng 2
Bình luận (0)
Ag + 2HNO3 ⟶ AgNO3 + H2O + NO2
Cu + 4HNO3 → Cu(NO3)2 + 2NO2↑ + 2H2O
\(n_{NO_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
Gọi x,y lần lượt là số mol Ag, Cu
Ta có : \(\left\{{}\begin{matrix}108x+64y=2,36\\x+2y=0,05\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}x=0,01\\y=0,02\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}m_{Ag}=0,01.108=1,08\left(g\right)\\m_{Cu}=0,02.64=1,28\left(g\right)\end{matrix}\right.\)
=> \(\%m_{Ag}=\dfrac{1,08}{2,36}.100=45,76\%\)
=>%mCu = 100 - 45,76 =54,24%
Đúng 2
Bình luận (0)
Số mol của khí nito đioxxit
nNO2= \(\dfrac{V_{NO2}}{22,4}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
Pt : Cu + 4HNO3 → Cu(NO3)2 + 2NO2 + 2H2O\(|\)
1 4 1 2 2
0,025 0,05
Số mol của đồng
nCu = \(\dfrac{0,05.1}{2}=0,025\left(mol\right)\)
Khối lượng của đồng
mCu = nCu . MCu
= 0,025 . 64
= 1,6 (g)
Khối lượng của bạc
mAg = 2,36 - 1,6
= 0,76 (g)
0/0 mCu= \(\dfrac{m_{Cu}.100}{m_{hh}}=\dfrac{1,6.100}{2,36}=67,8\)0/0
0/0mAg = \(\dfrac{m_{Ag}.100}{m_{hh}}=\dfrac{0,76.100}{2,36}=32,2\)0/0
Chúc bạn học tốt
Đúng 0
Bình luận (2)
Hòa tan hết 6,95 gam hỗn hợp Al và Fe vào dung dịch HNO3 đặc, nóng (dư) thu được 10,08 lít khí NO2 duy nhất (điều kiện tiêu chuẩn). Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu
\(n_{Al}=a\left(mol\right),n_{Fe}=b\left(mol\right)\)
\(m=27a+56b=6.95\left(g\right)\left(1\right)\)
\(n_{NO_2}=\dfrac{10.08}{22.4}=0.45\left(mol\right)\)
Bảo toàn e :
\(3a+3b=0.45\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.05,b=0.1\)
\(m_{Al}=0.05\cdot27=1.35\left(g\right)\)
\(m_{Fe}=0.1\cdot56=5.6\left(g\right)\)
Đúng 2
Bình luận (0)