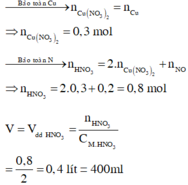Cho 19,2g một kim loại A tác dụng hết với dung dịch HNO3 2M thu được 4,48 lít khí NO ( đktc, sản phẩm khử duy nhất) Tìm A, tính khối lượng muối và thể tích dung dịch HNO3 cần dùng?

Những câu hỏi liên quan
Cho 19,2g một kim loại A tác dụng hết với dung dịch HNO3 2M thu được 4,48 lít khí NO ( đktc, sản phẩm khử duy nhất) Tìm A, tính khối lượng muối và thể tích dung dịch HNO3 cần dùng?
Cho Mg tác dụng với 200 ml dung dịch HNO3 thu được 4,48 lít khí NO2 (đktc) (sản phẩm khử duy nhất)
a) Tìm khối lượng kim loại Mg đã phản ứng
b) Tìm CM của axit đã dùng.
a) \(n_{NO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: Mg + 4HNO3 --> Mg(NO3)2 + 2NO2 + 2H2O
0,1<--0,4<------------------------0,2
=> mMg = 0,1.24 = 2,4 (g)
b) \(C_M=\dfrac{0,4}{0,2}=2M\)
Đúng 0
Bình luận (0)
Cho 11,2 gam hỗn hợp Cu và kim loại M tác dụng với dung dịch HCl dư thu được 3,136 lít (đktc). Cũng lượng hỗn hợp này cho tác dụng hết với dung dịch HNO3 loãng thu được 3,92 lít khí NO (đktc, sản phẩm khử duy nhất). Kim loại M là :
A. Mg B. Fe C. Mg hoặc Fe D. Mg hoặc Zn
Gọi số mol Cu, M là a, b (mol)
=> 64a + b.MM = 11,2 (1)
\(n_{NO}=\dfrac{3,92}{22,4}=0,175\left(mol\right)\)
Cu0 - 2e --> Cu+2
a--->2a
M0 - ne --> M+n
b--->bn
N+5 + 3e --> N+2
0,525<-0,175
Bảo toàn e: 2a + bn = 0,525 (2)
(1)(2) => 32bn - bMM = 5,6 (3)
\(n_{H_2}=\dfrac{3,136}{22,4}=0,14\left(mol\right)\)
PTHH: 2M + 2xHCl --> 2MClx + xH2
\(\dfrac{0,28}{x}\)<---------------------0,14
=> \(\dfrac{0,28}{x}=b\) (4)
(3)(4) => MM = 32n - 20x (g/mol)
Và \(0< x\le n\)
TH1: x = n = 1 => MM = 12 (Loại)
TH2: x = n = 2 => MM = 24 (Mg)
TH3: x = n = 3 => MM = 36 (Loại)
TH4: x = 1; n = 2 => MM = 44 (Loại)
TH5: x = 1; n = 3 => MM = 76 (Loại)
TH6: x = 2; n = 3 => MM = 56 (Fe)
Vậy M có thể là Mg hoặc Fe
=> C
Đúng 1
Bình luận (0)
Cho 7,55 gam hỗn hợp X gồm các kim loại Fe, Al, Cu tác dụng với dung dịch HNO3 loãng dư thu được 2,8 lít khí NO ( sản phẩm khử duy nhất ở đktc) và dung dịch Y chứa các muối có khối lượng là A. 30,8 gam. B. 69,55 gam C. 38,55 gam D. 15,3 gam
Đọc tiếp
Cho 7,55 gam hỗn hợp X gồm các kim loại Fe, Al, Cu tác dụng với dung dịch HNO3 loãng dư thu được 2,8 lít khí NO ( sản phẩm khử duy nhất ở đktc) và dung dịch Y chứa các muối có khối lượng là
A. 30,8 gam.
B. 69,55 gam
C. 38,55 gam
D. 15,3 gam
Đáp án A
nNO = 2,8/22,4 = 0,125 (mol)
BTNT N: nNO3 ( trong muối) = 3nNO = 0,375 (mol)
=> mmuối = mKL + mNO3- = 7,55 + 0,375.62 = 30,8 (g)
Đúng 0
Bình luận (0)
Cho Zn tác dụng với 200 ml dung dịch HNO3 4M thu được dung dịch muối và khí NO (sản phẩm khử duy nhất)
a) Viết phương trình hóa học của phản ứng trên.
b) Tìm khối lượng của kim loại Zn đã dùng.
c) Tìm thể tích khí sinh ra ở điều kiện tiêu chuẩn
a) 3Zn + 8HNO3 --> 3Zn(NO3)2 + 2NO + 4H2O
b) \(n_{HNO_3}=0,2.4=0,8\left(mol\right)\)
PTHH: 3Zn + 8HNO3 --> 3Zn(NO3)2 + 2NO + 4H2O
0,3<----0,8----------------------->0,2
=> mZn = 0,3.65 = 19,5 (g)
c) VNO = 0,2.22,4 = 4,48(l)
Đúng 1
Bình luận (0)
Đốt cháy 6,72g kim loại M với oxi dư thu được 8,4g oxit. Nếu cho 5,04g M tác dụng hết với dung dịch HNO3 dư thu được dung dịch X và khí NO (sản phẩm khử duy nhất). Thể tích khí NO ở đktc là
A. 1,176 lít.
B. 2,016 lít.
C. 2,24 lít.
D. 1,344 lít.
Đáp án A
mO = 8,4 – 6,72 = 1,68g (0,105 mol)
6,72g M cần 0,105 mol O => 5,04g M cần 0,07875
Ta có 2nO = 3nNO => nNO = 0,0525 => VNO = 1,176 lít
Đúng 0
Bình luận (0)
Đốt cháy 6,72g kim loại M với oxi dư thu được 8,4g oxit. Nếu cho 5,04g M tác dụng hết với dung dịch HNO3 dư thu được dung dịch X và khí NO (sản phẩm khử duy nhất). Thể tích khí NO ở đktc là A. 1,176 lít B. 2,016 lít C. 2,24 lít D. 1,344 lít
Đọc tiếp
Đốt cháy 6,72g kim loại M với oxi dư thu được 8,4g oxit. Nếu cho 5,04g M tác dụng hết với dung dịch HNO3 dư thu được dung dịch X và khí NO (sản phẩm khử duy nhất). Thể tích khí NO ở đktc là
A. 1,176 lít
B. 2,016 lít
C. 2,24 lít
D. 1,344 lít
Đáp án A
mO = 8,4 – 6,72 = 1,68g (0,105 mol)
6,72g M cần 0,105 mol O => 5,04g M cần 0,07875
Ta có 2nO = 3nNO => nNO = 0,0525 => VNO = 1,176 lít
Đúng 0
Bình luận (0)
Cho 19,2g kim loại M tác dụng với dung dịch HNO3 loãng dư thu được 4,48 lít khí duy nhất NO(đktc). Kim loại M là:
A. Mg.
B. Cu.
C. Fe.
D. Zn.
Đáp án B
Số mol NO là 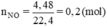
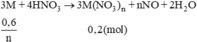
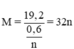 → {n = 2, M = 64)} ⇒ M là Cu
→ {n = 2, M = 64)} ⇒ M là Cu
Đúng 0
Bình luận (0)
Cho Cu tác dụng với dung dịch
HNO
3
theo sơ đồ sau:
Cu
+
HNO
3
→
Cu
(
NO
3
)
2
+
NO
↑
+
H
2...
Đọc tiếp
Cho Cu tác dụng với dung dịch HNO 3 theo sơ đồ sau: Cu + HNO 3 → Cu ( NO 3 ) 2 + NO ↑ + H 2 O
Cho m gam Cu tác dụng vừa đủ với V ml dung dịch HNO 3 2M, thu được 4,48 lít khí NO (sản phẩm khử duy nhất ở đktc). Giá trị của V là
A. 400.
B. 200.
C. 800.
D. 100.