500 ml dung dịch NaOH 5M vào 200 ml dung dịch NaOH 30% (d = 1,33) tính C%

Những câu hỏi liên quan
1. Thể tích dung dịch NaOH 0,1M tối thiểu cần cho vào dung dịch hỗn hợp chứa 0,01 mol HCl và 0,02 mol AlCl3 để lượng kết tủa thu được là cực đại bằng? 2. *Cho 500 ml dung dịch Ba(OH)2 0,1M vào V ml dung dịch Al2(SO4)3 0,1M; sau khi các phản ứng kết thúc thu được 12,045 gam kết tủa Giá trị của V là? 3. Hoà tan hoàn toàn 47,4 gam phèn chua KAl(SO4)2.12H2O (K2SO4.Al2(SO4)3.24H2O) vào nước, thu được dung dịch X. Cho toàn bộ X tác dụng với 200 ml...
Đọc tiếp
1. Thể tích dung dịch NaOH 0,1M tối thiểu cần cho vào dung dịch hỗn hợp chứa 0,01 mol HCl và 0,02 mol AlCl3 để lượng kết tủa thu được là cực đại bằng?
2. *Cho 500 ml dung dịch Ba(OH)2 0,1M vào V ml dung dịch Al2(SO4)3 0,1M; sau khi các phản ứng kết thúc thu được 12,045 gam kết tủa Giá trị của V là?
3. Hoà tan hoàn toàn 47,4 gam phèn chua KAl(SO4)2.12H2O (K2SO4.Al2(SO4)3.24H2O) vào nước, thu được dung dịch X. Cho toàn bộ X tác dụng với 200 ml dung dịch Ba(OH)2 1M, sau phản ứng thu được m gam kết tủA. Giá trị của m là?
giải 3 bài trên theo pthh, ko dùng pt ion ạ
B1:
Cho dd NaOH vào hỗn hợp thì dd NaOH sẽ phản ứng với HCl trước sau đó mới phản ứng với muối AlCl3
Để kết tủa là cực đại <=> Không có quá trình hoà tan Al(OH)3
\(NaOH+HCl\rightarrow NaCl+H_2O\\ AlCl_3+3NaOH\rightarrow Al\left(OH\right)_3\downarrow+3NaCl\\ n_{NaOH}=n_{HCl}+3.n_{AlCl_3}=0,01+0,02.3=0,07\left(mol\right)\\ \Rightarrow V_{ddNaOH}=\dfrac{n_{NaOH}}{C_{MddNaOH}}=\dfrac{0,07}{0,1}=0,7\left(lít\right)\)
Đúng 3
Bình luận (0)
2)
\(n_{Al_2\left(SO_4\right)_3}=0,0001.V\left(mol\right)\)
\(n_{Ba\left(OH\right)_2}=0,5.0,1=0,05\left(mol\right)\)
PTHH: \(3Ba\left(OH\right)_2+Al_2\left(SO_4\right)_3\rightarrow3BaSO_4+2Al\left(OH\right)_3\)
0,0003.V<--0,0001.V------>0,0003.V-->0,0002.V
\(2Al\left(OH\right)_3+Ba\left(OH\right)_2\rightarrow Ba\left(AlO_2\right)_2+4H_2O\)
(0,1-0,0006.V)<-(0,05-0,0003.V)
=> 233.0,0003.V + 78.(0,0008.V-0,1) = 12,045
=> V = 150 (ml)
3) \(n_{K_2SO_4.Al_2\left(SO_4\right)_3.24H_2O}=\dfrac{47,4}{948}=0,05\left(mol\right)\)
=> \(\left\{{}\begin{matrix}n_{K_2SO_4}=0,05\left(mol\right)\\n_{Al_2\left(SO_4\right)_3}=0,05\left(mol\right)\end{matrix}\right.\)
\(n_{Ba\left(OH\right)_2}=0,2.1=0,2\left(mol\right)\)
PTHH: \(3Ba\left(OH\right)_2+Al_2\left(SO_4\right)_3\rightarrow3BaSO_4+2Al\left(OH\right)_3\)
0,15<-------0,05----------->0,15----->0,1
\(Ba\left(OH\right)_2+K_2SO_4\rightarrow BaSO_4+2KOH\)
0,05---------------------->0,05--->0,1
\(KOH+Al\left(OH\right)_3\rightarrow KAlO_2+2H_2O\)
0,1--->0,1
=> mkt = mBaSO4 = 0,2.233 = 46,6(g)
Đúng 2
Bình luận (0)
\(n_{Ba\left(OH\right)_2}=0,5.0,1=0,05\left(mol\right)\\3Ba\left(OH\right)_2+Al_2\left(SO_4\right)_3\rightarrow3BaSO_4\downarrow+2Al\left(OH\right)_3\downarrow\\ \)
TH1: Nếu Al(OH)3 không bị hoà tan
\(\Rightarrow m_{kt}=m_{BaSO_4}+m_{Al\left(OH\right)_3}=233.0,05+78.\dfrac{2}{3}.0,05=14,25>10,045\left(loại\right)\)
TH2: Nếu Al(OH)3 bị hoà tan hoàn toàn.
\(2Al\left(OH\right)_3+Ba\left(OH\right)_2\rightarrow Ba\left(AlO_2\right)_2+4H_2O\)
=> \(m_{kt}=m_{BaSO_4}=233.0,05=11,65\left(g\right)< 12,045\left(g\right)\left(loại\right)\)
TH3: Kết tủa bị hoà tan 1 phần
Đặt:
\(n_{Al_2\left(SO_4\right)_3}=a\left(mol\right)\Rightarrow n_{Al^{3+}}=2a\left(mol\right);n_{SO_4^{2-}}=3a\left(mol\right)\\ n_{OH^-}=4.n_{Al^{3+}}-n_{\downarrow}\\ \Leftrightarrow0,1.2.0,5=4.2a-n_{\downarrow}\\ \Leftrightarrow n_{\downarrow}=8a-0,1\\ n_{BaSO_4}=3a\\ m_{\downarrow}=12,045\\ \Leftrightarrow\left(8a-0,1\right).78+3a.233=12,045\\ \Leftrightarrow a=0,015\left(mol\right)\\ \Rightarrow V_{ddAl_2\left(SO_4\right)_3}=\dfrac{0,015}{0,1}=0,15\left(lít\right)\\ \Rightarrow V=150\left(ml\right)\)
Đúng 2
Bình luận (0)
1: Cho 1,8 lít H2O vào 200 ml dung dịch OH nồng độ a mol/lit thu được dung dịch có pH 13. Giá trị của a là A. 1 B. 0,5 C. 1,2 D 1,6 2:Câu 6: Trộn 200 ml dung dịch HCl 0,15M với 300 ml dung dịch NaOH 0,12M, sau đó thêm phenolphtalein vào thì dung dịch sẽ có màu: A. hồng B. tím C. không màu D. đỏ 2: Trộn 200 ml dung dịch HCl 0,15M với 300 ml dung dịch NaOH 0,12M, sau đó thêm phenolphtalein vào thì dung dịch sẽ có màu: ...
Đọc tiếp
1: Cho 1,8 lít H2O vào 200 ml dung dịch OH nồng độ a mol/lit thu được dung dịch có pH = 13. Giá trị của a là A. 1 B. 0,5 C. 1,2 D 1,6
2:Câu 6: Trộn 200 ml dung dịch HCl 0,15M với 300 ml dung dịch NaOH 0,12M, sau đó thêm phenolphtalein vào thì dung dịch sẽ có màu: A. hồng B. tím C. không màu D. đỏ
2: Trộn 200 ml dung dịch HCl 0,15M với 300 ml dung dịch NaOH 0,12M, sau đó thêm phenolphtalein vào thì dung dịch sẽ có màu: A. hồng B. tím C. không màu D. đỏc
Câu 6 :
200ml = 0,2l
300ml = 0,3l
\(n_{HCl}=0,15.0,2=0,03\left(mol\right)\)
\(n_{NaOH}=0,12.0,3=0,036\left(mol\right)\)
Pt : \(HCl+NaOH\rightarrow NaCl+H_2O|\)
1 1 1 1
0,03 0,036
Lập tỉ số só sánh : \(\dfrac{0,03}{1}< \dfrac{0,036}{1}\)
⇒ HCl phản ứng hết , NaOH dư
⇒ Tính toán dựa vào số mol của HCl
Khi thêm phenolplatein vào dung dịch NaOH dư thì dung dịch sẽ có màu đỏ
⇒ Chọn câu : D
Chúc bạn học tốt
Đúng 3
Bình luận (0)
Cần thêm vào bao nhiêu ml dung dịch NaOH 0,25M vào 50 ml dung dịch hỗn hợp HCl 0,1M và H2SO4 0,05M để thu được dung dịch có pH =2 ?
A. 35,5 ml
B. 36,5 ml
C. 37,5 ml
D. 38,5 ml
Cần thêm vào bao nhiêu ml dung dịch NaOH 0,25M vào 50 ml dung dịch hỗn hợp HCl 0,1M và H2SO4 0,05M để thu được dung dịch có pH =2 ?
A. 36,5 ml
B. 73ml
C. 22,4ml
D. 300ml
Đáp án A.
Hướng dẫn :
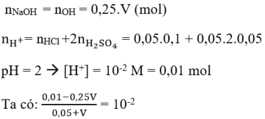
⇒ 0,01 - 0,25.V = 0,01.0,05 + 0,01 V à 0,26.V = 0,01 - 0,01.0,05
⇒ V = 0,0365 l = 36,5 ml
Đúng 0
Bình luận (0)
Cho 100 ml dung dịch CH3COOH a M vào 200 ml dung dịch NaOH 5M . Tính a
CH3COOH+NAOH->CH3COONA+H2O
tính số mol naoh= 5x0,2=1 (mol)
thay số mol naoh vào tìm ra số mol của ch3cooh
tính theo công thức Cm= n/v=1/0,1=10 M
NHƯNG NÓ CÓ CHO PHẢN ỨNG VÙA ĐỦ KHÔNG CHỨ ĐỀ CHUNG QUÁ NHƯNG CHẮC KQ ĐÚNG Á
Đúng 0
Bình luận (0)
Cho 125 ml dung dịch NaOH 2M vào 100 ml dung dịch H2SO4 2M và khuấy đều. Hỏi khi nhúng giấy quỳ tím vào thì giấy quỳ tím chuyển sang màu gì?Nhanh ạ.Cảm ơn vì đã giúp.
Câu 10: 10.1: Cần bao nhiêu ml dung dịch NaOH 3% có khối lượng riêng là 1,05 g/ml và bao nhiêu ml dung dịch NaOH 10% có khối lượng riêng là 1,12 g/ml để pha chế được 2 lít dung dịch NaOH 8% có khối lượng riêng là 1,1 g/ml.10.2: Cho 39,6 gam hỗn hợp KHSO3 và K2CO3 vào 400 gam dung dịch HCl 7,3% sau phản ứng thu được hỗn hợp khí X có tỉ khối với H2 là 25,333 và dung dịch A.a) Hãy chứng minh trong A còn dư axit.b) Tính nồng độ phần trăm các chất trong...
Đọc tiếp
Câu 10: 10.1: Cần bao nhiêu ml dung dịch NaOH 3% có khối lượng riêng là 1,05 g/ml và bao nhiêu ml dung dịch NaOH 10% có khối lượng riêng là 1,12 g/ml để pha chế được 2 lít dung dịch NaOH 8% có khối lượng riêng là 1,1 g/ml.
10.2: Cho 39,6 gam hỗn hợp KHSO3 và K2CO3 vào 400 gam dung dịch HCl 7,3% sau phản ứng thu được hỗn hợp khí X có tỉ khối với H2 là 25,333 và dung dịch A.
a) Hãy chứng minh trong A còn dư axit.
b) Tính nồng độ phần trăm các chất trong A.
10.2 :
a) \(n_{HCl\left(bđ\right)}=0,8\left(mol\right)\)
Giả sử HCl dư
PTHH : \(KHSO_3+HCl-->KCl+SO_2+H_2O\)
\(K_2CO_3+2HCl-->2KCl+H_2O+CO_2\)
Có : \(M_X=25,333\cdot2=50,666\) (g/mol)
Dùng pp đường chéo :
=> nSO2 = \(\dfrac{1}{2}\)nCO2
=> nKHSO3 = \(\dfrac{1}{2}\)nK2CO3
Đặt \(\left\{{}\begin{matrix}n_{KHSO_3}=a\left(mol\right)\\n_{K_2CO_3}=b\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}120a+138b=39,6\\a=\dfrac{1}{2}b\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}a=0,1\\b=0,2\end{matrix}\right.\)
=> \(n_{HCl\left(pứ\right)}=n_{KHSO_3}+2n_{K_2CO_3}=0,5\left(mol\right)\) < 0,8 => HCl dư (giả sử đúng)
b) Theo ĐLBTKL :
\(m_{dd\left(spu\right)}=m_{hh}+m_{ddHCl}-m_X=39,6+400-\left(0,1\cdot64+0,2\cdot44\right)=424,4\left(g\right)\)
Có : \(tổng.n_{KCl\left(spu\right)}=n_{HCl\left(pứ\right)}=0,5\left(mol\right)\)
=> \(\left\{{}\begin{matrix}C\%KCl=\dfrac{74,5\cdot0,5}{424,4}\cdot100\%=8,78\%\\C\%HCl=\dfrac{\left(0,8-0,5\right)\cdot36,5}{424,4}\cdot100\%=2,58\%\end{matrix}\right.\)
Đúng 0
Bình luận (0)
Bài
a, Dẫn 1,68 lít CO2 ở (đktc) sục vào 250 ml dung dịch KO dư. Tính CM của KOH đã phản ứng và của muối tạo thành?
b, Dẫn 28 lít CO2 ở (đktc) vào 300g dung dịch KOH 23%. Tính C% của muối tạo thành?
c, Cho 448 ml CO2 ở (đktc) vào bình chứa 100ml dung dịch NaOH 0,25M. Tính khối lượng muối tạo thành?
a) CO2+2KOH----->K2CO3+H2O
n CO2=1,68/22,4=0,075(mol)
Theo pthh
n KOH=2n CO2=0,15(mol)
CM KOH=0,15/0,25=0,6(M)
b) CO2+2KOH---->K2CO3+H2O(1)
CO2+KOH--->KHCO3(2)
n CO2=28/22,4=1,25(mol)
m KOH=300.23/100=69(g)
n KOH=69/56=1,23(mol)
-->1,23/1,25<1
Tạo 1 muối axit -->xảy ra pư 2
Theo pthh
n KHCO3=n KOH=1,23(mol)
m KHCO3=1,23.100=123(g)
m dd sau pư=300+(1,25.80)=400(g)
C% KHCO3=123/400.100%=30,75%
Chúc bạn học tốt
Thêm từ từ từng giọt của 100 ml dung dịch chứa Na2CO3 1,2M và NaHCO3 0,6M vào 200 ml dung dịch HCl 1M, sau phản ứng hoàn toàn thu được dung dịch X. Cho dung dịch nước vôi trong dư vào dung dịch X thì thu được bao nhiêu gam kết tủa? A. 10 gam. B. 8 gam. C. 12 gam. D. 6 gam.
Đọc tiếp
Thêm từ từ từng giọt của 100 ml dung dịch chứa Na2CO3 1,2M và NaHCO3 0,6M vào 200 ml dung dịch HCl 1M, sau phản ứng hoàn toàn thu được dung dịch X. Cho dung dịch nước vôi trong dư vào dung dịch X thì thu được bao nhiêu gam kết tủa?
A. 10 gam.
B. 8 gam.
C. 12 gam.
D. 6 gam.
Đáp án D
Cho từ từ dung dịch (Na2CO3; NaHCO3) vào dung dịch HCl xảy ra đồng thời các phản ứng (1); (2): (ở đây chú ý tỉ lệ: cứ 1 giọt dung dịch x mol NaHCO3 thì tương ứng chứa 2x mol Na2CO3).
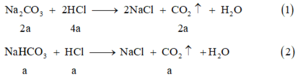
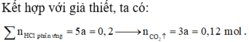
Dung dịch X cho vào dung dịch nước vôi trong dư Ca(OH)2 xảy ra các phản ứng:
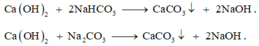
« Nhận xét: Toàn bộ số mol cacbon có trong X đều chuyển hết về kết tủa CaCO3.
Theo đó, bảo toàn nguyên tố cacbon, ta có:
![]()
Theo đó, yêu cầu khối lượng kết tủa thu được là
![]()
Đúng 0
Bình luận (0)






















