1.Hỗn hợp X gồm O2,N2,CO2. Ti lệ mol 2:3:2. Vx=31,36 L.mx=?
2.Hỗn hợp Xgồm FE2O3,CaO. Tỉ lệ mol tương ứng là 1:2. Tính mx
Hỗn hợp khí gồm (N2, O2) có tỉ lệ mol tương ứng là 1: 2. Tính khối lượng mol trung bình của hỗn hợp. Hỗn hợp khí đó nặng hơn khí hiđro bao nhiêu lần?
1. Hỗn hợp X chứa Để và Cu có tỉ lệ mol tương ứng là 1:2. Số mol của Fe và Cu có trong 27,6 g hỗn hợp lần lượt là?
2. Hỗn hợp A chứa Fe, FeO , Fe3O4 , Fe2O3 ( có tỉ lệ mol tương ứng là 1:2:3:4) .Số mol của FeO và Fe2O3 có trong 30,72 g lần lượt là?
3. Cho 24 g hỗn hợp Đi có chứa CuO và Fe2O3 với tỉ lệ mol tương ứng là 1:2. Thành phần % về khối lượng của Fe2O3 và CuO có trong D là?
4. Hỗn hợp X chứa MgCo3 và CaCO3 có tỉ lệ khối lượng tương ứng là 21:25. Số mol của MgCO3 và CaCO3 có trong 18,4 g hỗn hợp X lần lượt là?
5. Cho 27,2 g hỗn hợp A chứa NaOH và KOH có tỉ lệ khối lượng tương ứng là 10:7.Thành phần % về số mol của NaOH và KOH trong hỗn hợp A lần kượt là?
6. Hỗn hợp khí X gồm O2 và Cl2 có tỉ lệ mol tương ứng là 2:1 .Số mol của O2 và Cl2 có trong 10,08 lít khí X (ở đktc) lần lượt là?
7. Hỗn hợp khí X gồm O2 và Cl2 có tỉ khối hơi so vs hiđro là 22,5 .Số mol của O2 và Cl2 có trong 13,44 lít khí X ( ở đktc) lần lượt là?
Mình ghi đáp án thôi nhé
1 .
nFe = 0.15 mol
nCu = 0.3 mol
2.
nFeO = 0.04 mol
nFe2O3 = 0.08 mol
3.
nCuO = 0.06 mol
nFe2O3 = 0.12 mol
4.
nMgCO3 = nCaCO3 = 0.1 mol
5.
nNaOH = 0.4 mol
nKOH = 0.2 mol
%NaOH = 66.67%
%KOH = 33.33%
6.
nO2 = 0.3 mol
nCl2 = 0.15 mol
7.
nO2 = 0.4 mol
nCl2 = 0.2 mol
Cho các peptit X, Y, Z mạch hở, đều chứa gốc Ala trong phân tử, tổng số nguyên tử oxi trong 3 phân tử peptit X, Y, Z là 9. Đốt cháy hoàn toàn 24,42 gam hỗn hợp A gồm X, Y,Z (tỉ lệ số mol tương ứng là 1 : 2 : 2) cần vừa đủ 1,17 mol khí O2 thu được CO2, H2O và N2. Mặt khác, đun nóng 0,07 mol hỗn hợp B gồm X, Y, Z (tỉ lệ số mol tương ứng là 3 : 2 : 2) bằng dung dịch NaOH vừa đủ, cô cạn dung dịch sau phản ứng được m gam hỗn hợp ba muối của glyxin, alanin và valin. Giá trị của m là
A. 19,14
B. 15,40.
C. 16,66
D. 20,48
Chọn đáp án B.
Đipeptit mạch hở tạo từ đồng đẳng của glyxin có dạng CnHmN2O3 => Ít nhất phân tử có 3 oxi
Mà 3 phân tử X,Y,Z lại có tổng số nguyên tử oxi là 9 = 3×3 = Cả 3 chất đều là đipeptit
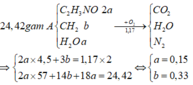
Vì nX : nY : nZ = 1 : 2 : 2 mà nX + nY+ nZ = 0,15 => nX = 0,03; nY = nZ = 0,06
Đặt X là Ala(Gly+xCH2); Y là Ala(Gly+yCH2) và Z là Ala(Gly+zCH2)
=> 0,03x + 0,06y + 0,06z + 0,15 = 0,33 => x + 2y + 2z = 6
Các giá trị x, y, z thuộc 0 (Gly) hoặc 1 (Ala) hoặc 3 (Val)
0,15 + (0,03 + 0,06)×3= 0,42 > 0,33 => Chỉ có 1 trong x, y, z bằng 3 hay chỉ có 1 peptit chứa Val Nếu peptit chứa Val có số mol là 0,03 => x = 3 => 2y + 2z = 3 vô lý vì 2y + 2z phải là số chẵn
=> Y hoặc Z phải chứa Val => Giả sử Z là Ala–Val (hoặc Val–Ala) => z = 3
=> x + 2y = 0 => x = y = 0 => X và Y chỉ khác cách sắp xếp như Gly-Ala và Ala-Gly
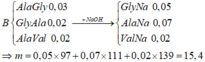
Với thí nghiệm sau, nX : nY : nZ = 3 : 2 : 2 mà nX + nY + nZ = 0,07 => nX = 0,03 và
nY = nZ = 0,02
Vì nY vẫn bằng nZ => Peptit Y hay Z chứa Val đều được
Tính khối lượng mol trung bình của các hỗn hợp khí sau đây:
a) Hỗn hợp gồm H2 và Cl2 có tỉ lệ 1 : 1 về số mol.
b) Hỗn hợp gồm CO và N2 có tỉ lệ 2 : 3 về số mol.
c) Hỗn hợp gồm H2, CO2 và N2 có tỉ lệ 1 :2 :1 về số mol.
Cho biết công thức tính khối lượng mol phân tử trung bình của một hỗn hợp:
MTB= \(\dfrac{M_1\cdot n_1+M_2\cdot n_2+.....}{n_1+n_2+.....}\)
Trong đó:
MTB là khối lượng mol phân tử trung bình của hỗn hợp.
M1, M2... là khối lượng mol của các chất trong hỗn hợp.
n1, n2,... là số mol tương ứng của các chất.
(MỌI NGƯỜI TRẢ LỜI GIÙM MÌNH CÂU THỨ 2 VÀ THỨ 3 THÔI Ạ, THANKS)
Nung nóng hỗn hợp X gồm FeS và FeS2 trong bình kín chứa không khí (gồm 20% thể tích O2 và 80% thể tích N2) đến khi phản ứng xảy ra hoàn toàn, thu được Fe2O3 duy nhất và hỗn hợp khí Y gồm N2, SO2 và O2 có tỉ lệ mol tương ứng 16:2:1. Phần trăm khối lượng của FeS trong X là
A. 59,46%
B. 42,31%
C. 68,75%
D. 26,83%
5. Hỗn hợp A chứa Fe ,FeO , Fe3O4, Fe2O3 ( có tỉ lệ mol tương ứng là 1:2:3:4). Số mol của FeO và Fe2O3 có trong 30,72g A lần lượt là?
9. Cho hỗn hợp X có chứa FeO , Fe3O4 và Fe2O3 với tỉ lệ mol tương ứng là 3:1:2. Thành phần % về khối lượng của Fe3O4 có trong 38,44g X là?
20. Cho 33,6 lít hỗn hợp khí B (đktc) gồm SO2 và O2 có tỉ lệ mol tương ứng là 2:3. Tỉ khối hơi của B số vs khí hiđro là?
5. Hỗn hợp A chứa Fe ,FeO , Fe3O4, Fe2O3 ( có tỉ lệ mol tương ứng là 1:2:3:4). Số mol của FeO và Fe2O3 có trong 30,72g A lần lượt là?
---
Gọi x,2x,3x,4x lần lượt là số mol của Fe,FeO, Fe3O4, Fe2O3 trong 30,72(g) A. (mol) (x>0)
mA= 30,72(g)
<=>mFe+ mFeO+mFe3O4+mFe2O3=30,72
<=> 56x+72.2x+232.3x+160.4x=30,72
<=>1536x=30,72
<=>x=0,02
=>nFeO=2x=0,04(mol)
nFe2O3=4x=0,08(mol)
9. Cho hỗn hợp X có chứa FeO , Fe3O4 và Fe2O3 với tỉ lệ mol tương ứng là 3:1:2. Thành phần % về khối lượng của Fe3O4 có trong 38,44g X là?
Gọi 3x,x,2x lần lượt là số mol FeO, Fe3O4 và Fe2O3 trong 38,44g hhX (x>0)
Ta có: mX= 38,44
<=>mFeO+mFe3O4+mFe2O3=38,44
<=>3x.72+x.232+2x.160=38,44
<=> 768x=38,44
<=> x=961/19200
=> \(\%mFe3O4=\frac{\frac{961}{19200}.232}{38,44}.100\approx30,208\%\)
20. Cho 33,6 lít hỗn hợp khí B (đktc) gồm SO2 và O2 có tỉ lệ mol tương ứng là 2:3. Tỉ khối hơi của B số vs khí hiđro là?
---
nB= 1,5(mol)
nSO2= 2/5 . 1,5=0,6(mol)
nO2= 1,5 - 0,6=0,9(mol)
-> \(\overline{M}_B=\frac{m_B}{n_B}=\frac{m_{SO2}+m_{O2}}{n_B}=\frac{0,6.64+0,9.32}{1,5}=44,8\left(\frac{g}{mol}\right)\\ \rightarrow d_{\frac{B}{H_2}}=\frac{\overline{M}_B}{M_{H_2}}=\frac{44,8}{2}=22,4\)
Hỗn hợp khí X gồm O2, CO2 và khí Y chưa biết có tỉ khối đối với hidro là 26. Tỉ lệ số mol của 3 khí tương ứng là 1 : 2: 3. Tổng khối lượng hỗn hợp X là 31,2 gam.
a/ Tìm khối lượng mol của khí Y.
b/ Trong phân tử Y, số hạt mang điện gấp 2 lần số hạt không mang điện. Phân tử Y có 3 nguyên tử của 2 nguyên tố, 2 nguyên tử của 2 nguyên tố này có số proton gấp đôi nhau. Tìm CTHH của Y.
c/ Hỗn hợp T gồm N2 và C2H4. Cần trộn thêm bao nhiêu gam T vào 31,2 gam X để được hỗn hợp Z có tỉ khối đối với heli là 10,6?
a) Gọi số mol O2, CO2, Y là a, 2a, 3a (mol)
\(\overline{M}_X=26.2=52\left(g/mol\right)\)
=> \(n_X=\dfrac{31,2}{52}=0,6\left(mol\right)\)
=> a + 2a + 3a = 0,6
=> a = 0,1
Có: 0,1.32 + 0,2.44 + 0,3.MY = 31,2
=> MY = 64 (g/mol)
b) Giả sử Y tạo bởi 2 nguyên tố A, B
CTHH: A2B
Do số hạt mang điện gấp 2 lần số hạt không mang điện
=> 4pA + 2pB = 2.(2nA + nB)
=> 2pA + pB = 2nA + nB (1)
MY = 64 (g/mol)
=> 2.MA + MB = 64
=> 2(pA + nA) + pB + nB = 64
=> 2pA + pB + 2nA + nB = 64 (2)
Thay (1) vào (2)
=> 4pA + 2pB = 64
=> 2pA + pB = 32
- TH1: Nếu pA = 2.pB
=> pA = 12,8 (L)
- TH2: Nếu 2.pA = pB
=> pA = 8(Oxi); pB = 16 (Lưu huỳnh)
=> CTHH có dạng O2S hay SO2
c) \(\overline{M}_T=28\left(g/mol\right)\)
Gọi khối lượng T cần thêm là a (g)
=> \(n_T=\dfrac{a}{28}\left(mol\right)\)
mZ = 31,2 + a (g)
nZ = \(0,6+\dfrac{a}{28}\left(mol\right)\)
=> \(\overline{M}_Z=\dfrac{31,2+a}{0,6+\dfrac{a}{28}}=10,6.4=42,4\left(g/mol\right)\)
=> a = 11,2 (g)
a) Gọi số mol O2, CO2, Y là a, 2a, 3a (mol)
¯¯¯¯¯¯MX=26.2=52(g/mol)M¯X=26.2=52(g/mol)
=> nX=31,252=0,6(mol)nX=31,252=0,6(mol)
=> a + 2a + 3a = 0,6
=> a = 0,1
Có: 0,1.32 + 0,2.44 + 0,3.MY = 31,2
=> MY = 64 (g/mol)
b) Giả sử Y tạo bởi 2 nguyên tố A, B
CTHH: A2B
Vì số hạt mang điện gấp 2 lần số hạt không mang điện
=> 4pA + 2pB = 2.(2nA + nB)
=> 2pA + pB = 2nA + nB (1)
MY = 64 (g/mol)
=> 2.MA + MB = 64
=> 2(pA + nA) + pB + nB = 64
=> 2pA + pB + 2nA + nB = 64 (2)
Thay (1) vào (2)
=> 4pA + 2pB = 64
=> 2pA + pB = 32
- TH1: Nếu pA = 2.pB
=> pA = 12,8 (L)
- TH2: Nếu 2.pA = pB
=> pA = 8(Oxi); pB = 16 (Lưu huỳnh)
=> CTHH có dạng O2S hay SO2
c) ¯¯¯¯¯¯MT=28(g/mol)M¯T=28(g/mol)
Gọi khối lượng T cần thêm là a (g)
=> nT=a28(mol)nT=a28(mol)
mZ = 31,2 + a (g)
nZ = 0,6+a28(mol)0,6+a28(mol)
=> ¯¯¯¯¯¯MZ=31,2+a0,6+a28=10,6.4=42,4(g/mol)M¯Z=31,2+a0,6+a28=10,6.4=42,4(g/mol)
=> a = 11,2 (g)
Bài 2: Trong một bình kín thể tích 56 lít chứa hỗn hợp khí A gồm N2 và H2 theo tỉ lệ mol là 1:4 ở 0oC và 200 atm.
Tính số mol khí của hỗn hợp A.
Tính số mol mỗi khí có trong hỗn hợp ban đầu.
Bài 3: Một hỗn hợp X gồm NH3 và O2 theo tỉ lệ mol 2:5 chiếm thể tích là 62,72 lít ở 0oC và 2,5 atm. Tính số mol NH3 và O2 trong hỗn hợp.
Bài 4. Một hỗn hợp gồm O2, O3 ở điều kiện tiêu chuẩn có tỉ khối đối với hiđro là 18. Thành phần % về thể tích của O3 trong hỗn hợp là:
A. 15% | B. 25% | C. 35% | D. 45% |
Bài 5. Tỉ khối hơi của N2 và H2 so vs O2 là 0,3125. Thành phần % thể tích của N2 trong hỗn hợp là bao nhiêu?
Bài 6. Để thu được dung dịch HCl 25% cần lấy m1 gam dung dịch HCl 45% pha với m2 gam dung dịch HCl 15%. Tỉ lệ m1/m2 là:
A. 1:2 | B. 1:3 | C. 2:1 | D. 3:1 |
Bài 7: Để pha được 500 ml dung dịch nước muối sinh lí (C = 0,9%) cần lấy V ml dung dịch NaCl 3%. Giá trị của V là:
A. 150 | B. 214,3 | C. 285,7 | D. 350 |
Bài 8: Cho m (g) Fe tác dụng vừa đủ với 182,5g dung dịch HCl 10% thu dung dịch A và V lít khí H2 (ở đkc).
Tìm m, V?
Xác định khối lượng dung dịch A.
Tìm nồng độ phần trăm của dung dịch A thu được.
Bài 9: Cho m (g) Fe2O3 tác dụng vừa đủ với 400ml dung dịch HCl 1,5M thu được dung dịch A.
Xác định m.
Tìm nồng độ mol của dung dịch A, coi thể tích dung dịch thay đổi không đáng kể
Bài 10: Cho 13g kẽm tan hoàn toàn trong dung dịch HCl 20% vừa đủ thu được dung dịch X và V lít khí H2.
Viết phương trình phản ứng.
Tính nồng độ phần trăm của dung dịch A.
Em tách bài ra nha 1-2 bài/1 câu hỏi để nhận được hỗ trợ nhanh nhất nha.
Hỗn hợp A gồm 3 peptit mạch hở X, Y và Gly-Ala-Gly (trong đó X, Y có cùng số liên kết peptit và đều được tạo thành từ alanin và valin, MX > MY) có tỉ lệ mol tương ứng là 2 : 3 : 1. Đốt cháy hoàn toàn 76,08 gam hỗn hợp A cần 4,356 mol O2 và sinh ra 10,2144 lít N2 (đktc). Số nguyên tử hiđro trong phân tử Y là
A. 53.
B. 57.
C. 45.
D. 65.
Chọn C.
Quy đổi hỗn hợp thành C2H3ON (0,912 mol), CH2 (x mol), H2O (y mol) Ta có:
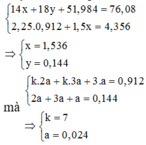
Þ X, Y là heptapeptit
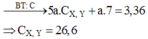
ÞY là (Ala)5(Val)2 có 45H.