Cho 16,6g C2H5OH và CH3COOH vào Mg thu được 2,24l khí (đktc) Tính Khối lượng mỗi chất trong hỗn hợp thu đc

Những câu hỏi liên quan
Cho 10g hỗn hợp Cu và Mg vào H2So4 loãng dư sau phản ứng thu được 2,24l khí (đktc). Tính phần trăm khối lượng Cu trong hỗn hợp ban đầu
Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: Cu + H2SO4 ---x--->
Mg + H2SO4 ---> MgSO4 + H2
Theo PT: \(n_{Mg}=n_{H_2}=0,1\left(mol\right)\)
=> \(m_{Mg}=0,1.24=2,4\left(g\right)\)
=> \(m_{Cu}=10-2,4=7,6\left(g\right)\)
=> \(\%_{m_{Cu}}=\dfrac{7,6}{10}.100\%=76\%\)
Đúng 1
Bình luận (0)
cho 40,5 g hỗn hợp Natri và Natri oxit vào nước( dư). Sau phản ứng thấy thoát ra 2,24l khí H2 (đktc)
a) Lập PTHH
b) Tính khối lượng mỗi chất trong hỗn hợp
c) Tính khối lượng bazơ thu được
a)\(n_{H_2}=\dfrac{2,24}{22,4}=0,1mol\)
\(2Na+2H_2O\rightarrow2NaOH+H_2\)
0,2 0,1
\(NaO+H_2O\rightarrow2NaOH\)
b)\(m_{Na}=0,2\cdot23=4,6g\)
\(m_{NaO}=m_{hh}-m_{Na}=40,5-4,6=35,9g\)
c)\(n_{NaO}=\dfrac{35,9}{39}=0,92mol\Rightarrow n_{NaOH}=2n_{NaO}=1,84mol\)
\(\Rightarrow m_{NaOH}=1,84\cdot40=73,6g\)
Đúng 1
Bình luận (1)
cho 9,6g hỗn hợp canxi và canxi oxit vào nước(Dư), phản ứng kết thúc thu được 2,24l khí H2 ở đktc.
a) lập pthh
b) tính khối lượng mỗi chất trong hỗn hợp ban đầu
c) tính khối lượng dd bazơ thu được
\(a.Ca+H_2O\rightarrow Ca\left(OH\right)_2+H_2\\ CaO+H_2O\rightarrow Ca\left(OH\right)_2\\ b.n_{H_2}=n_{Ca}=0,1\left(mol\right)\\ \Rightarrow m_{Ca}=0,1.40=4\left(g\right)\\ \Rightarrow m_{CaO}=9,6-4=5,6\left(g\right)\\ c.n_{CaO}=\dfrac{5,6}{56}=0,1\left(mol\right)\\ \Sigma n_{Ca\left(OH\right)_2}=n_{Ca}+n_{CaO}=0,1+0,1=0,2\left(mol\right)\\ \Rightarrow m_{Ca\left(OH\right)_2}=0,2.74=14,8\left(g\right)\)
Đúng 4
Bình luận (0)
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ pthh:Ca+2H_2O\rightarrow Ca\left(OH\right)_2+H_2\)
0,1 0,1 0,1
\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)(2)
\(m_{Ca}=0,1.40=4\left(g\right)\\
m_{CaO}=9,6-4=5,6\left(g\right)\)
\(n_{CaO}=\dfrac{5,6}{56}=0,1\left(mol\right)\\
n_{Ca\left(OH\right)_2\left(2\right)}=n_{CaO}=0,1\left(mol\right)\)
\(n_{Ca\left(OH\right)_2}=\left(0,1+0,1\right).74=14,8\left(g\right)\)
Đúng 1
Bình luận (0)
Một hỗn hợp gồm
C
H
3
C
O
O
H
và
C
2
H
5
O
H
có khối lượng 10,6 g, khi tác dụng hết với Na thu được 2,24 lít khí (đktc). Khối lượng
C
H
3
C
O
O
H
trong hỗn hợp đầu là (Cho H1, C12, O16) A. 3,6 g B. 4,6 g C. 6 g D. 0,6 g
Đọc tiếp
Một hỗn hợp gồm C H 3 C O O H và C 2 H 5 O H có khối lượng 10,6 g, khi tác dụng hết với Na thu được 2,24 lít khí (đktc). Khối lượng C H 3 C O O H trong hỗn hợp đầu là (Cho H=1, C=12, O=16)
A. 3,6 g
B. 4,6 g
C. 6 g
D. 0,6 g
cho 7,2g hỗn hợp Fe và Fe2CO3 tác dụng hết với 94,9 dung dịch HCL thu được dung dịch A và 2,24l khí B(đktc)
a/tính%khối lượng mỗi chất trong hỗn hợp đồng
b/ tính C% các chất trong dung dịch A
\(a/n_{khí}=\dfrac{2,24}{22,4}=0,1mol\\ n_{Fe}=a;n_{FeCO_3}=b\\ Fe+2HCl\rightarrow FeCl_2+H_2\\ FeCO_3+2HCl\rightarrow FeCl_2+CO_2+H_2O\\ \Rightarrow\left\{{}\begin{matrix}56a+116b=7,2\\a+b=0,1\end{matrix}\right.\\ \Rightarrow a=\dfrac{11}{150};b=\dfrac{2}{75}\\ \%m_{Fe}=\dfrac{11:150.56}{7,2}\cdot100\%=57,04\%\\ \%m_{FeCO_3}=100\%-57,04\%=42,96\%\\ b/n_{FeCl_2}=\dfrac{11}{150}+\dfrac{2}{75}=0,1mol\\ C_{\%FeCl_2}=\dfrac{0,1.127}{7,2+94,9-\dfrac{11}{150}\cdot2-\dfrac{2}{75}\cdot44}\cdot100\%=12,6\%\)
Đúng 3
Bình luận (0)
cho 25.8 hỗn hợp C2H5OH và C3COOH tác dụng vừa đủ với Kali thu được 5,6 lít khí H2 (đktc)
a) viết các phương trình hoá học
b) tính khối lượng mỗi chất trong hỗn hợp
Đề là: `C_2 H_5 OH` và `CH_3 COOH` nhỉ?
-Giải-
`a)PTHH:`
`C_2 H_5 OH+K->C_2 H_5 OK+1/2H_2 \uparrow`
`CH_3 COOH+K->CH_3 COOK+1/2H_2 \uparrow`
`b)n_[H_2]=[5,6]/[22,4]=0,25(mol)``
Gọi `n_[C_2 H_5 OH]=x;n_[CH_3 COOH]=y`
`=>` $\begin{cases} 46x+60y=25,8\\\dfrac{1}{2}x+\dfrac{1}{2}y=0,25 \end{cases}$
`<=>` $\begin{cases} x=0,3\\y=0,2 \end{cases}$
`@m_[C_2 H_5 OH]=0,3.46=13,8(g)`
`@m_[CH_3 COOH]=25,8-13,8=12(g)`
Đúng 1
Bình luận (0)
Hoà tận hoàn toàn 9,4 gam hỗn hợp Mg và MgO vào dung dịch HNO3 loãng dư thu được 336ml khí NO duy nhất (đktc) tính phần trăm khó lượng mỗi chất trong hỗn hợp ban đầu và khối lượng muối thu được sau phản ứng
Xem chi tiết
PTHH: \(MgO+2HNO_3\rightarrow Mg\left(NO_3\right)_2+H_2O\) (1)
\(3Mg+8HNO_3\rightarrow3Mg\left(NO_3\right)_2+2NO+4H_2O\) (2)
Ta có: \(n_{NO}=\dfrac{0,336}{22,4}=0,015\left(mol\right)\) \(\Rightarrow n_{Mg}=0,0225\left(mol\right)\)
\(\Rightarrow\%m_{Mg}=\dfrac{0,0225\cdot24}{9,4}\cdot100\%\approx5,74\%\) \(\Rightarrow\%m_{MgO}=94,26\%\)
Theo PTHH: \(\left\{{}\begin{matrix}n_{Mg\left(NO_3\right)_2\left(2\right)}=0,0225mol\\n_{Mg\left(NO_3\right)_2\left(1\right)}=n_{MgO}=\dfrac{9,4-m_{Mg}}{40}=0,2215\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\Sigma n_{Mg\left(NO_3\right)_2}=0,244\left(mol\right)\) \(\Rightarrow m_{Mg\left(NO_3\right)_2}=0,244\cdot148=36,112\left(g\right)\)
Đúng 2
Bình luận (0)
Khi cho 5,30 gam hỗn hợp gồm etanol C2H5OH và propan-1-ol CH3CH2CH2OH tác dụng với natri (dư) thu được 1,12 lít khí (đktc).Tính thành phần phần trăm khối lượng của mỗi chất trong hỗn hợp.
Gọi số mol của etanol là x của propan-1-ol là y (mol)
Theo (1) và (2) ta có hệ phương trình:
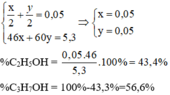
Đúng 0
Bình luận (0)
Cho 6g hỗn hợp bột gồm Mg và oxit của nó tác dụng với dung dịch HCl vừa đủ thu được 2,24l khí H2 (ở đktc). Tính phần trăm về khối lượng của MgO có trong hỗn hợp
nH2=2.24/22.4=0.1 mol
pt: Mg+2HCL->MgCl2+H2
nMg=nH2=0.1 mol
mMg=0.1*24=2.4g
=>mMg=6-2.4=3.6g
%mMg=(3.6/6)*100=60%
Đúng 0
Bình luận (1)
\(n_{H_2}=\dfrac{2.24}{22.4}=0,1\left(mol\right)\)
Ta có phương trình hoá học sau:
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(n_{Mg}=n_{H_2}=0,1\left(mol\right)\)
\(m_{Mg}=0,1.24=2,4\left(g\right)\)
\(\Rightarrow m_{Mg}=6-2,4=3,6\left(g\right)\)
\(\Rightarrow\%m_{Mg}=\dfrac{3,6}{6}.100=60\%\)
Chúc bạn học tốt nha!!!
Đúng 0
Bình luận (0)

























